могут превращаться в другие молекулы, при этом изменений в
АТОМАХ не происходит. Это называется химическая реакция.О, об этом мы тоже поговорим. В свое время.
Однако, даже не меняя ничего в своем МОЛЕКУЛЯРНОМ составе, вещества способны преподнести вам немало сюрпризов.
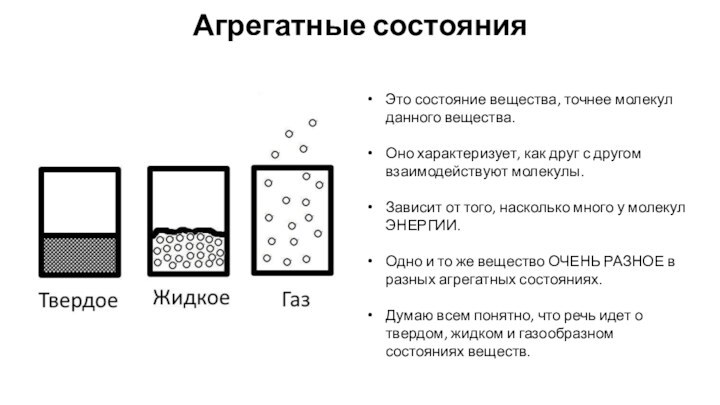
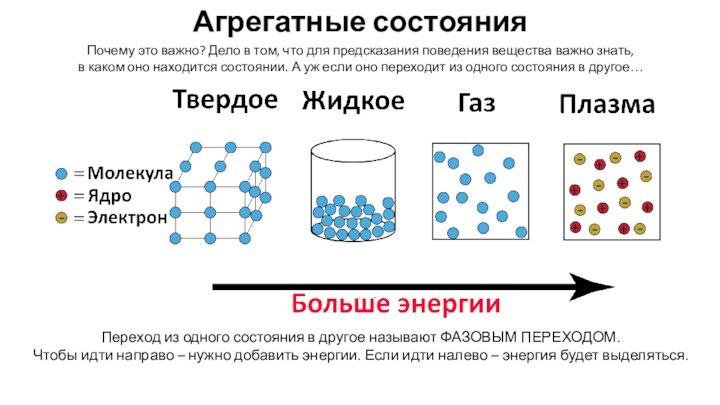
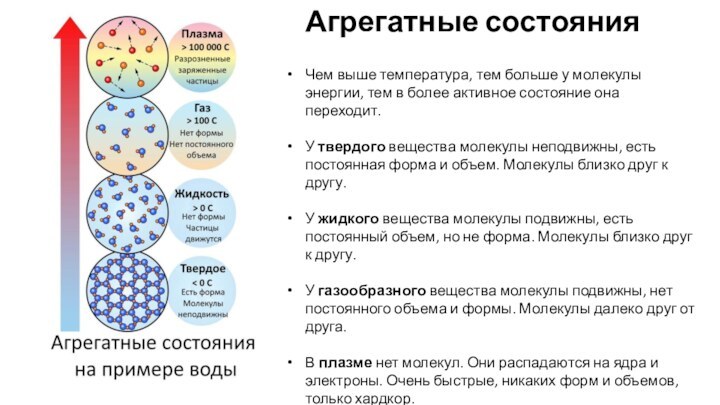
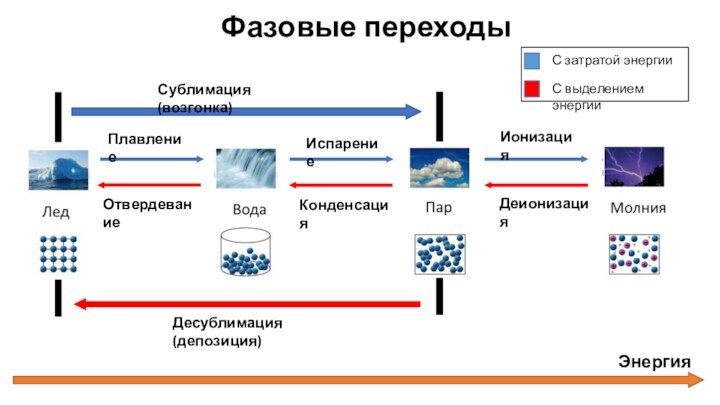
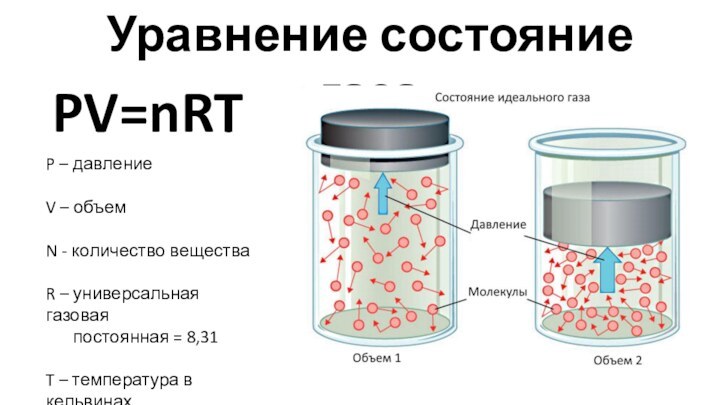
И первый из них – это АГРЕГАТНЫЕ СОСТОЯНИЯ!