Слайд 4
Кристалдық тордың түйіндеріндегі атомдардан бөлінген электрондар
оның барлық құрылымдық бөліктеріне ортақ күйге көшеді. Кристалдың ішінде
еркін орын ауыстыратын электрондар ондағы бүкіл атомдар мен иондарды өзара байланыстырады. Мұндай кристалдардың түйіндегі өзара байланыстырады. Мұндай кристалдың түйініндегі атомдар мен иондар арасында еркін қозғалыста болатын электрондарды «электрон газы» деп те атайды.
Металдық байланыс дегеніміз – металдық тор түйіндеріндегі атомдар мен оң зарядталған иондар және электрон газы (бос электрондардан тұратын) арасында түзілетін байланыс.
Теріс зарядталған ортақтасқан электрондардың жиынтығы оң зарядталған металл иондары – катиондарды және тордың түйіндеріндегі атомдарды өзара байланыстырып, берік ұстап тұрады. Осылайша металдық кристалдық тор пайда болады.

Металдардың физикалық қасиеттері
Металл кристалындағы атомдар, иондар «электрон газымен» берік ұстасып, металдық байланыс түзеді дедік. Кристалдағы бос электрондарға тәуелді металдар белгілі бір ортақ қасиеттерге ие болады. Бұл қасиеттерге жылу және электрөткізгіштік, металдық жылтыр, иілімділік, т.б. қасиеттері жатады.
Электр және жылуөткізгіштігі. Электр өрісінің әсерінен электрондар бағытты қозғалысқа ие болады, сөйтіп электр тогы пайда болады. Электрөткізгіштігі ең жоғары металдар күміс пен мыс, одан кейін алтын, алюминий, темір болып келеді. Ең электрөткізгіштік сынапқа тән
Көптеген металдардың жылуөткізгіштігінің өзгеру реті электрөткізгіштігінің өзгеру ретімен сай келеді. Жылуөткізгіштік те электрөткізгіштік тәрізді электрондардың қозғалғыштығына және кристалдағы бөлшектердің тербелмелі қозғалысына тәуелді. Осы құбылыстардың арқасында металл кесегіндегі қызу бөлшектердің бірінен-біріне беріліп, өзара тез теңеседі. Мысалы, күміс қасық шыны стаканға қарағанда жылуды 500 еседей тез өткізеді.
Металдық жылтыры. Бұл металдардың өзіне тәе қасиеттерінің бірі – оны адамдар өте жоғары бағалап, кейбір көркемөнер туындыларын жасауға пайдаланады. Металдың бәрі де жалтырайды, бірақ мөлдір емес, өзіндік жылтыры бар. Олар көбіне сұр түсті болып келеді. Бұлай болу себебі, металл кристалдарының ішіндегі бос кеңістікте электрондар бар, олар күн сәулесін жұтып тербеліске ұшырайды да, өзіне тән толқындар шығара бастайды, оған сәйкес түсті адам көзбен көреді.
Металдар радиотолқындарды да шағылыстырады, сондықтан оны металл денелерді анықтауға арналған радиолокацияда пайдаланады.
Слайд 6
Иілімділігі (пластикалығы). Металдарды соққанда, ұсақ түйіршіктерге

бөлініп шашырап қалмайды, небәрі пішінін өзгертіп тапталады не жаншылады,
яғни соғуға төзімді пластикалық қасиетін – иілімділігін көрсетеді. Олай болатын себебі, атомдар қабаттары металдық байланысты сақтай отырып бірінің бетінде бірі сырғып жылжи алады. Металл кесегіндегі электрондар, оның өне бойымен бірге қозғалып, сырғыған қабаттарды үнемі байланыстырып тұрады.
Металдардың мілімділігі мынадай қатар бойынша кемиді: Au, Ag, Cu, Sn, Pb, Zn, Fe. Мысалы, алтынды таптап, қалыңдығы 0,003 мм жұқа қабықшаға айналдыруға болады. Оны әртүрлі денелерге алтын «жалатқанда» қолданады.
Металдар иілімділігінің әралуандығы олардың кристалдық торы құрылысының әртүрлі болуына тәуелді. Металдар куб (бүйірлі және көлемді орталықтанған) және гексагональды торлар түзе алады.
Кубтық торлы металдар иілімділеу болады, себебі олардың атомдық қабаты жоғары да, төмен де, көлденең бағытта да сырғи алады. Ал гексагональды торлы металдар бір жазықтық бойынша сырғиды, сондықтан иілімділігі аздау болады.
Металдардың жалпы қасиеттерімен бірге әрқайсысының өзіне тән қасиеттері де бар. Оның себебі металдардың атомдары мен иондарының радиустары әртүрлі және олардың кеңістікте орналасуы да түрліше. Металдардың валенттік электрондары мен металдық байланысының беріктігі де бірдей емес.
Балқу температуралары. 1000 С-тан жоғары температурада балқитын металдарды қиын балқитындар, ал одан төмен болса, оңай балқитындар деп бөледі. Ең оңай балқитын металл – сынап, оның балқу температурасы -38,9С. Ең қиын балқитын
Слайд 9
Атомдары берген электрондарды қосып алатын атомдар немесе иондар
атқарады. Металдар және олармен әрекеттесетін тотықтырғыш заттардың арасында реакция
түрлері:
Слайд 11
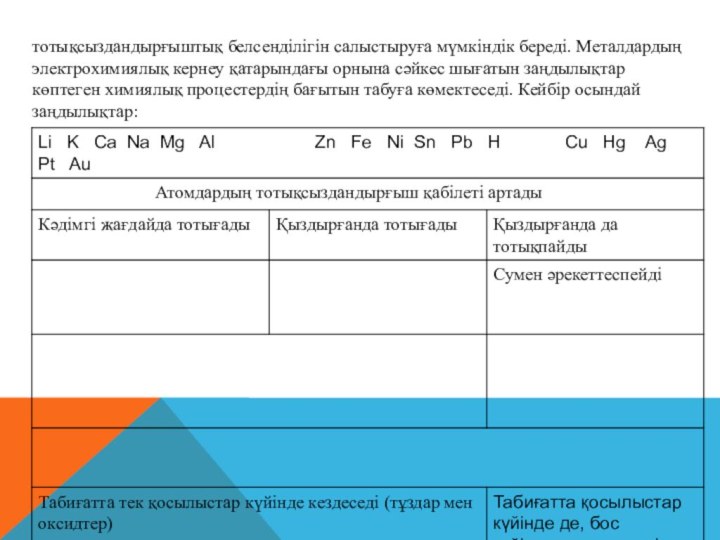
тотықсыздандырғыштық белсенділігін салыстыруға мүмкіндік береді. Металдардың
электрохимиялық кернеу
қатарындағы орнына сәйкес шығатын заңдылықтар көптеген химиялық процестердің бағытын
табуға көмектеседі. Кейбір осындай заңдылықтар:
Слайд 12
Металдардың кернеу қатарын қолданғанда, олардың

қасиеттеріндегі кейбір ерекшеліктерді есте сақтау керек. Мысалы, ең белсенді
металдар – Li, K, Ca, Na, Sr, Ba белсенділігі төмендеу металдардың судағы ерітіндісінен оларды ығыстырып шығаруға қолданылмайды, себебі сілтілік және сілтілік жер металдар кәдімгі жағдайда судың өзімен қарқынды әрекеттесетіні белгілі.
Металдардың адам өміріндегі маңызы
Металдар адамзат қоғамына ерте заманнан белгілі. Өркениетті өндірістің дамуына сәйкес және адамдардың металды игеру мен қолдануына орй тарихта бүтіндей металл дәуірінің аты қалды. Геология мен металлургияның негізін салған, металдарды зерттеуші Георгий Агрикола XVI ғасырда былай деп жазды: «Адамдар металдарсыз өмір сүре алмайды ... егер металдар болмаса ... Адамдар жабайы аңдардыі арасында ең аянышты өмір сүрген болар еді».
Тас ғасырда-ақ алғашқы табылған металдар сом күйдегі тума алтын мен күміс болатын. «Металдар» деген сөздің өзі ертедегі гректің осыған үндес «іздеу» деген сөзінен шығуы мүмкін. Адамзат қоғамы бертін келе металдарды табиғи қосылыстарынан бөліп алуды үйренді. Мәселен, мыс біздің заманымызға дейінгі III мыңжылдықта оның орнына мысқа қарағанда беріктеу қоланы бастады. Сөйтіп, мыс дәуірінің орнын қола дәуірі басты.
Адам алғаш рет таза темірмен аспаннан түскен метеориттің сынығы арқылы танысты. Темірді балқытып бөліп алудың құпиясы біздің заманымызға дейінгі 1500 жылдарда Кіші Азияда ашылды, содан бастап темір дәуірі басталды.
Слайд 13
Біздің заманымыздың бас кезінде небәрі

7 металл белгілі болса, XVIII ғасырда 17 металл ашылды.
Басқа металдарды алу үшін ғылым мен техниканың, өнеркәсіптің дамуы қажет еді. Бұл процесс күні бүгінге дейін жалғасып келеді. Мәселен, ядролық реакцияның көмегімен табиғатта кездеспейтін көптеген радиоактивті жасанды элементтер алынды.
Металдар қосылыстарының литосфера мен биосферадағы орны. Қазіргі адамзат қоғамының дамуы үшін металдардың маңызы орасан зор. Бүгінгі күндері таңғажайып қасиеттері бар синтетикалық заттардың сан алуан түрі өндірілгеніне қарамастан, металдар осы заманғы техникаға қажетті ең маңызды конструкциялық материал болып отыр. Олар автомобильдердің, ұшақтардың, зымырандардың, станоктардың, өте дәл құралдардың және электрондық техниканың негізі болып саналады. Металдар – құрылыстың, технологияның конструкциялардың, химиялық реакциялардың, құбырлардың, мұнай өндіретін мұнаралардың және т.б. негізгі өзегі. Қазіргі кезде техникада 40-тан астам металдар кеңінен қолданылады.
Металдар – жай заттар ғана емес, олар химиялық элементтер. Осы элементтер тірі және өлі табиғаттың аса маңызды құрамды бөлігі болып табылады. Жердің беткі қабаты – литосфера: алюминий, темір, кальций, магний, натрий, калий қосылыстарынан тұрады. Бұл химиялық элементтер оттек пен кремнийді қоса алғанда жер массасының 99%-ын құрайды. Теңіздер мен мұхиттардың суында, нптрий, магний, кальций, стронций, алтын, т.б. металдардың катиондары бар.