Слайд 2
Представители педагогической науки
А.В.Дистервег /29.10.1790 – 07.07.1866/
В.А.Сухомлинский /28.09.1918 –
02.09.1970/
К.Д.Ушинский /19.02.1824 – 22.12.1870/
Д.И.Менделеев /27.01.1834 – 20.01.1907/
А.М. Бутлеров /03.09.1828
– 05.08.1886/
П.Н.Лебедев /24.02.1866 – 01.03.1912/
И.И.Мечников /03.05.1845 – 02.07.1916/
И.М.Сеченов /01.08.1829 – 02.11.1905/
Химия – наука о веществах, их свойствах и превращениях
Химическая реакция - превращение,
в результате которого из одних веществ получаются другие, новые вещества, отличающиеся от исходных по составу и свойствам
Слайд 3
Пояснительная записка
Методическая разработка темы «Изменение, происходящие с веществами»
предназначена для учащихся 8 классов. Она составлена на основе
программы курса химии для 8-11 классов общеобразовательных учреждений автора О.С.Габриелян.
Тема является одной из важных курса химии, так как знание типов химических реакций и закона сохранения массы веществ дает возможность управлять превращениями веществ, находить экономически безопасные способы производства веществ и материалов и охраны окружающей среды от химических загрязнений.
Освоение важных знаний и овладение умениями и навыками по теме служит фундаментом для изучения дальнейшего курса химии.
Слайд 4
Актуальность
понятие
Химическая реакция
Форма движения материи
Формирование целостной картины мира
основное
важное
Слайд 5
Принципы отбора содержания
преемственность
принцип доступности и последовательности
принцип научности
формирование предметной компетенции
единство содержания и
методики преподавания
учёт возрастных особенностей учащихся
принцип познавательной активности, самостоятельности, творчества
принцип разнообразия учебной деятельности
формирование рефлексивных качеств
Слайд 6
Система формирования знаний и умений учащихся
Уровни усвоения учебной
информации
Психолого – педагогические особенности
подросткового возраста
Быстрый рост, развитие и
перестройка организма ребенка.
Стремление к познанию, активность, инициативность, упорство в достижении цели.
Увеличение объема памяти, избирательность внимания.
Формирование активного самостоятельного, творческого мышления.
Нарастание способностей к абстрактному мышлению.
Слайд 7
Система деятельности учителя по формированию
знаний и умений
Формирование

знаний учебного материала.
Формирование умений и навыков.
Формирование понимания изучаемого материала.
Развитие
внимания.
Развитие мировоззрения.
Постановка цели
Организация деятельности
Формирование знаний учебного материала
- Найдите в тексте ключевые слова.
- Разбейте текст на смысловые части.
- Найдите дополнительный материал в других источниках информации.
Формирование понимания изучаемого материала
- Составьте вопросы по данной теме.
- Ответьте на вопросы, отражающие причинно-следственные связи: «Почему?», «Зачем?»
- Перекодируйте словесную информацию в виде схемы, таблицы.
Формирование умений и навыков
- Установите, какие знания необходимо использовать для выполнения данного задания.
- Ответьте на вопрос «Почему?» и «Как?», связанные с каким-либо действием и способом его осуществления.
Развитие внимания
- Найдите ошибку в тексте, схеме, ответе одноклассника.
- Установите последовательность каких-либо действий.
Развитие мировоззрения
- Привести примеры объектов или процессов действительности, описываемых данным явлением.
- Составить содержательную прикладную задачу.
Слайд 8
Цели обучения
Познакомить учащихся с классификацией химических
реакций и основным законом химии (закон сохранения массы веществ).
Научить
различать физические и химические явления, составлять уравнения химических реакций, определять типы химических реакций, делать вычисления по химическим уравнениям реакций.
Совершенствовать умения обращаться с химической посудой и лабораторным оборудованием.
Показать возможность использования приобретенных знаний и умений в практической деятельности и повседневной жизни для безопасного обращения с веществами и материалами; очистки загрязненных веществ от примесей.
Слайд 9
Задачи
Образовательные
Развивающие
Воспитательные
Закрепить знания учащихся о физических и химических
явлениях;
сформировать

представление о классификации химических
реакций;
сформировать первоначальные умения и
навыки решения основных типов задач по химии.
Развивать эмоциональное
восприятие у учащихся,
используя мультимедиа;
развить познавательный интерес, используя в содержании уроков элементов новизны знаний и умений, устанавливая связь изученного материала с жизнью;
развить практические умения учащихся при выполнении экспериментальных задач;
развить у школьников умение выделять главное, существенное в изученном материале, сравнить, обобщить изученные факты, логически излагать свои мысли при решении задач.
Продолжить формирование научного мировоззрения, таких качеств личности, как ответственное отношение к порученному делу, умение объективно оценивать результаты своего труда;
продолжить формирование мотивации учебной деятельности;
продолжить формирование представлений о положительной роли химии для объяснения происходящих процессов в природе и в организме человека.
Слайд 10
Результаты обучения
Будут знать
Будут уметь
сущность химических
реакций
классификацию
химических реакций
по различным признакам
взаимосвязь химических
превращений между
неорганическими и
органическими
веществами
распознавать
химические реакции
по типам
объяснять механизмы
протекания
химических реакций
решать задачи
различных типов
Слайд 11
Технология и формы организации деятельности
Классно-урочная система
урок
домашняя
работа
внеклассная работа
Лекционно-семинарская система
лекция
семинар
зачёт
консультация
практикум
экзамены
собеседование
ИКТ (информационно коммуникативные технологии)
Здоровьесберегающие технологии
(комбинированный, сообщения новых знаний, формирования и закрепления умений и навыков, обобщающий, контрольный )
внеурочная работа
экскурсии
Формы организации учебной деятельности
фронтальная
индивидуальная
парная
групповая
Система контроля
Самостоятельные работы
Практическая работа
Контрольная работа Тестирование
Методы организации учебно-познавательной деятельности
По источнику передачи и восприятию учебной информации:
словесные(рассказ, беседа, лекция, диспут, конференция); наглядные (наблюдение, демонстрация); практические (лабораторные, практические работы)
По степени самостоятельности и активности мышления учащихся: репродуктивный (беседа, работа с книгой, устное изложение, наблюдение), продуктивный (проблемное, частично-поисковое, исследовательское, экспериментальное изложение)
По логике передачи и восприятию учебной информации: дедуктивные (от общего к частному),индуктивные (от частного к общему
Слайд 13
Структура содержания тематических модулей
образовательной программы
Слайд 20
Образовательная программа «Химия»
Автор: О.С.Габриелян
Учебно-методический
комплект
Учебник
Рабочая тетрадь
к учебнику
Программа курса химии
8-11 классы
Методические рекомендации для учителя
«Контрольные и проверочные работы»
Слайд 21
Приемы, используемые на разных этапах урока
Слайд 22
Этапы уроков РОП
Урок 1: Физические явления.
Цель: Сформировать понятия

о физических явлениях.
Методические рекомендации
2) Демонстрация опытов учителем с
использованием фронтальной беседы о происходящих явлениях
- плавление парафина ; - растворение перманганата калия;
- возгонка йода; - диффузия душистых веществ.
3) Выполнение лабораторного опыта «Сравнение скорости испарения воды и спирта по исчезновению их капель на фильтровальной бумаге» учащимися в парах
нанесение пипеткой капель воды и спирта на фильтровальную бумагу;
замечают время исчезновения капель воды и спирта с фильтровальной бумаги;
оформление вывода в рабочих тетрадях.
Изучение нового материала:
1)Актуализация знаний на основе повторения материала о природных явлениях по вопросам.
Вопросы:
Какие явления можно наблюдать в природе? Приведите примеры таких явлений.
По каким признакам их можно разделить на группы? Приведите примеры.
В чём особенность природных явлений в каждой группе?
Задачи:
Показать способы разделения смесей и области применения этих способов в быту.
Дать понятия о физических явлениях в химии.
Слайд 23
Закрепление знаний:
Просмотр презентации об очистке воды в городе
Дзержинске (фильм прилагается).
Беседа по презентации с целью проверки усвоения
знаний.
Работа в паре по заданиям в рабочей тетради (стр.88-89) Габриеляна с последующей взаимопроверкой:
- записать определение;
- назвать физические свойства веществ;
- записать об использовании физических явлений в быту и народном хозяйстве;
- определить оборудование для разделения смесей.
4) Самостоятельная работа с текстом и рисунками учебника
Слайд 24
Д/З
1) изучить текст § 25 стр. 129-134
2) выполнить
письменно упражнения № 3, 6
3) подготовить сообщения, презентации об
очистке воды в домашних условиях
4) Работа с занимательным материалом
Слайд 25
Урок 2: Химические реакции.
Цель: Сформировать понятие о химических
реакциях, их отличий от физических
Задачи:
- Познакомить с признаками
и условиями протекания химических реакций.
Показать различия реакций экзо и эндотермических реакций.
Дать определение реакциям горения.
Методические рекомендации
Проверка и закрепление ранее полученных знаний:
Открытый тестовый диктант
- Фильтрование применяют для разделения смесей, если компоненты обладают:
а) различной растворимостью;
б) различной температурой кипения;
в) различными размерами частиц;
г) различной массой
- Выпаривание применяют для выделения веществ из смеси, если компоненты обладают:
а) различной плотностью;
б) различным агрегатным состоянием;
в) различной растворимостью;
г) различной температурой кипения.
- Методами отстаивания и фильтрования можно разделить смесь:
а) растительного масла и воды;
б) поваренной соли и воды;
в) речного песка и воды
Слайд 26
3) Формулировка вывода о значении чистой воды
для
организма человека.
2) Просмотр презентаций учащихся об очистке воды
в
домашних условиях.
Изучение нового материала:
Актуализация знаний в ходе беседы на основе
повторения материала о природных явлениях:
- Как называются изменения, происходящие в природе?
- Какие группы явлений вы помните?
- Что происходит при физических явлениях?
- На каких различиях в свойствах веществ основаны способы разделения?
2) Объяснение учителем основных понятий темы:
химические реакции, их сущность, признаки, условия протекания.
Слайд 27
3) Демонстрация опытов учителем:
- горение
магния;
-
горение фосфора;
- взаимодействие соляной кислоты с мелом;
- получение гидроксида меди (11) и
растворение его в кислотах
4) Повторение правил техники безопасности при работе с лабораторным оборудованием и реактивами
(а) тушить спиртовку только колпачком;
(б) запрещается зажигать одну спиртовку от другой, передавать спиртовку в зажженном виде;
(в) запрещается пробовать вещества на вкус;
(г) запрещается брать вещества руками;
(д) запрещается выливать или высыпать
остатки реактивов в склянки и банки,
из которых они были взяты;
(е) запрещается менять пробки и пипетки
от различных банок или склянок;
(ж) работать только над столом;
(з) смыть водой, затем нейтрализующим веществом
реактив,
если он попал на кожу или одежду;
(и) собирайте остатки веществ в
специально предназначенную посуду
Слайд 28
6) Групповая работа с текстом

и рисунками учебника
(стр. 135-138)
Реакции, протекающие с выделением теплоты,
называют экзотермическими
Реакции, протекающие с поглощением теплоты,
называют эндотермическими
5) Выполнение лабораторных опытов учащимися в парах:
- Окисление меди в пламени спиртовки.
- Помутнение известковой воды от выдыхаемого углекислого газа.
Карточка-инструкция для групп
Проведите лабораторный опыт:
«Растворение сахара в холодной и горячей воде». Сделайте вывод. Возьмите два стакана, налейте в них по 20 мл. воды, опустите в стаканы термометры. Измерьте температуру воды. Затем в один стакан прибавьте немного серной кислоты, а в другой - кристаллы аммиачной селитры NН4NO3
Наблюдения и выводы запишите – заполните пропуски.
В первом случае, при растворении кислоты, наблюдается……………температуры;
во втором случае, при растворении аммиачной селитры, наблюдается………………………………………… температуры.
Следовательно при растворении серной кислоты теплота……………
При растворении аммиачной селитры теплота ……………………………
Слайд 29
Реакции, протекающие с выделением теплоты и света называются
- РЕАКЦИЯМИ ГОРЕНИЯ
Реакции, протекающие с выделением теплоты, называются –
ЭКЗОТЕРМИЧЕСКИМИ (+Q)
4Al+3O2=2Al2O3+Q
Протекающие с выделением теплоты – ЭНДОТЕРМИЧЕСКИМИ (-Q)
N2+O2 2NO-Q
Слайд 30
Заполните схему:
Проверьте себя
Закрепление знаний:
1) Беседа с составлением схемы
о распределении природных явлений с дальнейшей самопроверкой по данному
образцу
Д/З
1) изучить текст § 26
2) выполнить письменно упражнения №1-3
2) Решение проблемной задачи урока
в процессе
заполнения таблицы,
на основе полученных знаний
3) Индивидуальная работа в тетрадях Габриеляна с использованием
текста учебника
Слайд 31
Урок 3: Химические уравнения. Закон сохранения
массы веществ.
Цель: Показать количественную сторону химических реакций, значение закона
сохранения массы веществ, роль Ломоносова в открытии этого закона.
Задачи:
Научить составлять химические уравнения, пользуясь законом сохранения массы веществ.
Дать понятие индекса и коэффициента.
Методические рекомендации
Проверка и закрепление ранее полученных знаний:
Проверьте себя
Укажите химические явления:
а) Распространение запаха духов;
б) Ржавление железа;
в) Испарение воды;
г) Получение сахарной пудры из кристаллов сахара;
д) Гниение растительных остатков;
е) Почернение серебряных изделий.
Примеры химических явлений:
б) ржавление железа;
д) гниение растительных остатков;
е) почернение серебряных изделий.
Запомните: химические явления называют также химическими реакциями
Ответьте на вопрос: как вы определили, что данные явления - химические?
1) Тематический диктант
Слайд 32
Изучение нового материала:
1) Решение проблемной задачи урока в
процессе изучения текстового материала и иллюстраций опытов учебника
2)
Объяснение учителем основного понятия «химическое уравнение» с использованием алгоритма составления уравнения химической реакции:
- запишите формулы исходных веществ, соединив их знаком «+» (левая часть
уравнения;
- поставьте стрелку;
- запишите после стрелки формулы продуктов реакции (это правая часть
уравнения);
- расставьте коэффициенты так, чтобы число атомов одинаковых элементов в
левой и правой частях уравнения были равны);
- замените стрелку знаком равенства.
Слайд 33
ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ
2 Н2О → 2Н2 +
О2
4Н + 2О → 4Н + 2О
m1
m2
m3
m1 = m2
+ m3
Лавуазье (1789)
Ломоносов (1756)
Пишем уравнения ХР
Решаем задачи по уравнениям ХР
4 • 1 + 2 • 16 = 4 • 1 + 2 • 16
36 =36
Слайд 34
3) Объяснение учителем понятий «индекс» и «коэффициент» в
химическом уравнении
Закрепление знаний:
Сульфат натрия + хлорид бария → хлорид
натрия + сульфат бария
Азот + кислород → оксид азота (V)
Алюминий + … → бромид алюминия (III)
… + … → фосфид цинка (II)
Расставьте коэффициенты в схемах реакций. В каком уравнении сумма коэффициентов равна 7
1) Индивидуальная работа с дидактическим материалом по отработке умений составлять химические уравнения
Д/З
1) повторить текст параграфа 27
2) выполнить письменно задания №1-3
Слайд 35
Урок 4: Расчёты по химическим уравнениям
Цель: Научить решать
задачи с использованием понятий «количество
вещества», «массы и объёма вещества».
Задачи:
- Рассмотреть решение задач с вычислением по химическим уравнениям массы и количества вещества по известной массе или количеству вещества .
Рассмотреть решение задач на вычисление массы, количества, объёма вещества продукта реакции, если известна масса исходного вещества, содержащая определённую долю примесей.
Методические рекомендации:
Изучение нового материала:
Проверка и закрепление ранее полученных знаний:
Парная работа со взаимоконтролем по теме «Химические уравнения» в рабочих тетрадях Габриеляна – стр. 91-93
Разбор задач с использованием текста и алгоритма решения задач
- чтение текста задачи;
- выбор данных;
- решение задачи по алгоритму;
- запись ответа задачи.
Закрепление материала:
Групповая работа по составлению задач.
Д/З
Повторить параграф 28
Решить задачи 1-3
Слайд 36
1. Определённый вид атомов называется химическим элементом.
2.
Вещества делятся на простые и сложные
3. Явления, в результате
которых изменяются размеры, формы тел или агрегатные состояния называются физическими.
4. Химические – это явления, в результате которых из одних веществ образуются другие.
5. Реакции, идущие с поглощением тепла – называются эндотермические.
6. Экзотермические – это реакции, идущие с выделением тепла.
?
?
?
?
?
?
Урок 5-8: Реакции разложения, соединения, замещения обмена
Цель: Показать сущность всех типов реакций,
Задачи:
Ознакомить учащихся с классификацией реакций по числу и составу исходных веществ и продуктов реакции.
Сформировать умения различать типы химических реакций.
Закрепить умения писать химические уравнения.
Методические рекомендации
Проверка и закрепление ранее полученных знаний:
1. Работа с деформированным текстом в виде компьютерного слайда с последующей проверкой
Слайд 37
Реакция, уравнение которой
2СО(г) → СО2(г)+ С(тв) + Q
относится к реакциям:
А) соединения, экзотермическим
Б) разложения, экзотермическим
В) соединения, эндотермическим
Г)
разложения, эндотермическим
Реакция, уравнение которой
N2 + O2 →2NO - Q
относится к реакциям:
А) соединения, эндотермическим
Б) соединения, экзотермическим
В) разложения, эндотермическим
Г) разложения, экзотермическим
3. Работа по дидактическим карточкам «Подумай и ответь!»
( дидактические карточки разработаны для 25 вариантов)
2. Самостоятельная работа в рабочих тетрадях Габриеляна
(стр. 101-102 № 3, 5, 6)
расставление коэффициентов в схемах химических реакций;
найти реакции получения кислорода в лаборатории;
записать определения скорости, катализатора, ферментов.
1 вариант
2 вариант
4. Просмотр презентаций учащихся по выбранным темам
5. Сообщения и доклады учащихся с использованием дополнительной литературы
Слайд 38
Объяснение нового материала:
Объяснение учителем основных понятий изучаемых тем:
2)
Демонстрация опытов учителем:
- разложение перманганата калия;
- горение магния;
- разложение пероксида водорода; - горение фосфора;
- получение гидроксида меди (11); - электролиз воды;
- растворение полученного гидроксида в кислотах;
- взаимодействие оксида меди (11) с серной кислотой при нагревании;
реакция разложения;
катализаторы;
ферменты;
скорость химической реакции
реакция соединения;
обратимые и необратимые реакции;
каталитические и некаталитические реакции
реакция замещения;
ряд активности металлов
реакция обмена;
реакции нейтрализации;
условия протекания реакций обмена в растворах до конца
Например:
2KMnO4?K2MnO4+ MnO2 + O2
Опыт взаимодействие алюминия с бромом
Слайд 39
3) Выполнение лабораторных опытов с последующим оформлением результатов
в виде рисунков и таблиц, формулирование выводов
Алгоритм проведения лабораторных
опытов:
соблюдение правил по технике безопасности;
знакомство с инструкцией по выполнению лабораторной работы;
поэтапное планирование выполнения опытов;
проведение опытов;
оформление результатов опытов в тетрадях.
Темы лабораторных опытов:
Окисление меди в пламени спиртовки.
Помутнение известковой воды от выдыхаемого углекислого газа.
Получение углекислого газа взаимодействием соды и кислоты.
Замещение меди в растворе хлорида меди (11) железом.
Zn + 2HCl = ZnCl2 + H2
2Fe +3H2O = Fe2O3 +3H2
Слайд 40
1. Взаимодействие А1 с НС1:
Положите в пробирку кусочек алюминия,

прилейте 3-4 мл. соляной кислоты (НС1). Что наблюдаете? Запишите
уравнение реакции.
2. Взаимодействие СuS04 и Fе:
В химический стакан прилейте раствор сульфата меди (II) (Си804) и опустите кусочек железа (скрепка). Что наблюдаете? Запишите уравнения реакции.
3. Взаимодействие Сu(ОН)2 с Н2SО4:
Получите нерастворимое основание Си(ОН)2: в пробирку прилейте сульфат меди (II) (СuS04) и добавьте 2-3 мл. гидроксида натрия (NаОН) образуется осадок - это получилось нерастворимое основание гидроксид меди (II), к осадку прилейте раствор разбавленной серной кислоты (Н2SО4). Что наблюдаете? Запишите уравнение реакции.
ИНСТРУКЦИЯ ПРОВЕДЕНИЯ ЛАБ./ОПЫТОВ
1. Взаимодействие Мg с НС1:
Положите в пробирку кусочек магния, прилейте 3-4 мл. соляной кислоты (НС1). Что наблюдаете? Запишите уравнение реакции.
2. Взаимодействие СuS04 и Fе:
В химический стакан прилейте раствор сульфата меди (II) (СuS04) и опустите кусочек железа (скрепка). Что наблюдаете? Запишите уравнения реакции.
3. Взаимодействие Сu(ОН)2 с Н2SО4:
Получите нерастворимое основание Сu(ОН)2: в пробирку прилейте сульфат меди (II) (СuS04) и добавьте 2-3 мл. гидроксида натрия (NаОН) образуется осадок - это получилось нерастворимое основание гидроксид меди (II), к осадку прилейте раствор разбавленной серной кислоты (Н2SО4). Что наблюдаете? Запишите уравнение реакции.
Слайд 41
4) Работа с текстом и иллюстрациями учебника с
выяснением признаков реакции разложения, соединения, замещения, обмена
Слайд 42
СХЕМА РАЗЛОЖЕНИЯ ВОДЫ
Атом водорода
Атом кислорода
↯
Вода
Слайд 43
Закрепление знаний:
1) Поочерёдное заполнение граф сводной таблицы «Типы
химических реакций» на основе текста учебника и наблюдений демонстрационных
опытов
Слайд 44
Типы химических реакций
NaOH + HCl → NaCl +
H2O
CaCO3 → CaO + CO2
Fe + Cl2 → FeCl3
H2
+ CuO → Cu + H2O
Реакция соединения
Реакция замещения
+
Реакция обмена
+
+
+
Реакция разложения
+
+
2) Парная работа со схемами химических реакций с последующей проверкой через КТ
Слайд 45
1. Назовите реакции обмена
А) действие на соду кислотой
Б)
горение магния
В) прокаливание карбоната кальция
Г) растворение цинка в кислоте
2.
Метод отстаивания используют для веществ, имеющих:
1. разную растворимость
2. разную температуру кипения
3. разную плотность
4. разное агрегатное состояние
3) Викторина «Кто хочет стать отличником?»
Делительная воронка используется для:
1. выпаривания веществ
2. отделение веществ с разной плотностью
3. для перегонки веществ
4. для кристаллизации
Д/З:
изучение текста параграфов
выполнение упражнений
подготовка сообщений
4) Использование задание познавательного
характера
Слайд 46
Урок 9: Типы химических реакций на примере свойств

воды.
Цель: Рассмотреть типы химических реакций на примере химического вещества
воды
Задачи:
Совершенствовать знания о роли воды в природе и жизни человека.
Проанализировать химические свойства воды, повторив основные типы
химических реакций.
- Обобщить и систематизировать знания о химических реакциях.
Методические рекомендации
Обобщение и закрепление знаний на основе химических свойств воды
1) Работа в группах с дополнительным и справочным материалом
Справочный материал
Значение воды для жизни организмов
Вода - самое распространенное неорганическое соединение в живых организмах нашей планеты. Количество воды в организме зависит от возраста. Эмбрион человека на 97 % состоит из воды, а у новорожденных ее количество составляет уже только 77 % массы. К 50 годам человек немного «усыхает», и вода составляет 60 % от массы его тела. Основная масса воды - 70 % - сосредоточена внутри клеток, 7 % - это кровь и лимфа, а остальная часть омывает клетки снаружи, это вода межтканевая. Зачем столько воды в организме?
• Вода входит в состав всех клеток и тканей тела, в ней протекают все биохимические процессы. Клетка без воды - это уже не живая клетка. Из 26 кг воды в твоем теле на внутриклеточную воду приходится 18 кг.
• Вода служит основой крови и лимфы. На это расходуется 2 кг воды.
Вода является той средой, где совершаются процессы пищеварения. Без воды пища не может ни проходить по желудочно-кишечному тракту, ни усваиваться организмом. На процессы пищеварения и выделения расходуется около 6 кг воды в виде желудочного сока, слюны, мочи, пота и др.
Вода вымывает из клеток отработанные продукты обмена веществ и выносит их из организма, как через почки (с мочой), так и через кожу (с потом).
Вода в твоем организме выступает и как растворитель веществ, и как переносчик веществ по организму. У нее есть еще одна важная роль - через систему потоотделения она регулирует температуру твоего тела
Слайд 47
Справочный материал для групповой работы
Вода – растворитель
Из свойств

воды особенно важна ее способность растворять вещества.
Вода -
универсальный растворитель. В ней могут растворяться вещества различной химической природы, образованные ковалентными полярными и ионными связями. В воде могут растворяться твердые, жидкие и газообразные вещества. Но не все они одинаково хорошо растворяются в воде. Вещества бывают хорошо растворимое, малорастворимые и практически нерастворимые. Широко применяются водные растворы твердых веществ. Любая природная вода - раствор. Величина, характеризующая способность веществ растворяться в воде, - это растворимость, которая определяется массой вещества, способной раствориться в 100 г воды при определенной температуре.
Растворимость зависит от температуры, но не всегда одинаково. На нее влияет агрегатное состояние вещества.
Карточка-инструкция для группы
Из предложенного перечня веществ выберите те, с помощью которых можно продемонстрировать постепенность растворения веществ в воде:
СаО, SiO2, СаСО3, КМn04, К2Сr2О7, NH4N03.
Слайд 48
Зашифрованное слово: тип реакции, в ходе которой
одного сложного вещества образуется несколько простых № сложных веществ.
Вопросы
Реакция
взаимодействия веществ с кислородом, которая сопровождается выделением света и тепла.
Вещество, в состав которого входит ОН-группа.
...+02->N02.
Обязательный элемент в составе оксидов.
Вещество, которое состоит из атомов металла и кислотного остатка.
... + S->FeS
Тип реакции: 2А1 + 3 СиО -> 3 Си + А1203.
Реакция, при которой из двух или нескольких веществ образуется одно сложное.
H2S04 - класс веществ.
10. Тип реакции: H2S04 + 2NaOH -> Na2S04 + 2Н20.
Ответы: 1. Горение. 2. Основание. 3. Азот. 4. Кислород. 5. Соль. 6. Железо. 7. Замещение. 8. Соединение. 9. Кислота. 10. Обмен.
2) Обобщение и закрепление знаний в ходе заполнения граф кроссворда
Слайд 49
Задание:
заполните пустые клетки
формулами веществ, расставьте необходимые коэффициенты и
определите типы этих реакций
3) Индивидуальная работа по карточкам
4) Выбор
объекта исследования. Оформление выводов.
Слайд 50
Урок 10: Контрольная работа по теме
«Изменения, происходящие
с веществами».
Цель: Проконтролировать усвоение знаний учащимися по теме
«Изменения, происходящие с веществами»
Задачи:
Проверить знания учащихся типов химических реакций.
- Выявить умения составлять химические уравнения.
- Выявить умения проводить расчёты по химическим уравнениям и решать задачи.
Слайд 51
К/р «Изменения, происходящие с

веществами»
Вариант 1
1. Выпишите предложение, в котором говорится о физическом явлении:
а) при прокаливании медная пластинка чернеет;
б) при пропускании углекислого газа известковая вода мутнеет;
в) при нагревании вода превращается в пар;
г) под действием света фотопленка, на которую нанесен бромид серебра, чернеет.
Расставьте коэффициенты в схемах химических реакций и укажите тип каждой из них:
а) Си + 8 — Си28; б) МпО2 + С — СО + Мn.
Лампочка прибора для определения электропроводности веществ загорится при погружении электродов в:
а) жидкий азот;
б) раствор хлорида калия;
в) раствор сахара;
г) кристаллический сульфат натрия.
Вычислите массу и количество вещества оксида углерода(1V), образовавшегося при полном сгорании 36г угля.
Названия только неоднородных смесей записаны в ряду:
а) масло, речная вода, раствор поваренной соли;
б) сахар, уголь, дождевая вода;
в) кровь, молоко, раствор глины;
г) керосин, раствор уксусной кислоты, смесь растительного масла с водой.
6. К раствору гидроксида бария по каплям приливают раствор серной кислоты.
Электропроводность системы при этом будет:
а) вначале возрастать, затем уменьшаться;
б) вначале уменьшаться, затем возрастать;
в) постепенно возрастать;
г) постепенно уменьшаться.

Контрольная работа
К/р «Изменения, происходящие с веществами
Вариант 2
1. Выпишите предложение, в котором говорится о химическом явлении:
а) при пропускании электрического тока вода превращается
в два газообразных вещества — кислород и водород;
б) при нагревании растворимость сахара в воде повышается;
в) при температуре О °С вода превращается в лед;
г) при температуре 100 °С вода кипит.
2. Расставьте коэффициенты в схемах химических реакций и укажите тип каждой из них:
а) МпO2 + А1 -* А1203 + Мn; б)Р + 02 -» Р205.
3. Лампочка прибора для определения электропроводности веществ не загорится при погружении
электродов в:
а) дистиллированную воду;
б) расплав хлорида кальция;
в) соляную кислоту;
г) раствор гидроксида натрия.
4. Рассчитайте массу и количество вещества кальция, вступившего в реакцию с 32 г кислорода.
5. Названия только однородных смесей записаны в ряду:
а) молоко, природный газ, песок;
б) чистый воздух, раствор соли, водопроводная вода;
в) нефть, мел, мука;
г) смесь мела с водой, кровь, раствор марганцовки.
6. К раствору нитрата серебра по каплям приливают соляную кислоту. Электропроводность системы при этом будет:
а) постепенно возрастать;
б) постепенно уменьшаться;
в) вначале возрастать, затем уменьшаться;
г) вначале уменьшаться, затем возрастать.
Слайд 53
Тест по теме: «Изменения, происходящие с веществами»
А1)Физическое явление
1.Ржавление железа
2. плавление металла
3.горение природного газа
4.скисание молока
А2)Химическое явление
1.плавление льда
2.испарение воды
3.разложение серной кислоты
4.растворение сахара в воде
А3)Для выделения поваренной соли из её раствора в воде можно использовать
1.фильтрование
2.отстаивание смеси в воде
3.дистиляцию
4.выпаривание и кристаллизацию
А4)Экзотермическая реакция-это реакция, протекающая
1.с выделением газа
2.с образованием осадка
3.с выделением теплоты
4.с поглощением теплоты
Слайд 54
А5) Составьте уравнение реакции по схеме: CH4 +O2=CO2
+ H2O ответ дайте в виде коэффициентов в уравнении
реакции.
1.5
2.6
3.7
4.8
А6) Определите количество вещества гидроксида натрия, необходимое для полной нейтрализации 2 моль серной кислоты
1. 1моль
2. 2моль
3. 3моль
4. 4моль
А7)Укажите уравнение реакции разложения
1.Mg(OH)2 = MgO + H2O
2.Mg + 2HCl = MgCl2 + H2
3.Mg + O2 = 2MgO
4.2Mg + CO2 = 2MgO + C
А8) Напишите уравнение реакции соединения по схеме: Na2O + H2O =….
Определите сумму коэффициентов этом уравнении
1.4
2.5
3.6
4.7
Слайд 55
А9) Металл, который не вытесняет водород из кислот
1.Cu
2.Fe
3.Al
4.Zn
А10) В ходе реакции
обмена между растворами Na2CO3 и HCl образуется
1.только вода
2.вода и газ
3.осадок
4.только газ
А11) Укажите оксид, который
взаимодействует с водой
1. оксид меди
2.оксид цинка
3. оксид кремния
4.оксид бария
Слайд 56
Структура содержания тематических модулей образовательной программы
8
класс
Слайд 57
Структура содержания тематических модулей образовательной программы
Слайд 58
Кластер по разделу
«Химические реакции»
Химические реакции
8 класс
Первоначальные понятия
9
класс
Расширение знаний
о химических реакциях
10 класс
Особенности химических реакций
в органической
химии
11 класс
Повторение, систематизация знаний
Содержание
Понятие
Что говорить?
Методика
Как вести урок?
Форма организации
Вид занятия
Цели и результаты
Зачем?
Слайд 59
Структура содержания тематических модулей образовательной программы
8
класс
Слайд 60
Структура содержания тематических модулей образовательной программы
9
класс
Слайд 61
Структура содержания тематических модулей образовательной программы
10
класс
Слайд 62
Структура содержания тематических модулей образовательной программы
11
класс
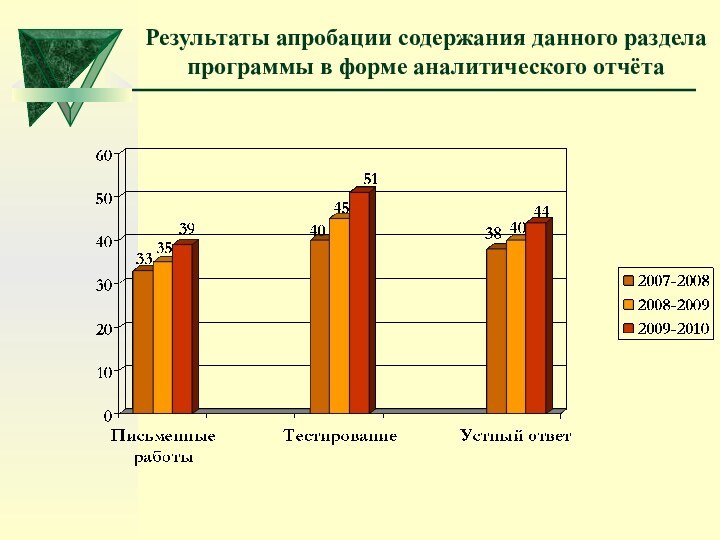
Слайд 63
Результаты апробации содержания данного раздела
программы в форме
аналитического отчёта
2007-2008 учебный год
2008-2009 учебный год
2009-2010 учебный год
Слайд 64
Результаты апробации содержания данного раздела
программы в форме
аналитического отчёта
Слайд 65
Вывод
Система работы по данному разделу – целенаправленный процесс,
в результате которого учащиеся убеждаются в том, что «химическая
реакция» является одной из важных форм движения материи, через которую происходят познания целостности картины мира.
Слайд 66
Источники информации для учителя:
1) Аверкиева Г.И. Загадки реакций

обмена. –М: Химия в школе, 1982 г №2 стр.57
2)
Брейгер Л.Н. Химия 11-й класс поурочные планы. –Волгоград: Учитель, 1997 г
3) Габриелян О. С. Химия 8-9/ методическое пособие. –М: Дрофа, 2001 г.
4) Габриелян О. С., Рунов Н. Н. Химический эксперимент в школе. –М: Дрофа, 2000 г.
5) Городова Н.М. Сборник тестовых заданий по химии для 8-9 классов. –М: Наука, 1998 г
6) Денисова В.Г. Мастер- класс учителя химии 8-11 класс. –М: Глобус, 2010 г
7) Кирюшин Д.М. Методы обучения в средней школе. –М: Просвещение, 1991 г.
8) Крицман В.А. Д.И. Менделеев о химических реакциях. –М: Химия в школе, 1984 г №3 С.16
9) Маршанова Г.Л. Сборник задач по органической химии. –М: Издат-школа, 2005 г.
10) Маршанова Г.Л. 500 задач по химии 8-11 классы. –М: Издат-школа, 2000 г
11) Пасечник Б.Н. Развитие самостоятельности и творческих способностей учащихся при изучении химии. –М: Химия в школе 1986 №1 С.55
12) Плетнер Ю.В., Полосин В.С. Практикум по методике обучения химии.
–М: Просвещение, 1998 г.
13) Радецкий А.М., Курьянова Т.Н. Дидактический материал по общей химии для 11 класса./ Пособие для учителя. –М: Просвещение, 2001 г
14) Савич Г.З. Формирование понятий о химической реакции. –М: Просвещение, 1991 г.
15) Чертков И.Н. Обучение химии в 10-м классе ( в двух частях). –М: Просвещение, 1992 г
16) Эмануэль Н.М. Химическая кинетика. –М: Знание, 1991 г.