- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Кислоты. Физические свойства. Получение. 8 класс
Содержание
- 2. Если формулы начало Представляется с металла, ОН
- 3. Распределите формулы по классам в
- 4. «Кислоты, номенклатура, классификация, физические и химические свойства».
- 5. Кислоты в природе Апельсины, лимоны и
- 6. Яблочной кислотой богаты плоды рябины, барбариса, малины, яблони
- 7. салициловая, яблочная, лимонная, винная, эллаговая, фолиевая, кофейная, хлорогенная, муравьиная, щавелевая кислоты содержатся в малине.
- 8. Муравьиная кислота содержится в едких выделениях муравьев, в крапиве, хвое ели.
- 9. СОСТАВ КИСЛОТ:КИСЛОТЫ – СЛОЖНЫЕ ВЕЩЕСТВА, СОСТОЯЩИЕ ИЗ
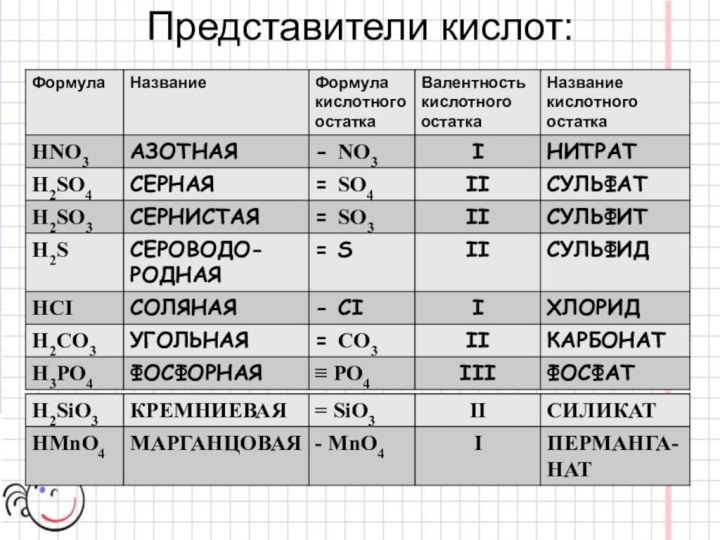
- 10. Представители кислот:
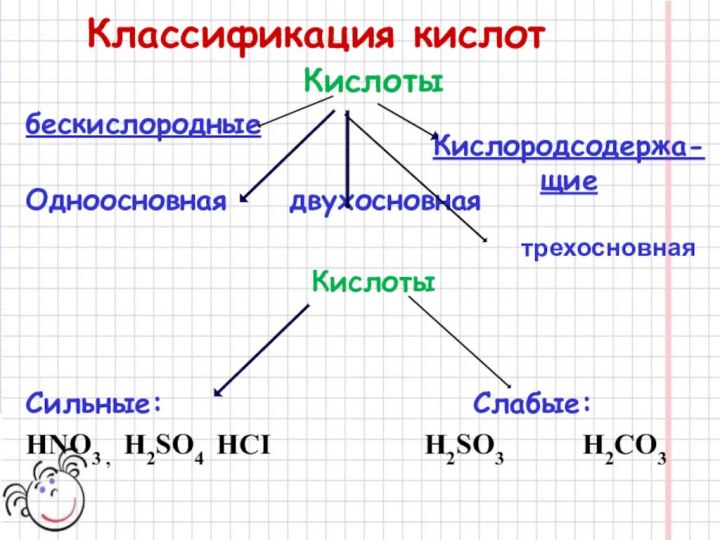
- 11. Классификация кислотКислотыбескислородныеОдноосновная двухосновнаяКислотыСильные:
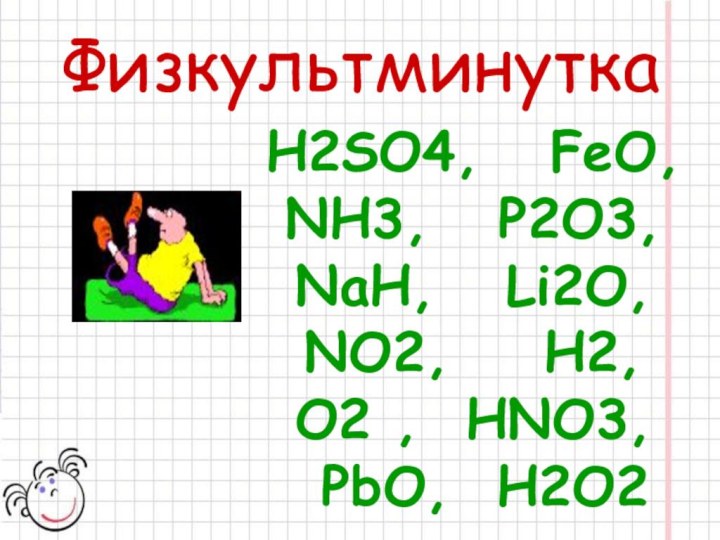
- 12. Физкультминутка Н2SO4, FeО, NН3, P2О3,
- 13. Способы получения кислотВзаимодействие кислотных оксидов с водой:SO3
- 14. Скачать презентацию
- 15. Похожие презентации
Если формулы начало Представляется с металла, ОН – красуется затем, Вещества знакомы всем. Не надо придумывать им название Ведь эти вещества…Что такое основания? Как отличить основание от других классов?










Слайд 2 Если формулы начало Представляется с металла, ОН – красуется затем, Вещества
знакомы всем.
Не надо придумывать им название
Ведь эти вещества…
основания? Как отличить основание от других классов?Слайд 3 Распределите формулы по классам в таблицу : HCl, HNO3,
H2SO4, Ca(OH)2, K2O, Na2O, Al2O3, Zn(OH)2, Al(OH)3.
Слайд 5 Кислоты в природе Апельсины, лимоны и грейпфруты, киви, яблоки,
абрикосы, дыня, ежевика и многие другие фрукты и овощи
содержат аскорбиновую кислоту — это химическое название витамина С.
Слайд 7
салициловая, яблочная, лимонная, винная, эллаговая, фолиевая, кофейная,
хлорогенная, муравьиная, щавелевая кислоты содержатся в малине.
Слайд 9
СОСТАВ КИСЛОТ:
КИСЛОТЫ – СЛОЖНЫЕ ВЕЩЕСТВА, СОСТОЯЩИЕ ИЗ АТОМОВ
ВОДОРОДА, КОТОРЫЙ МОЖЕТ ЗАМЕЩАТЬСЯ НА АТОМЫ МЕТАЛЛА.
Mg + 2
HCI = MgCI2 + H2Al + H2SO4 = AI2(SO4)3 + H2
Слайд 11
Классификация кислот
Кислоты
бескислородные
Одноосновная двухосновная
Кислоты
Сильные:
Слабые:
HNO3 , H2SO4 HCI H2SO3 H2CO3
Кислородсодержа- щие
трехосновная
Слайд 13
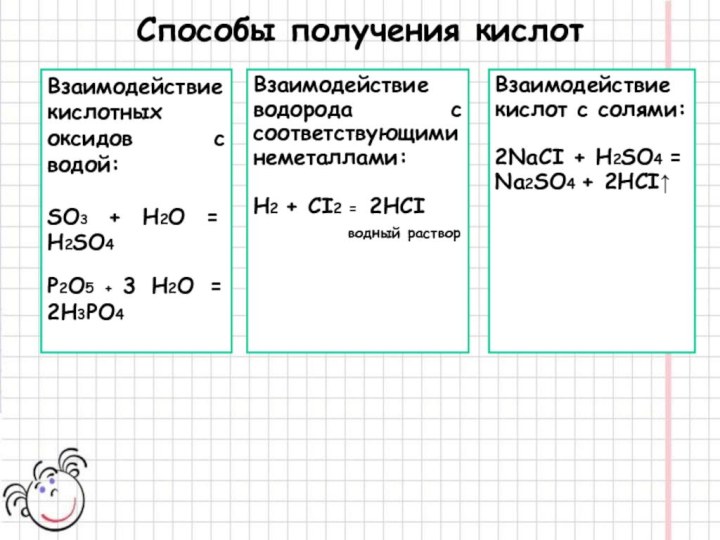
Способы получения кислот
Взаимодействие кислотных оксидов с водой:
SO3 +
H2O = H2SO4
P2O5 + 3 H2O = 2H3PO4
Взаимодействие
водорода с соответствующими неметаллами:Н2 + CI2 = 2HCI
водный раствор
Взаимодействие кислот с солями:
2NaCI + H2SO4 = Na2SO4 + 2HCI↑