- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Содержание
Содержание
- 2. СодержаниеНормативная базаПонятие о ВФМЦели, задачи и область применения ВФМОсуществление ВФМЗаключение
- 3. Верификация — это подтверждение соответствия конечного продукта
- 4. Нормативная база Требования GMP GMP EU, пункт
- 5. ОпределенияВерификацияОценка возможности использования методики по назначению в
- 6. Фармакопейные методики (ФМ) валидированы!
- 7. Цели и задачи ВФМЦельПодтверждение пригодности ФМ
- 8. Область применения ВФМДля каких методов?ТитриметрияХроматографияСпектрофотометрияДля каких показателей
- 9. ФМ, не требующие верификации Основные ФМ:
- 10. Верификация
- 11. ВФМ
- 12. Масштабы осуществления ВФМФакторы влиянияУровень подготовленности, знания и
- 13. Верификационные
- 14. Осуществление ВФМВФМ не требует полной ревалидации ФМВФМ
- 15. Верификация
- 16. Валидационные и верификационные требования к методикам ЖХ
- 17. Специфичность
- 18. Сначала
- 19. Дополнительные характеристики при ВФМОпределение примесейПредел обнаруженияПредел количественного определенияТочность (прецизионность)
- 20. Неудовлетворительные результаты ВФМ ФМ не может считаться
- 21. ЗаключениеВФМ должна осуществляться
- 22. Скачать презентацию
- 23. Похожие презентации




















Слайд 3 Верификация — это подтверждение соответствия конечного продукта предопределённым
эталонным требованиям.
Валидация - подтверждение на основе предоставления объективных свидетельств
того, что требования, предназначенные для конкретного использования или применения, выполнены.
Верификация - подтверждение на основе предоставления объективных свидетельств того, что установленные требования выполнены.
Слайд 4
Нормативная база
Требования GMP
GMP EU, пункт 6.15
(действующая версия с 01.10.2014):
«Методики испытаний должны быть валидированы. Лаборатория, использующая методику испытания и не проводившая ее валидацию, должна верифицировать пригодность этой методики»
Фармакопейные требования
U.S. Pharmacopeia 39 National Formulary 34 Volume I, Pages 1162-1163 General chapter «Verification of Compendial Procedures» 1226
Государственная фармакопея Республики Казахстан 2-ое издание (ГФ РК 2.0), том II Общая монография «Верификация фармакопейных методик» 1226
Слайд 5
Определения
Верификация
Оценка возможности использования методики по назначению в
реальных условиях
ее применения к лекарственному средству (активной субстанции и/или лекарственному препарату)Валидация
Экспериментальное доказательство пригодности методики для решения предполагаемых задач
Слайд 6
Фармакопейные методики (ФМ) валидированы!
Пользователи ФМ не должны проводить их валидацию, если они впервые применяются в их лабораториях, однако они должны установить и документировать пригодность этих методик в реальных условиях испытания данного лекарственного средства
Слайд 7
Цели и задачи ВФМ
Цель
Подтверждение пригодности ФМ
для испытания лекарственного средства
Задачи
Подтверждение пригодности условий
определенияОпределение и оценка рабочих аналитических характеристик верификации
Установление факторов, влияющих на рабочие аналитические характеристики верификации (вспомогательные вещества, профиль примесей и др.)
Слайд 8
Область применения ВФМ
Для каких методов?
Титриметрия
Хроматография
Спектрофотометрия
Для каких показателей качества?
Идентификация
Родственные
примеси
Количественное определение
При каких условиях?
Если ФМ впервые выполняется в лаборатории
Если ФМ впервые применяется к фармакопейным объектам испытания
Слайд 9
ФМ, не требующие верификации
Основные ФМ:
- методики мокрой химии
(например,
определение кислотного числа, воды),
- простые инструментальные
определения
(например, измерение рН)
- определение потери в массе
при высушивании;
- определение остатка после
прокаливания
- определение тяжелых металлов и др.
Повседневно выполняемые ФМ (рутинные)
Слайд 10 Верификация
микробиологических методик
ГФ РК & Европейская фармакопея
2.6.1. Стерильность
2.6.12.
Микробиологические испытания нестерильных продуктов: общее количество жизнеспособных аэробных микроорганизмов2.6.13. Микробиологические испытания нестерильных продуктов: испытание на определенные микроорганизмы
2.6.31. Испытание микробиологической чистоты лекарственных растительных препаратов для орального применения и экстрактов, используемых для их получения
2.7.2. Количественное определение антибиотиков микробиологическим методом
5.1.9. Руководство по использованию испытания на стерильность
Фармакопея США
51 Испытания антимикробной активности
61 Микробиологическая оценка нестерильных продуктов: перечень микробиологических испытаний
62 Микробиологическая оценка нестерильных продуктов: испытания на определенные микроорганизмы
71 Испытания стерильности
1227 Валидация микробиологичес-кой открываемости в фармакопейных объектах
Слайд 11 ВФМ
должна проводиться пользователем так, чтобы ее результаты обеспечивали уверенность в правильности выполнения методик
Слайд 12
Масштабы осуществления ВФМ
Факторы влияния
Уровень подготовленности, знания и опыт
пользователя
Тип методики
(испытание, метод) Оборудование или
измерительные приборы
Испытуемый(ые) материал(ы)
Конкретные этапы методики
Слайд 13 Верификационные
требования
должны быть основаны на оценке сложности методики и материала, к которому применяется методика
Слайд 14
Осуществление ВФМ
ВФМ не требует полной ревалидации ФМ
ВФМ предусматривает
оценку отдельных рабочих аналитических характеристик, приемлемых для
данной ФМВФМ учитывает путь синтеза активной субстанции, технологию производства лекарственного препарата
ВФМ включает оценку таких факторов, как влияние вспомогательных веществ на величину открываемости, пригодность хроматографических условий и колонки, приемлемость сигнала детектора и др.
Повторная ВФМ не предусматривается нормативными требованиями
ВФМ требует документирования (протокол, отчет)
Слайд 16 Валидационные и верификационные требования к методикам ЖХ
(количественное определение активного вещества в лекарственном препарате)
Слайд 17 Специфичность
как ключевой параметр в ВФМ
Что влияет?
Различный профиль примесей в активных субстанциях разных производителей, не соответствующий ФМ
Значительное отличие вспомогательных веществ в лекарственных препаратах разных производителей
Возможное образование вспомогательными веществами примесей, не определяемых ФМ
Возможное экстрагирование веществ из материала контейнера
Как подтверждается?
Соответствием требованиям для коэффициента разделения в хроматографических ФМ при проверке пригодности системы
Проведением испытаний с плацебо
Слайд 18 Сначала
проводят
проверку пригодности хроматографической системы и проверяют соответствие полученных результатов требованиям пригодности, затем в случае соответствия - испытания по ФМ (не наоборот!)Слайд 19 Дополнительные характеристики
при ВФМ
Определение примесей
Предел обнаружения
Предел количественного определения
Точность (прецизионность)
Слайд 20
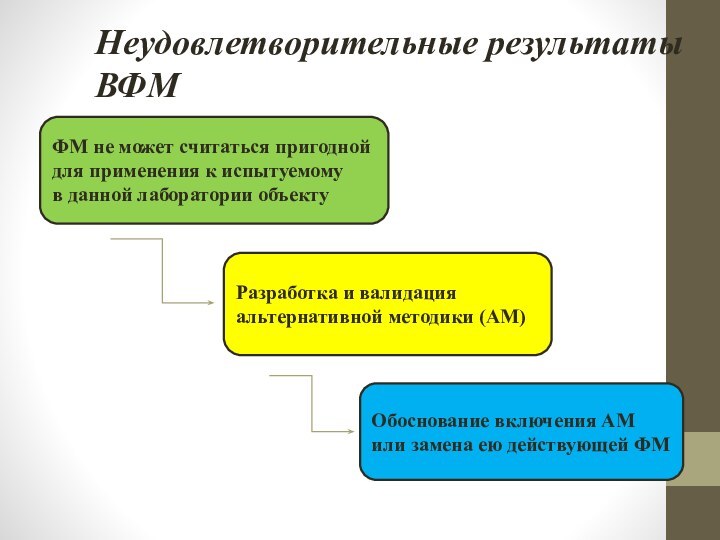
Неудовлетворительные результаты ВФМ
ФМ не может считаться пригодной
для применения к испытуемому
в данной лаборатории объектуРазработка и валидация альтернативной методики (АМ)
Обоснование включения АМ или замена ею действующей ФМ
Слайд 21
Заключение
ВФМ должна осуществляться
в соответствии с
требованиями GMP и фармакопейСведения об осуществлении ВФМ должны быть отражены в регистрационном досье заявленного лекарственного средства
Сведения об осуществлении ВФМ должны быть представлены при оценке условий производства в процессе выполнения экспертных работ при государственной регистрации лекарственного средства