- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему ГУС
Содержание
- 2. Атипичный вариант ГУС составляет 5-10% от всех
- 3. В основе аГУС лежит тромботическая микроангиопатия (ТМА),
- 4. Заболеваемость и распространенность аГУС изучены недостаточно. По
- 5. Патогенез Еще в 1970-1980 гг. было замечено, что
- 7. Все эти три пути сходятся в точке
- 9. CFH (фактор H) является наиболее важным протеином
- 10. ГУС ассоциируется с мутациями CFH у 20-25%
- 11. Предполагается, что мутации в генах CFH, MCP,
- 12. Клиническая манифестация аГУС. Очень раннее начало (даже
- 13. Приблизительно у 25% больных аГУС носит семейный
- 14. Начало заболевания, как правило, внезапное Симптомами у
- 15. У большинства пациентов при первом лабораторном исследовании
- 16. В случае запоздалой диагностики могут наблюдаться опасные
- 17. При гистологическом анализе пораженных сосудов выявляется ТМА,
- 18. В целом прогноз аГУС неблагоприятный. Смертность в
- 19. Рецидивы аГУС отмечаются при всех вариантах, чаще
- 20. Критериями постановки диагноза аГУС являются: 1) отсутствие
- 21. Необходимо исследование системы комплемента С3, С4, концентрации
- 22. У детей возраст начала указывает на необходимость
- 23. Лечение До настоящего времени терапией первой линии является
- 24. Эффективность ЗПП продемонстрирована в основном у пациентов
- 25. Противопоказанием к плазматерапии является ГУС, вызванный Streptococcus
- 26. Большинство эпизодов аГУС связаны с инфекций, что
- 27. Одной из важных клинических проблем является определение
- 28. Перспективным направлением лечения аГУС является воздействие на
- 29. Скачать презентацию
- 30. Похожие презентации
Атипичный вариант ГУС составляет 5-10% от всех случаев ГУС у детей, являетсягенетическим прогрессирующим заболеванием с крайне высоким риском внезапной смерти и необратимых инвалидизирующих повреждений жизненно важных органов, включая почки, печень, сердце и мозг



























Слайд 2 Атипичный вариант ГУС составляет 5-10% от всех случаев
ГУС у детей, является
риском внезапной смерти и необратимых инвалидизирующих повреждений жизненно важных органов, включая почки, печень, сердце и мозгСлайд 3 В основе аГУС лежит тромботическая микроангиопатия (ТМА), связанная
с неконтролируемой активацией системы комплемента . Основным органом-мишенью микроангиопатического тромбообразования
служат почки, однако в ряде случаев возможна генерализация ТМА, приводящая к развитию полиорганной ишемии с картиной полиорганной недостаточностиСлайд 4 Заболеваемость и распространенность аГУС изучены недостаточно. По данным
различных источников, в странах с достаточным уровнем диагностики распространенность
заболевания составляет от 1 до 3 пациентов аГУС на 1 миллион населения. Болезнь чаще манифестирует у детей до 18 лет, но приблизительно в 40% случаев диагностируется во взрослом возрасте.
Слайд 5
Патогенез
Еще в 1970-1980 гг. было замечено, что ряд
пациентов с аГУС имели низкий уровень C3 плазмы крови.
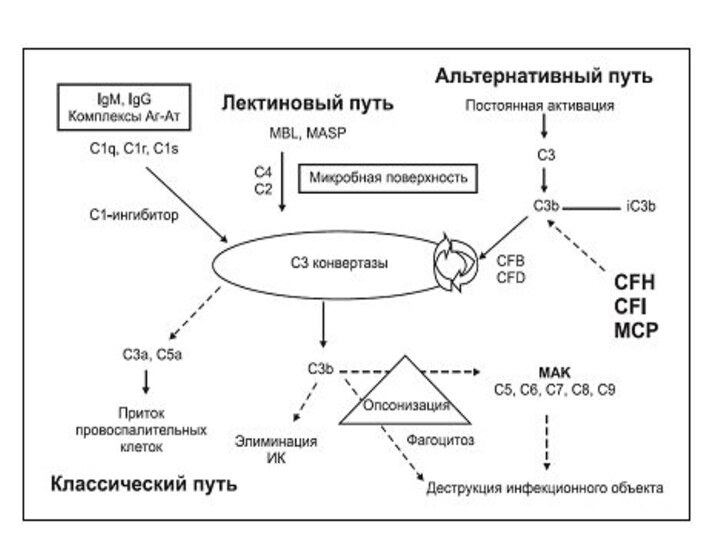
Впечатляющий прогресс был достигнут в течение последних 10 лет, продемонстрировавший, что 4 регуляторных белка альтернативного пути активации комплемента фактор H (CFH), мембранный кофакторный белок (MCP или CD46), фактор I (CFI) и тромбомодулин (THBD), а также 2 протеина С3-конвертазы, С3 и фактор B (CFB) играют роль в патогенезе аГУССлайд 7 Все эти три пути сходятся в точке расщепления
C3 фракции комплемента. В то время как активация классического
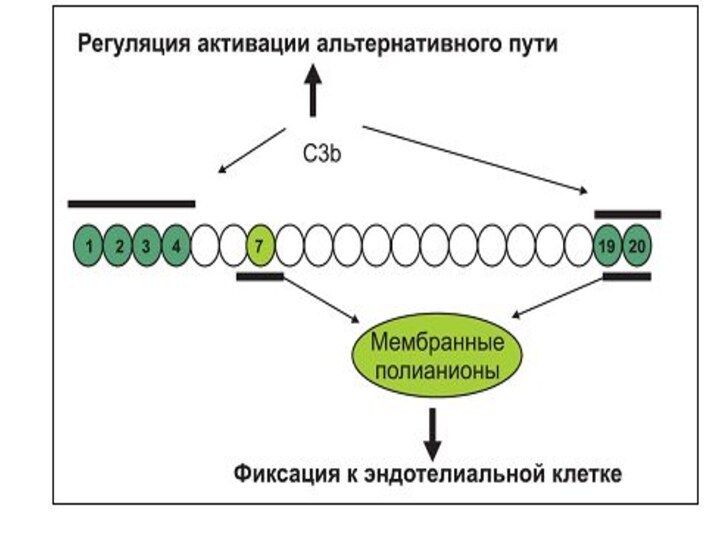
и лектинового путей начинается после связывания с иммунными комплексами или микроорганизмами соответственно, альтернативный путь активируется постоянно с образованием C3b, который беспорядочно связывается с патогенами и клетками хозяина. На чужеродной поверхности, например бактериальной, C3b связывает СFB, который затем расщепляется фактором D с формированием C3-конвертазы C3bBb. C3bBb в геометрической прогрессии расщепляет C3 (петля усиления) и формирует С5-конвертазу (C3bBb (C3b)n). Компонент C5b, получаемый в результате расщепления С5, принимает участие в образовании мембраноатакующего комплекса (МАК) C5b9, который вызывает опсонизацию, фагоцитоз и лизис бактерий). Указанная реакция в норме строго контролируется на поверхности клеток хозяина, которые защищены от локальной амплификации депозитов C3b рядом контролирующих систему комплемента протеинов: CFH (гликопротеин плазмы, кофактор для CFI), CFI (сериновая протеаза плазмы, которая расщепляет и инактивирует C3b с формированием iC3b в присутствии кофакторов, включающих МСР (нециркулирующий гликопротеин, встроенный в мембраны всех клеток, кроме эритроцитов) и, возможно, THBD ( тромбомодулин). THBD – эндотелиальный гликопротеин, обладающий антикоагулянтными, противовоспалительными и цитопротективными свойствами, также являющийся регуляторным белком системы комплемента. В присутствии CFH отмечается конкуренция CFH и CFB за связывание C3b, что ограничивает образование С3-конвертазы. Когда CFH связан с C3b, закрепленным на поверхности клетки, CFB более не имеет возможности принимать участие в формировании С3-конвертазыСлайд 9 CFH (фактор H) является наиболее важным протеином в
системе регуляции альтернативного пути активации комплемента . Он состоит
из 20 коротких консенсусных повторов (SCRs) и содержит не менее двух C3b-связывающих участков.Первый участок, связывающийся с C3b, регулирующий жидкую фазу амплификации альтернативного пути, располагается в N-терминальном конце SCR1–4. Второй C3b-связывающий участок расположен в SCR19–20 С терминального домена. CFH также содержит два полианионных связывающих участка в SCR7 и SCR19–20. Эндотелиальные клетки богаты полианионными молекулами, в частности, гликозаминогликанами. Защита клеток хозяина зависит от инактивации поверхностно-связанного C3b, вторичной по отношению к связыванию CFH с поверхностно-связанным C3b. Все последние научные исследования наглядно продемонстрируют роль SCR19–20 в защите эндотелиальных клеток .Четыре протеина – CFH, CFI, MCP и THBD – локально взаимодействуют для расщепления C3b до неактивной молекулы (iC3b). Мутации этих белков приводят к утрате защиты эндотелиальных клеток
Слайд 10 ГУС ассоциируется с мутациями CFH у 20-25% пациентов,
MCP — у ≈15 % и CFI — у
≈10 %. Мутации фактора В (CFB) встречаются крайне редко (1%), в то время как мутации C3 фракции комплемента встречаются у 10% пациентов. Приблизительно 10% детей имеют сочетанные мутации. В дополнение, 10% детей имеют приобретенный функциональный дефицит CFH в связи с наличием анти-CFH антител. Только 30% aГУС сегодня не находит должного объясненияСлайд 11 Предполагается, что мутации в генах CFH, MCP, CFI
и THBD, обнаруженные у пациентов с аГУС, приводят к
образованию дефекта защиты эндотелиальных клеток от активации системы комплемента. В целом, все идентифицированные генетические дефекты приводят к усилению образования C3-конвертазы, а следовательно, и С5-конвертазы, и расщеплению C5. Вследствие этого усиливается высвобождение С5а и МАК на поверхности клеток эндотелия, вызывающее дополнительное их повреждение с обнажением субэндотелиального матрикса и образованием тромбов. Это приводит к потреблению тромбоцитов и повреждению эритроцитов. Кроме того, продемонстрирована значительная роль CFH в регуляции структуры и функции тромбоцитов. При наличии С-концевых мутаций способность CFH связываться с тромбоцитами снижается, что приводит к_активации комплемента на поверхности тромбоцитов. Это, в свою очередь, вызывает активацию тромбоцитов, их агрегацию, высвобождение тканевого фактора, экспрессирующего микрочастицы, и содействует образованию тромбов в микроциркуляторном русле
Слайд 12
Клиническая манифестация аГУС.
Очень раннее начало (даже в периоде
новорожденности) характерно для аГУС, связанного с мутациями CFH и
CFI (средний возраст 6 мес и 2 мес — соответственно). Наоборот, при мутации MCP заболевание всегда начинается старше 1 года. Этиологически неопределенные варианты аГУС могут начаться в любом возрасте. Анти-CFH антитела чаще отмечаются ближе к подростковому периоду.Провоцирующими факторами являются некоторые инфекции (верхних дыхательных путей, лихорадка, гастроэнтериты), они запускают первый эпизод аГУС и рецидивы независимо от генетического варианта у 2/3 пациентов. Диарея провоцирует аГУС у 1/3 пациентов, что иногда затрудняет дифференциацию с Д+ ГУС.
Слайд 13 Приблизительно у 25% больных аГУС носит семейный характер.
Неотягощенный семейный анамнез не исключает возможности генетической передачи заболевания.
Лишь половина носителей мутации в семье в течение жизни имеют манифестацию заболевания.Слайд 14 Начало заболевания, как правило, внезапное Симптомами у детей
раннего возраста являются бледность, общее недомогание, плохой аппетит, рвота,
сонливость и иногда отеки Экстраренальные проявления в виде поражения ЦНС проявляются судорогами, сопором, комой и выявляются у менее чем 20% пациентов. В патогенезе энцефалопатии играют важную роль одновременно несколько факторов: отёк мозга, гипоксия, кровоизлияния в вещество мозга. Массивное внутрисосудистое потребление тромбоцитов может спровоцировать развитие коагулопатии потребления: гипер- или гипокоагуляция, гипопротромбинемия, гипофибриногенемия, повышение уровня продуктов деградации фибрина, Д-димера, замедленный фибринолиз, нарушение агрегации тромбоцитовСлайд 15 У большинства пациентов при первом лабораторном исследовании выявляется
полная диагностическая триада ГУС: гемоглобин 40-90 г/л тромбоцитопения (
с отсутствием или с небольшим риском геморрагических осложнений и почечная дисфункция (мочевина >8 ммоль/л, креатинин >110 мкмоль/л), с наличием или отсутствием анурии, олигоурии, протеинурии при сохраненном диурезе. Лейкоцитоз, умеренно выраженный ретикулоцитоз. Для подтверждения неиммунного характера анемии выполняется реакция Кумбса- отрицательная при ГУС. Наличие шизоцитов, а также неопределяемый гаптоглобин, в сочетании с высоким уровнем ЛДГ, подтверждают микроангиопатический внутрисосудистый генез гемолизаСлайд 16 В случае запоздалой диагностики могут наблюдаться опасные для
жизни осложнения: гиперкалиемия (≥6 ммоль/л), ацидоз (сывороточный бикарбонат
ммоль/л) и перегрузка объёмом с развитием артериальной гипертензии и гипонатриемии (<125 ммоль/л). Артериальная гипертензия встречается часто, имеет тяжелое течение и связана как с перегрузкой объемом в случаях олигурии/анурии, так и с вторичной, по отношению к почечной ТМА, гиперренинемией. Возможно развитие сердечной недостаточности или неврологических осложнений (судороги) вследствие гипертензии. Большинство взрослых и половина всех пациентов детского возраста нуждаются в проведении гемодиализа при поступленииСлайд 17 При гистологическом анализе пораженных сосудов выявляется ТМА, характеризующаяся
утолщением стенок артериол и капилляров, с выраженным повреждением эндотелия
(отек и отслойка), субэндотелиальным накоплением протеинов и клеточного детрита, фибриновыми и тромбоцитарными тромбами, обтурирующими просвет сосуда. ТМА преимущественно поражает микрососуды почек, хотя в патологический процесс могут вовлекаться микрососуды головного мозга, сердца, легких и желудочно-кишечного тракта. В клинической картине могут присутствовать симптомы полиорганной недостаточности: поражение лёгких, поджелудочной железы, желудочно-кишечного тракта, миокарда.Слайд 18 В целом прогноз аГУС неблагоприятный. Смертность в острой
стадии составляет 5-10%. Приблизительно у 50% пациентов развивается терминальная
ХПН, чаще в течение 1 года от начала манифестацииСлайд 19 Рецидивы аГУС отмечаются при всех вариантах, чаще у
пациентов с мутацией MCP. Провоцирующие инфекции при этом сопровождаются
острым гемолизом, тромбоцитопенией и острой почечной недостаточностью в результате гемоглобинурии. В большинстве этих случаев функция почек полностью восстанавливается. Промежуток времени между рецидивами может колебаться от нескольких недель до многих лет.Наиболее благоприятный прогноз отмечается при наличии MCP мутации, наиболее неблагоприятный — при CFH и сочетанных мутациях. По данным французских авторов, смерть или терминальная ХПН в течение менее чем 1 года от начала заболевания отмечены у 60% с мутацией CFH, у 37% с мутацией CFI, у 33% с мутацией С3, у 60% с комбинированными мутациями, у 32% в группе с неизвестной этиологией и 0% с мутацией MCP. У больных с анти-CFH антителами в случае раннего лечения ЗПП заболевание имеет благоприятное течение