- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Химические свойства оксидов
Содержание
- 2. Классификация оксидов по химическим свойствамОКСИДЫНесолеобразующиеБезразличныеСО, NO, N2O, SiOСолеобразующие ОсновныеВаО, СаО КислотныеSO3, N2O5АмфотерныеZnO, Al 2O3химические свойства
- 3. Несолеобразующие оксиды – это оксиды, которые не
- 4. Солеобразующие оксиды – это оксиды, которые взаимодействуют
- 5. Основные оксиды – это оксиды, которым в
- 6. Кислотные оксиды – это оксиды, которым в
- 7. Амфотерные оксиды – это оксиды, которым соответствуют
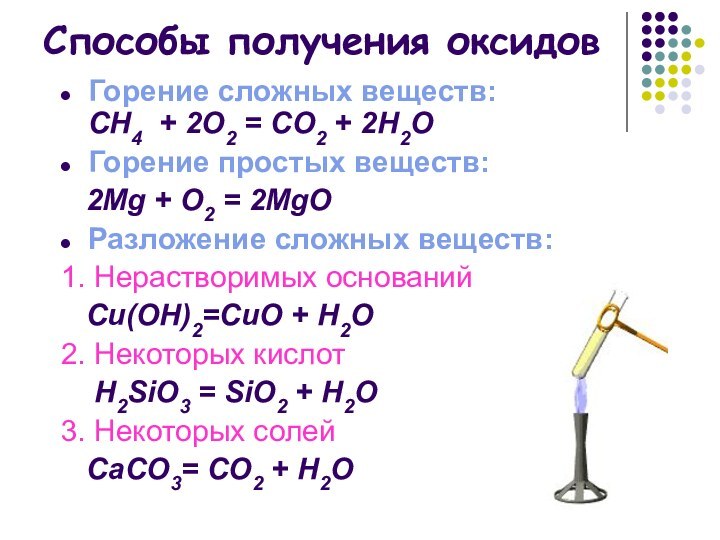
- 8. Химические свойства основных оксидовосновной оксид + вода
- 9. Химические свойства кислотных оксидовкислотный оксид + вода
- 10. Химические свойства амфотерных оксидов
- 11. Скачать презентацию
- 12. Похожие презентации
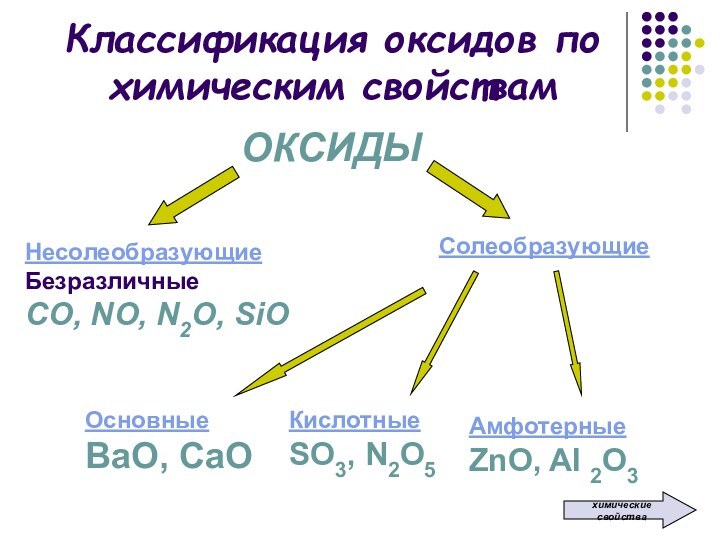
Классификация оксидов по химическим свойствамОКСИДЫНесолеобразующиеБезразличныеСО, NO, N2O, SiOСолеобразующие ОсновныеВаО, СаО КислотныеSO3, N2O5АмфотерныеZnO, Al 2O3химические свойства









Слайд 2
Классификация оксидов по химическим свойствам
ОКСИДЫ
Несолеобразующие
Безразличные
СО, NO, N2O, SiO
Солеобразующие
Слайд 3 Несолеобразующие оксиды – это оксиды, которые не взаимодействуют
ни с кислотами, ни с основаниями и не образуют
солейСО, NO, N2O, SiO
Слайд 4 Солеобразующие оксиды – это оксиды, которые взаимодействуют с
кислотами или со щелочами с образованием солей и воды
Слайд 5 Основные оксиды – это оксиды, которым в качестве
гидроксидов соответствуют основания
Образованы металлами в степени окисления +1, +2
К2О
→ КОНMgO → Mg(OH)2
Слайд 6 Кислотные оксиды – это оксиды, которым в качестве
гидроксидов соответствуют кислоты
Образованы неметаллами и металлами в степени окисления
+5 и вышеSО3 → Н2SО4
Слайд 7 Амфотерные оксиды – это оксиды, которым соответствуют гидроксиды,
проявляющие свойства как оснований, так и кислот
Образованы металлами в
степени окисления +3, +4, а также оксиды ВеО, ZnO, SnO, PbOZnO → Zn(OH)2 или Н2ZnО2
Слайд 8
Химические свойства основных оксидов
основной оксид + вода =
основание
СаO + H2O = Са(OН)2
основный оксид + кислота = соль + вода
CuO + 2 HCL = CuCL2 + H2O
CuO + 2H+ +2CL- = Cu2 + + 2CL- +Н2О
CuO + 2H+ = Cu2 + +Н2О
основный оксид + кислотный оксид = соль
MgO + SO3 = MgSO4
Слайд 9
Химические свойства кислотных оксидов
кислотный оксид + вода =
кислота
Р2O5 + 3H2O = 2H3РO4
кислотный оксид + основание = соль + вода
CO2 + Mg(OН)2= MgCO3 + H2O
CO2 + Mg+ +2OН- = MgCO3 + Н2О
кислотный оксид + основный оксид = соль
SO3 + MgO = MgSO4
Слайд 10
Химические свойства амфотерных оксидов
Основные
С кислотами: ZnO + 2НСl → ZnСl2 + Н2О
С кислотными оксидами: ZnO+ SiO2 = ZnSiO3
Кислотные
С основаниями: ZnO + 2NaОН = Na2ZnO2 +Н2О
С основными оксидами: ZnO + MgО = MgZnO2