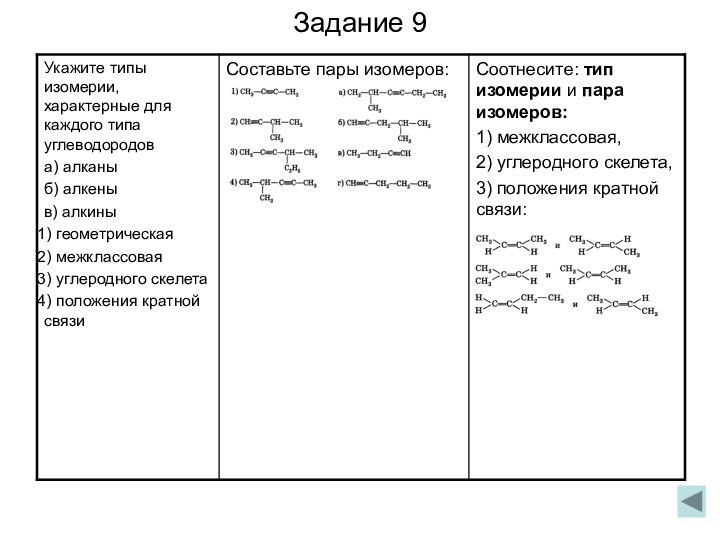
к классу
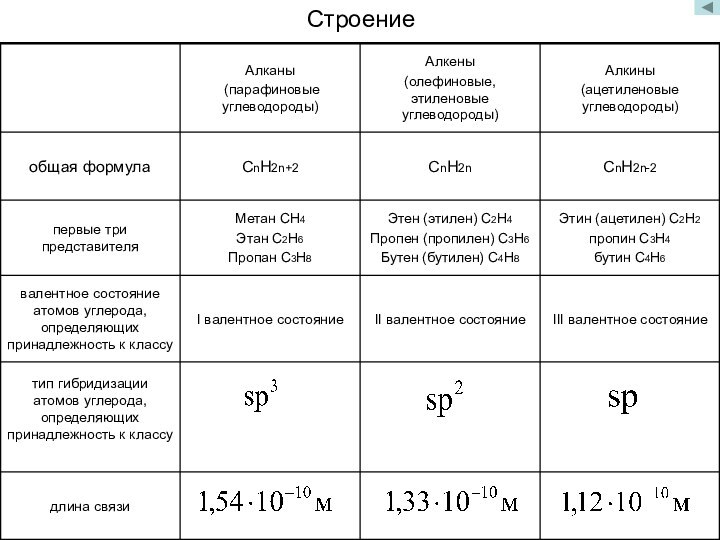
III валентное состояние
II валентное состояние
I валентное состояние
валентное состояние
атомов углерода, определяющих принадлежность к классуЭтин (ацетилен) С2Н2
пропин С3Н4
бутин С4Н6
Этен (этилен) С2Н4
Пропен (пропилен) С3Н6
Бутен (бутилен) С4Н8
Метан CH4
Этан C2H6
Пропан C3H8
первые три представителя
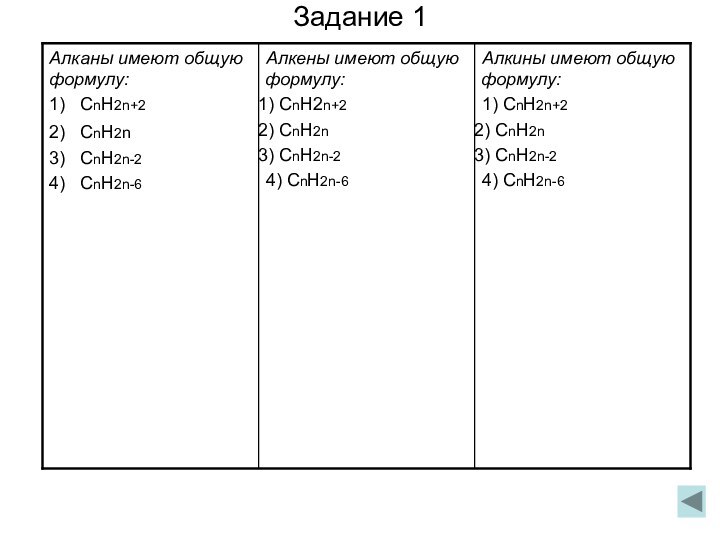
CnH2n-2
CnH2n
СnH2n+2
общая формула
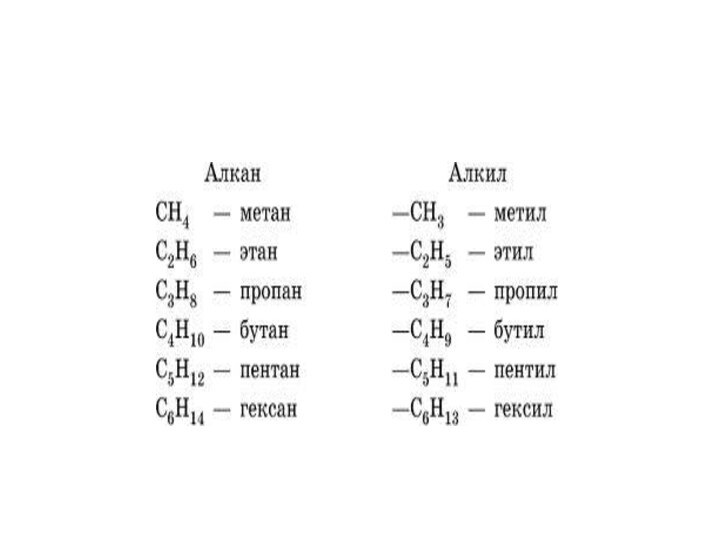
Алкины
(ацетиленовые углеводороды)
Алкены
(олефиновые, этиленовые углеводороды)
Алканы
(парафиновые углеводороды)