металл
Если металл образует соединения с разными степенями окисления, то
степень окисления указывается после названия металла в скобках римской цифрой, например, гидроксид меди(II).Гидроксид натрия NaOH
Гидроксид калия KOH
Гидроксид кальция Ca(OH)2
Гидроксид магния Mg(OH)2
Гидроксид алюминия Al(OH)3
Гидроксид железа (III) Fe(OH)3
Гидроксид меди (II) Cu(OH)2
Гидроксид никеля (II) Ni(OH)2
Число гидроксогрупп в молекуле гидроксида зависит от степени окисления металла.
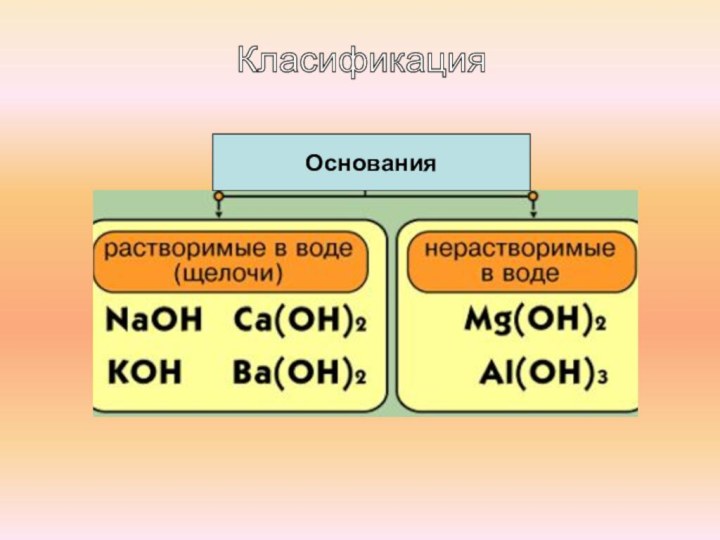
Основания – это сложные вещества, состоящие из атомов металлов и одной или нескольких гидроксогрупп (OH).