- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Тема № 4 Реакции терпеноидов
Содержание
- 2. 4.1 Реакции изомеризации Будучи продуктами биосинтеза, большинство
- 3. 4.1.1 Реакции изомеризации углеводородовВозможна изомеризация углеводородов при
- 4. α-пинен
- 5. 4.1.2 Изомеризационные превращения спиртовИзомеризационные превращения спиртов более
- 6. 4.1.2.1 Ациклические спиртыОсобенно склонны к
- 7. Механизм реакции изомеризации линалоола в кислой среде1) Протонирование гидроксильной группы способствует отщеплению воды от молекулы линалоола:
- 8. Процесс протекает легко, поскольку приводит к образованию
- 9. 2) Обратное присоединение воды к катионам 1
- 10. гераниол
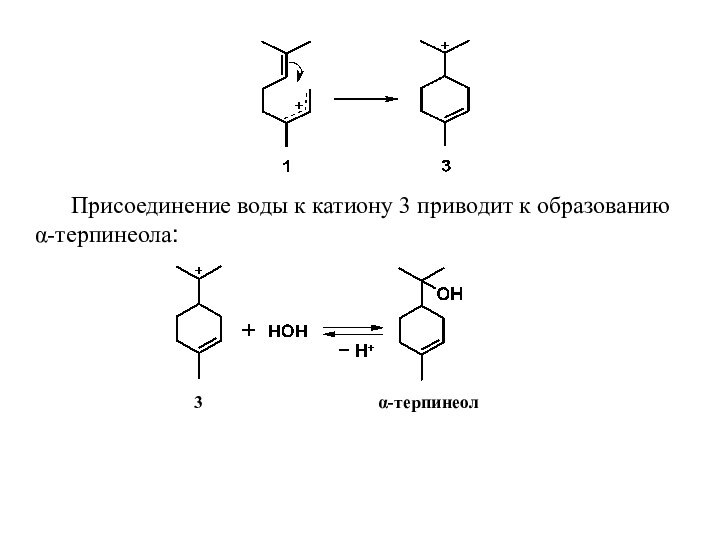
- 11. 3) Конформация катиона 1 предполагает возможность
- 12. Присоединение воды к катиону 3 приводит к
- 13. 4) Наряду с изомеризационными превращениями, в условиях
- 14. Аллильная перегруппировка линалоола имеет практическое значение, поскольку
- 15. 4.1.2.2
- 16. ментол
- 17. 4.2 РЕАКЦИИ ДВОЙНЫХ СВЯЗЕЙ Большинство терпеноидов являются
- 18. 4.2.1.1 Присоединение водородаПрисоединение связано с разрывом π-связи
- 19. Бициклические терпеноиды могут присое-динять водород. Гидрирование
- 20. 4.2.2 Присоединение воды (реакция гидратации) Вода способна
- 21. 1 Гидратация мирцена. Наличие в молекуле мирцена
- 22. Гидратация легче протекает по сопряженным двойным связям.
- 23. нерол
- 25. Катионы 1 и 2, прежде чем присоединить
- 26. 2 Приосоединение воды
- 27. Терпин образуется
- 28. Частичной дегидратацией терпина можно получить одноатомные спирты
- 29. 4.3 Реакции
- 30. 4.3.1 Реакции дегидратации
- 31. Среди ациклических
- 32. Катионы 1 и 2 после отщепления протона
- 33. 4.3.2 Реакции с разрывом связи
- 34. 1 Механизм
- 35. 3 Переходный комплекс распадается, отщепляя воду и
- 36. Особенности реакции
- 37. 2 Реакция
- 38. 4.3.3 Окисление спиртов
- 40. нерол гераниол
- 41. 4.4 Реакции сложных эфиров терпеновых спиртов
- 42. Основными реакциями
- 43. Реакция начинается
- 44. 2 Реакция элиминирования
- 45. 4.5 РЕАКЦИИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙАльдегиды и кетоны терпенового
- 46. Реакции нуклеофильного присоединения (AN) являются наиболее характерными в ряду карбонильных соединений. Карбонильная группа легко протонируется кислотами:
- 48. 4.5.1 Реакции со спиртами
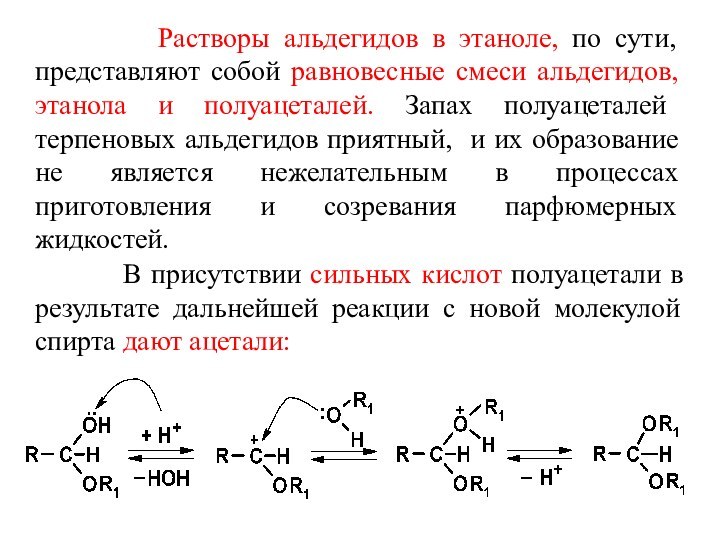
- 49. Растворы альдегидов
- 50. Реакция ацетализации обратима.
- 51. 4.5.2 Реакции с производными аммиака
- 52. Скачать презентацию
- 53. Похожие презентации


























Слайд 3
4.1.1 Реакции изомеризации углеводородов
Возможна изомеризация углеводородов при повышенной
температуре (350-400 °С.)
Эффективным способом управления хими-ческим превращением является
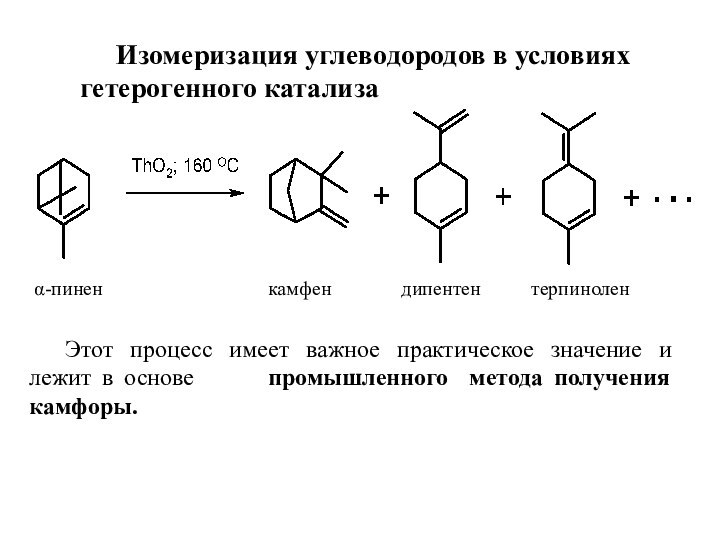
использование катализатора.Показано, что в присутствии некоторых алюмосиликатов, оксида алюминия и тория, т.е. в условиях гетерогенного катализа, α-пинен при температуре 150-160 °С изомеризуется в камфен с выходом около 70 %:
Слайд 4 α-пинен
камфен дипентен терпинолен
Этот процесс имеет важное практическое значение и лежит в основе промышленного метода получения камфоры.
Изомеризация углеводородов в условиях гетерогенного катализа
Слайд 5
4.1.2 Изомеризационные превращения спиртов
Изомеризационные превращения спиртов более разнообразны
по сравнению с превращениями углеводородов благодаря наличию гидроксильной группы
-ОНИзомеризация осуществляется в присутствии катализаторов. Наиболее активными катализаторами являются кислоты, воздействующие как на функциональную группу спиртов, так и на реакционные центры углеродного скелета – двойные связи и напряженные циклы.
Слайд 6
4.1.2.1 Ациклические спирты
Особенно склонны к изомеризации
спирты аллильной структуры – линалоол, гераниол, нерол, среди которых
наиболее активен третичный спирт линалоол.Под действием кислот при повышенной температуре линалоол образует сложную смесь, в которой наряду с линалоолом находятся гераниол, терпинеол, примеси нерола и других спиртов, а также углеводороды
Слайд 7
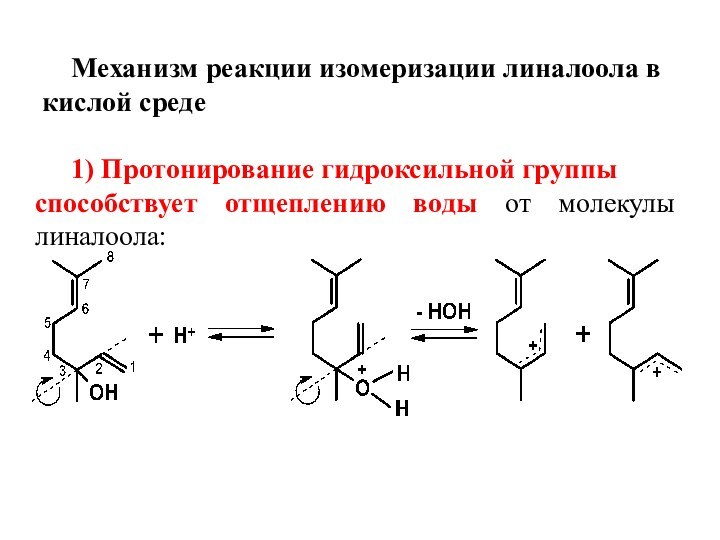
Механизм реакции изомеризации линалоола в
кислой среде
1) Протонирование
гидроксильной группы
способствует отщеплению воды от молекулы линалоола:
Слайд 8 Процесс протекает легко, поскольку приводит к образованию двух
устойчивых сопряженных (мезомерных) стереои-зомерных катионов 1 и 2.
Образование
двух стереоизомерных катионов объясняется свободным вращением концевой винильной группы в молекуле линалоола относительно простой связи, и невозможностью такого вращения в катионах 1 и 2 в связи с возникновением за счет сопряжения дополнительной частичной π-связи между атомами 2 и 3.Слайд 9 2) Обратное присоединение воды к катионам 1 и
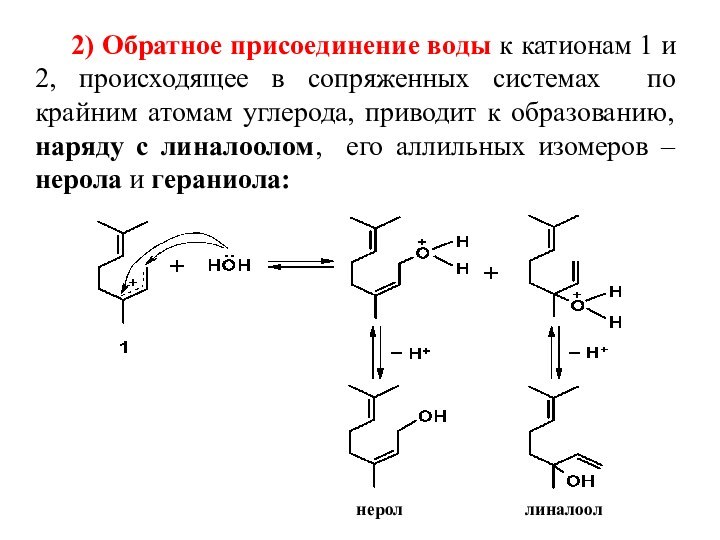
2, происходящее в сопряженных системах по крайним атомам углерода,
приводит к образованию, наряду с линалоолом, его аллильных изомеров – нерола и гераниола: нерол линалоол
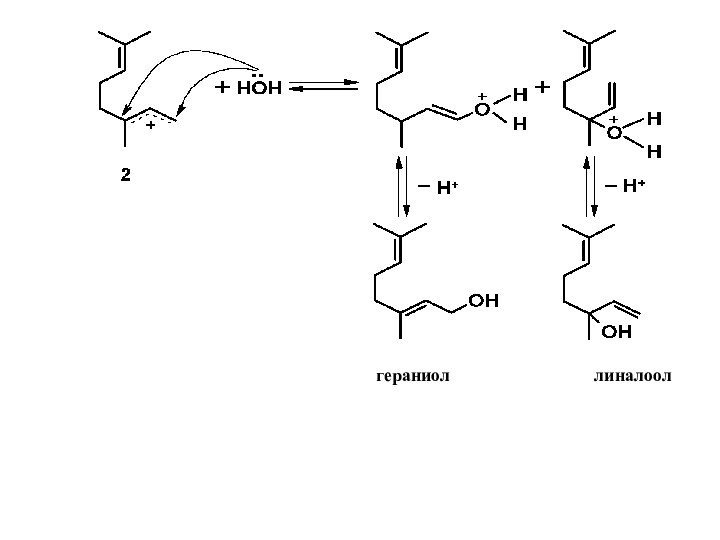
Слайд 11 3) Конформация катиона 1 предполагает возможность сближения
двойной связи с крайним атомом мезомерного катиона на расстояние,
соответствующее длине химической связи. На таком расстоянии напряженность электрического поля положительного заряда весьма велика и вызывает разрушение легко поляризуемой π-связи и возникновение новой σ-связи, замыкающей шестизвенный цикл с образованием углеродного скелета п-ментана (п-ментановая циклизация):Слайд 13 4) Наряду с изомеризационными превращениями, в условиях процесса
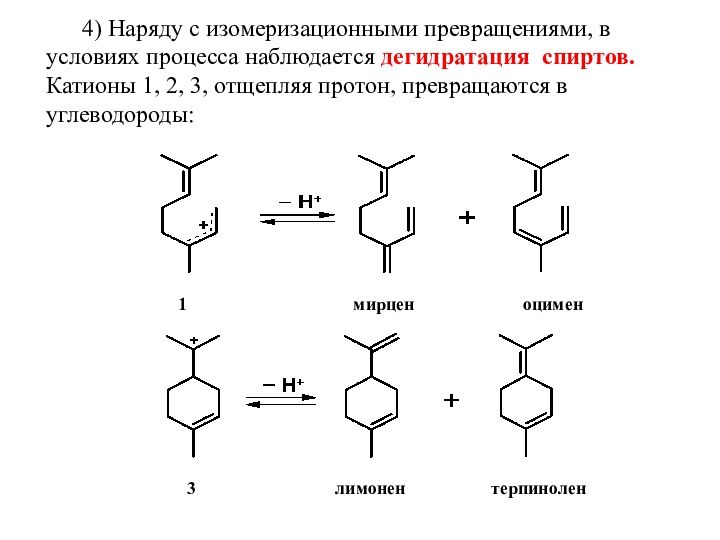
наблюдается дегидратация спиртов. Катионы 1, 2, 3, отщепляя протон,
превращаются в углеводороды: 1 мирцен оцимен
3 лимонен терпинолен
Слайд 14 Аллильная перегруппировка линалоола имеет практическое значение, поскольку позволяет
получить из относительно доступного линалоола гераниол и нерол, обладающие
запахом розы. Процесс предложено проводить, используя в качестве катализаторов соли переходных металлов (V, Mo, W, Cr и др.), которые вызывают меньше побочных превращений по сравнению с кислотами.Слайд 15 4.1.2.2 Моноциклические
спирты
Практически важным примером изомеризации, приводящей к изменению пространственной структуры
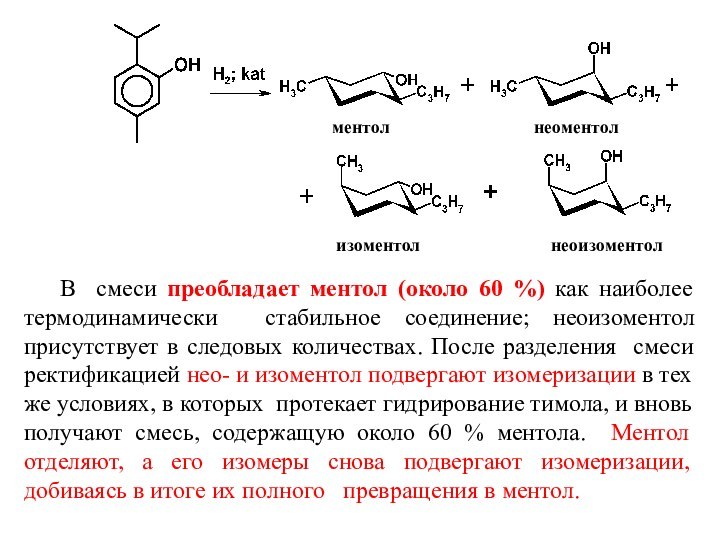
молекулы, является превращение нео- и изо-ментола в ментол. При получении ментола гидри-рованием тимола образуется смесь диастереомеров ментол, неоментол, изоментол, неоизоментол: Слайд 16 ментол
неоментол
изоментол неоизоментол
В смеси преобладает ментол (около 60 %) как наиболее термодинамически стабильное соединение; неоизоментол присутствует в следовых количествах. После разделения смеси ректификацией нео- и изоментол подвергают изомеризации в тех же условиях, в которых протекает гидрирование тимола, и вновь получают смесь, содержащую около 60 % ментола. Ментол отделяют, а его изомеры снова подвергают изомеризации, добиваясь в итоге их полного превращения в ментол.
Слайд 17
4.2 РЕАКЦИИ ДВОЙНЫХ СВЯЗЕЙ
Большинство терпеноидов являются ненасыщен-ными
соединениями и претерпевают превращения, обусловленные наличием двойных углерод-углеродных связей.
4.2.1 Реакции присоединения
Реакции присоединения – наиболее типичные реакции алкенов. По двойной связи могут присоединяться водород, галогены, галогеноводороды, вода, кислоты и другие реагенты. Многие из подобных реакций имеют большое значение в химии терпеноидов и широко используются в практических целях.
Слайд 18
4.2.1.1 Присоединение водорода
Присоединение связано с разрывом π-связи и
образованием вместо нее двух более прочных σ-связей.
В отсутствие
катализатора гидрирование протекает крайне медленно даже при сильном нагревании.Катализатор эффективно снижает величину энергии активации ∆Еа. Наиболее активными катализаторами являются металлы платиновой группы. Для практических целей чаще используют более доступные никелевые катализаторы.
Гидрирование – обратимый процесс. Катализаторы одновременно ускоряют и обратную реакцию – дегидрирования. Для сдвига равновесия в сторону продуктов гидрирования процесс проводят при высоком давлении.
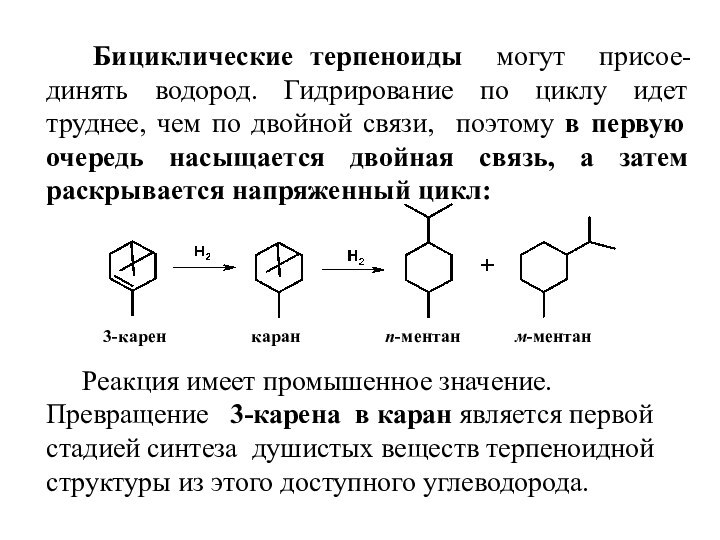
Слайд 19 Бициклические терпеноиды могут присое-динять водород. Гидрирование по
циклу идет труднее, чем по двойной связи, поэтому в
первую очередь насыщается двойная связь, а затем раскрывается напряженный цикл: 3-карен каран п-ментан м-ментан
Реакция имеет промышенное значение. Превращение 3-карена в каран является первой стадией синтеза душистых веществ терпеноидной структуры из этого доступного углеводорода.
Слайд 20
4.2.2 Присоединение воды (реакция гидратации)
Вода способна
присоединяться по наиболее реакционноспособным двойным связям и напряженным циклам
терпеноидов с образованием спиртов. Достаточная скорость реакции может быть достигнута лишь в присутствии катализаторов – кислот. Гидратация является типичной реакцией типа АЕ (электрофильного присоединения) и протекает по правилу Марковникова*.* При взаимодействии галогеноводородов и родственных им соединений с несимметричными алкенами атом водорода присоединяется по месту двойной связи к более гидрогенизированному атому углерода, т.е. к атому углерода, содержащему большее число атомов водорода.
Слайд 21 1 Гидратация мирцена. Наличие в молекуле мирцена нескольких
двойных связей приводит к образованию смеси различных спиртов.
Продукт
гидратации мирцена состоит из многих спиртов различного строения. Их образование может быть объяснено при рассмотрении механизма реакции.
Слайд 22
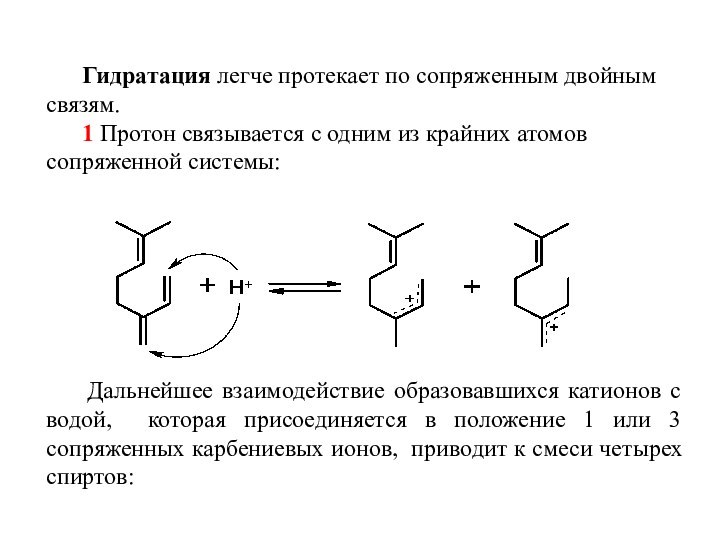
Гидратация легче протекает по сопряженным двойным связям.
1
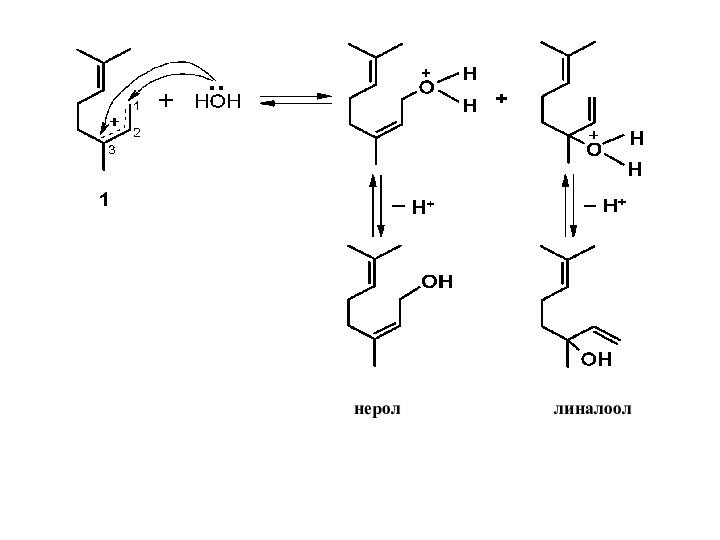
Протон связывается с одним из крайних атомов сопряженной системы:
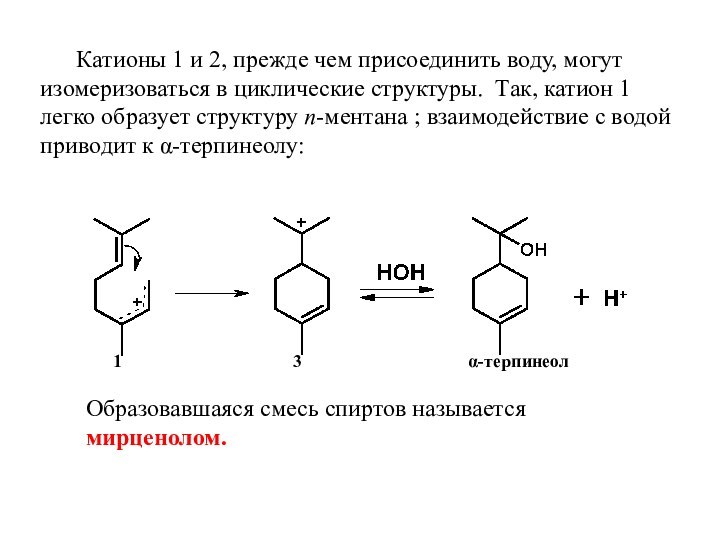
Дальнейшее взаимодействие образовавшихся катионов с водой, которая присоединяется в положение 1 или 3 сопряженных карбениевых ионов, приводит к смеси четырех спиртов:Слайд 25 Катионы 1 и 2, прежде чем присоединить воду,
могут изомеризоваться в циклические структуры. Так, катион 1 легко
образует структуру п-ментана ; взаимодействие с водой приводит к α-терпинеолу: 1 3 α-терпинеол
Образовавшаяся смесь спиртов называется мирценолом.
Слайд 26
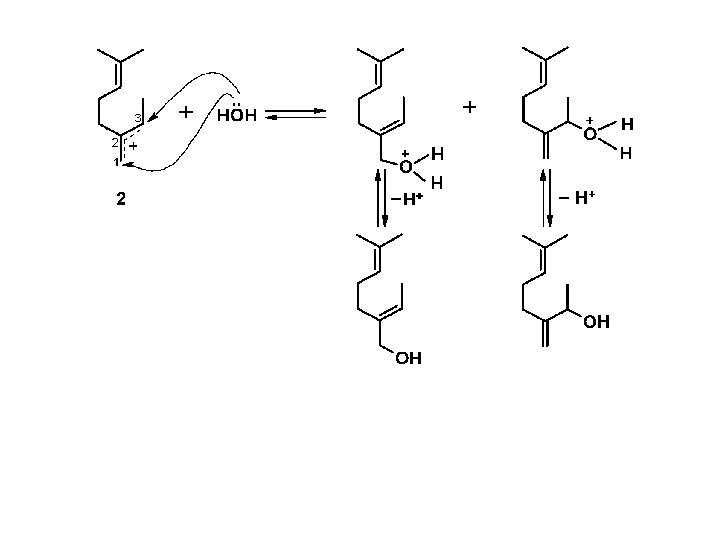
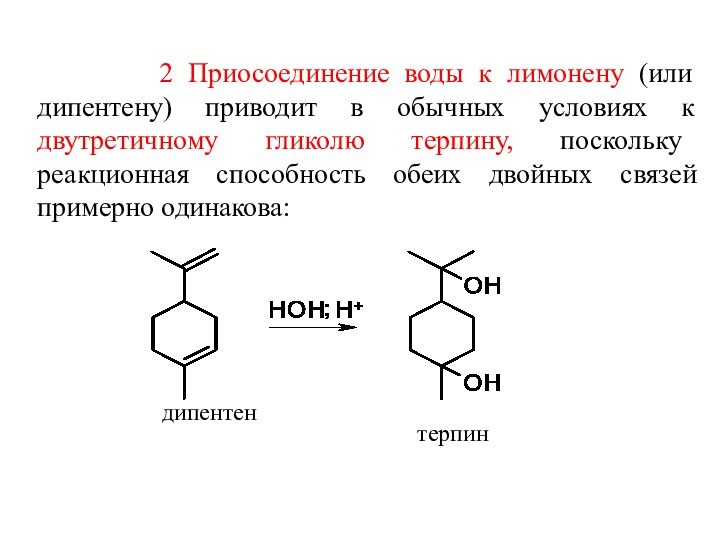
2 Приосоединение воды к
лимонену (или дипентену) приводит в обычных условиях к
двутретичному гликолю терпину, поскольку реакционная способность обеих двойных связей примерно одинакова: дипентен
терпин
Слайд 27
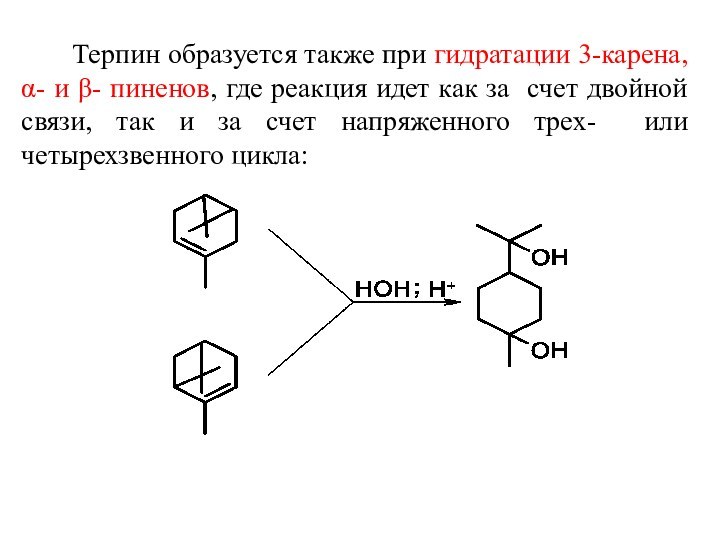
Терпин образуется также
при гидратации 3-карена, α- и β- пиненов, где реакция
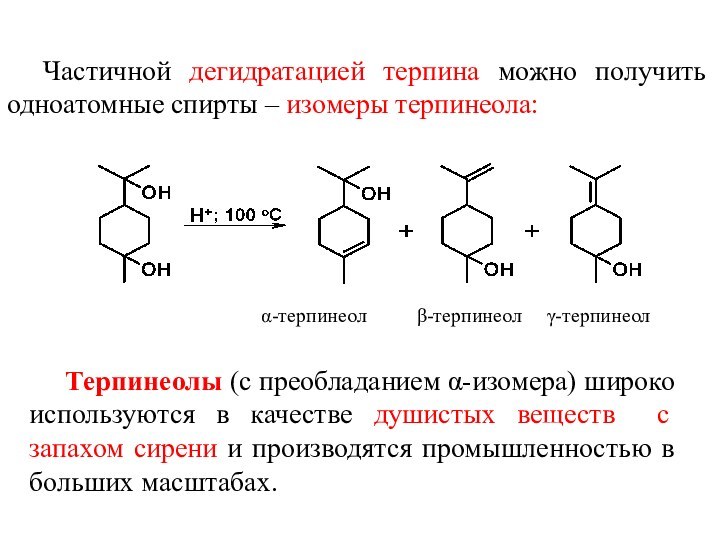
идет как за счет двойной связи, так и за счет напряженного трех- или четырехзвенного цикла:Слайд 28 Частичной дегидратацией терпина можно получить одноатомные спирты –
изомеры терпинеола:
α-терпинеол β-терпинеол γ-терпинеол
Терпинеолы (с преобладанием α-изомера) широко используются в качестве душистых веществ с запахом сирени и производятся промышленностью в больших масштабах.
Слайд 29
4.3 Реакции спиртов
Характерные химические свойства спиртов определяются
гидроксильной группой – функциональной группой данного класса органических соединений. Возможны два варианта разрыва связей с участием группы –ОН:– разрыв связи углерод – кислород ( R-|-OH) с отщеплением гидроксильной группы;
– разрыв связи кислород - водород ( RO-|-H) с отщеплением водорода.
Слайд 30
4.3.1 Реакции дегидратации
(отщепление
-OH)
Дегидратация спиртов, т.е. отщепление воды от
спирта с образованием алкена, является реакцией, обратной реакции гидратации алкенов, рассмотренной ранее. Дегидратация, как и гидратация, катализируется кислотами. Процесс проводят при нагревании, что увеличивает скорость реакции и способствует смещению равновесия вправо (дегидратация – эндотермический процесс; ΔН>0).Слайд 31 Среди ациклических терпеновых
спиртов легко отщепляют воду спирты аллильной структуры – гераниол,
нерол, линалоол. Легче всего реагирует линалоол, у которого спиртовая группа связана с третичным атомом углерода.Под действием кислоты происходит отщепление воды с образованием сопряженных катионов аллильной структуры, отличающихся простран-ственным расположением сопряженной системы:
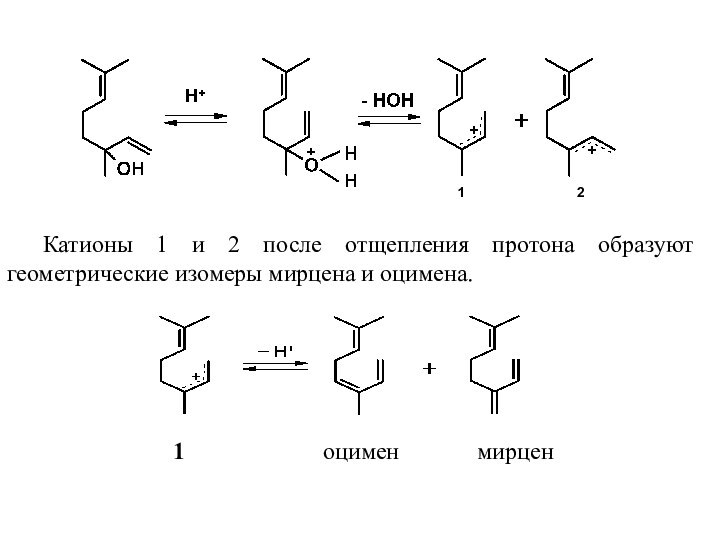
Слайд 32 Катионы 1 и 2 после отщепления протона образуют
геометрические изомеры мирцена и оцимена.
1 2 1 оцимен мирцен
Слайд 33
4.3.2 Реакции с разрывом связи
(
RO-|-H)
Реакции образования сложных эфиров
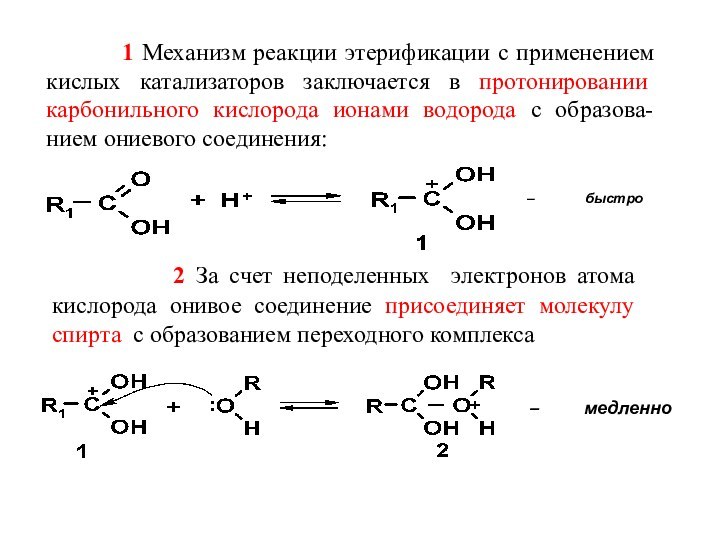
Превращение спиртов в сложные эфиры ацилированием карбоновыми кислотами или их ангидридами протекает с разрывом связи кислород – водород. Механизм реакции с карбоновыми кислотами (реакция этерификации) включает следующие ступени:Слайд 34 1 Механизм реакции
этерификации с применением кислых катализаторов заключается в протонировании карбонильного
кислорода ионами водорода с образова-нием ониевого соединения: 2 За счет неподеленных электронов атома кислорода онивое соединение присоединяет молекулу спирта с образованием переходного комплекса
– быстро
– медленно
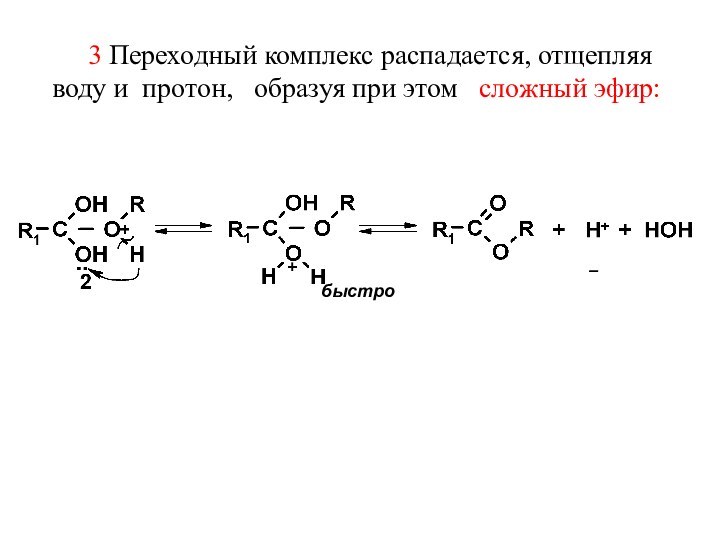
Слайд 35 3 Переходный комплекс распадается, отщепляя воду и протон,
образуя при этом сложный эфир:
– быстроСлайд 36 Особенности реакции этерификации
1 Реакция чувствительна к
пространственным затруднениям. Объемные разветвленные радикалы R и R1 сильно замедляют процесс. Поэтому наиболее легко реагируют первичные спирты и карбоновые кислоты, не имеющие разветвлений у α-звена. Вторичные спирты реагируют в 2 – 10 раз медленнее. Третичные спирты из-за больших стерических препятствий, создаваемых разветвленным радикалом R, образуют сложные эфиры в 10 – 100 раз медленнее. Повышение концентрации катализатора и температуры не приводит к результату, так как в этих условиях третичные спирты претерпевают дегидратацию. Вследствие этого третичные спирты (например, линалоол, терпинеол) не удается превратить в сложные эфиры реакцией с карбоновыми кислотами.Слайд 37 2 Реакция этерификации
обратима. Для повышения степени превращения спиртов применяют избыток одного
из реагентов и удаление воды из сферы реакции.3 Этерификация широко используется в промышленности душистых веществ для производства сложных эфиров первичных спиртов.
4 Более энергично и необратимо протекает взаимодействие спиртов с ангидридами кислот. Ацилирование ангидридами используют для получения сложных эфиров вторичных и третичных спиртов, а также в количественном анализе.
Слайд 38
4.3.3 Окисление спиртов
1 Первичные спирты окисляются до альдегидов. Из гераниола
и нерола действием дихромата натрия в кислой среде получают соответствующие изомеры альдегида цитраля (гераниаль и нераль). Цитронеллол легко окисляется до цитронеллаля.2 Окисление вторичных спиртов приводит к кетонам. Ментол, карвеол окисляются до соответствующих кетонов (ментона, карвона).
3 Третичные спирты в нейтральной среде окисляются трудно с расщеплением углерод-углеродных связей.
Слайд 39 В
кислой среде третичные спирты подвергаются дегидратации, а образовавшиеся алкены
далее легко окисляются по двойным связям до диолов или продуктов деструкции молекулы.Особым образом окисляется линалоол. Дихромат натрия в среде серной и уксусной кислот окисляет этот третичный спирт до альдегида цитраля. Это объясняется аллильной перегруппировкой линалоола в условиях окисления (кислая среда, нагревание) в первичные спирты гераниол и нерол, которые далее окисляются до цитраля:
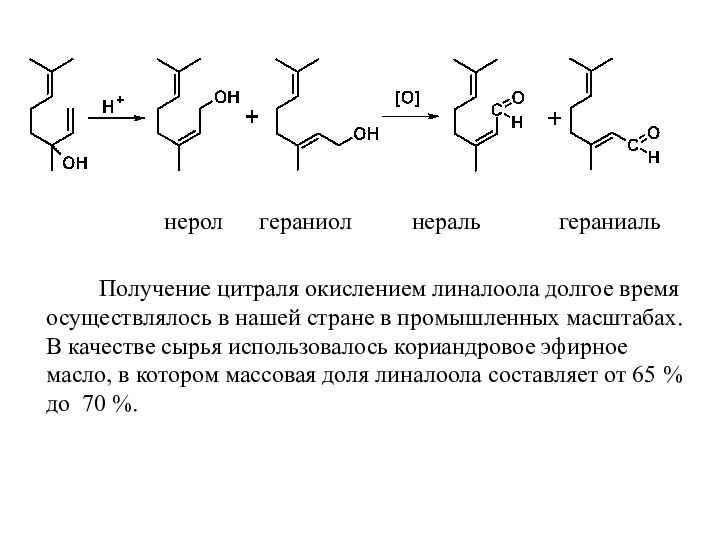
Слайд 40 нерол гераниол
нераль гераниаль
Получение цитраля окислением линалоола долгое время осуществлялось в нашей стране в промышленных масштабах. В качестве сырья использовалось кориандровое эфирное масло, в котором массовая доля линалоола составляет от 65 % до 70 %.
Слайд 41
4.4 Реакции сложных эфиров терпеновых спиртов
Сложные эфиры терпеновых спиртов входят
в состав многих эфирных масел и нередко оказываются главными компонентами масел.Наиболее распространены эфиры уксусной кислоты. В эфирных маслах шалфея, лаванды, бергамота основным и наиболее ценным компонентом является (-)-линалилацетат. В пальмарозовом масле, в цитронелловом, кориандровом маслах присутствует геранилацетат. Борнилацетат – главный компонент масла сибирской пихты. Аромат мятного масла вместе с ментолом и ментоном формирует также ментилацетат.
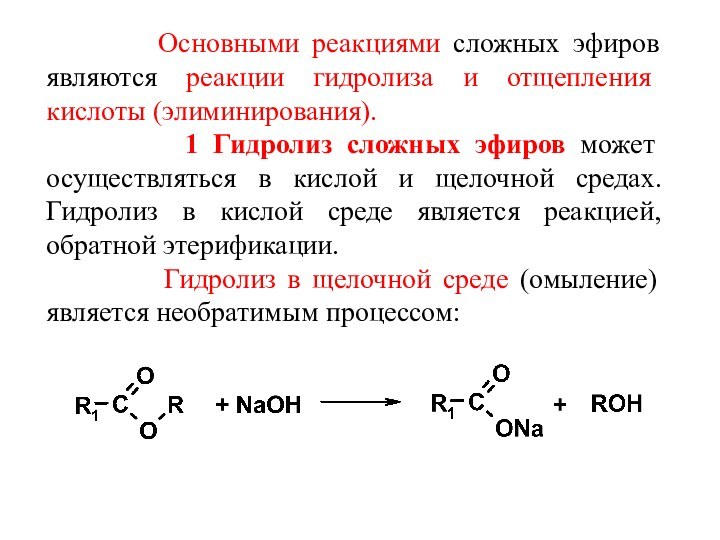
Слайд 42 Основными реакциями сложных
эфиров являются реакции гидролиза и отщепления кислоты (элиминирования).
1 Гидролиз сложных эфиров может осуществляться в кислой и щелочной средах. Гидролиз в кислой среде является реакцией, обратной этерификации.Гидролиз в щелочной среде (омыление) является необратимым процессом:
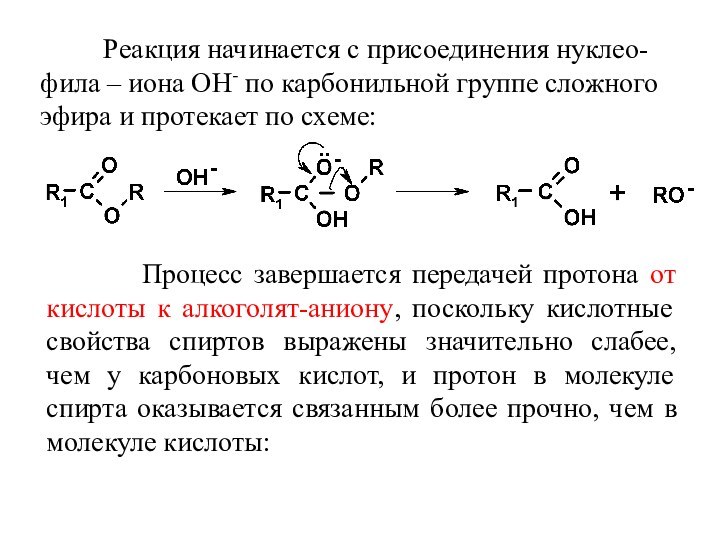
Слайд 43 Реакция начинается с
присоединения нуклео-фила – иона ОН- по карбонильной группе сложного
эфира и протекает по схеме: Процесс завершается передачей протона от кислоты к алкоголят-аниону, поскольку кислотные свойства спиртов выражены значительно слабее, чем у карбоновых кислот, и протон в молекуле спирта оказывается связанным более прочно, чем в молекуле кислоты:
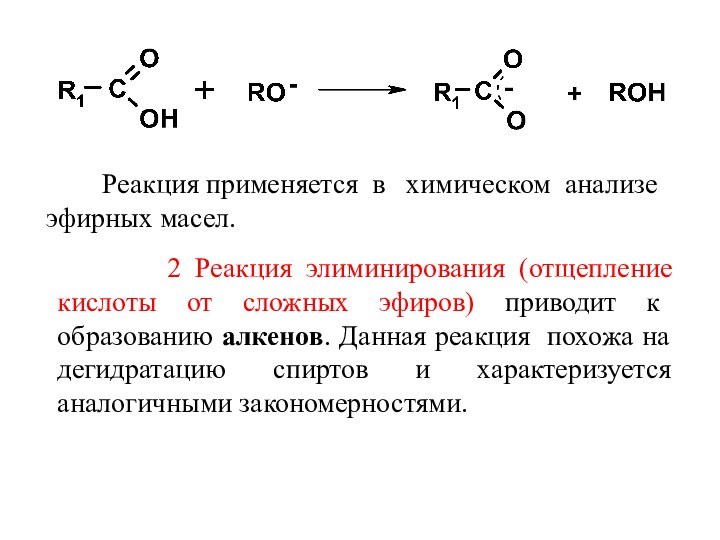
Слайд 44 2 Реакция элиминирования (отщепление
кислоты от сложных эфиров) приводит к образованию алкенов. Данная
реакция похожа на дегидратацию спиртов и характеризуется аналогичными закономерностями. Реакция применяется в химическом анализе эфирных масел.
Слайд 45
4.5 РЕАКЦИИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
Альдегиды и кетоны терпенового ряда
претерпевают все характерные для данного класса органических соединений превращения.
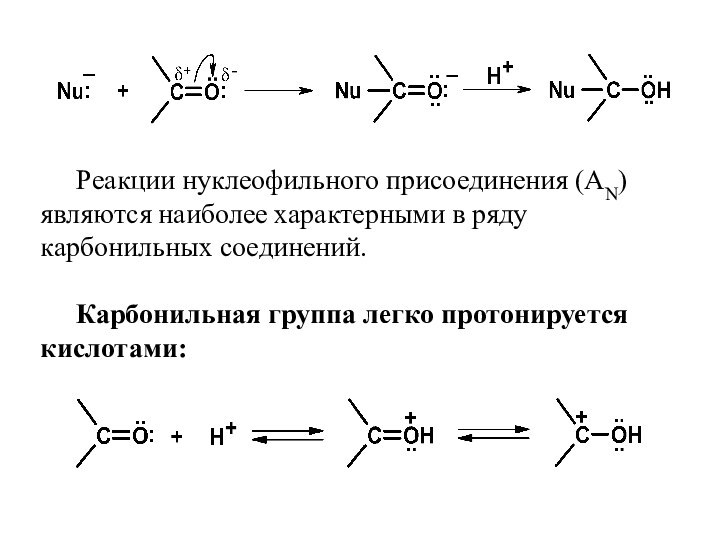
Двойная связь оксогруппы вследствие высокой электроотрицательности атома кислорода имеет полярный характер. При этом наиболее сильно смещено к атому кислорода подвижное электронное облако π-связи, благодаря чему атом углерода несет значительный положительный заряд и может атаковаться нуклеофильными агентами:Слайд 46 Реакции нуклеофильного присоединения (AN) являются наиболее характерными в
ряду карбонильных соединений.
Карбонильная группа легко протонируется кислотами:
Слайд 47
Протонирование приводит к увеличению положительного заряда на атоме углерода,
что способствует повышению скорости реакций с нуклеофилами. В качестве нуклеофилов выступают спирты, производные аммиака, гидросульфит натрия и другие реагенты, имеющие тенденцию образовывать связь с атомом углерода за счет свободной пары электронов.
Слайд 48
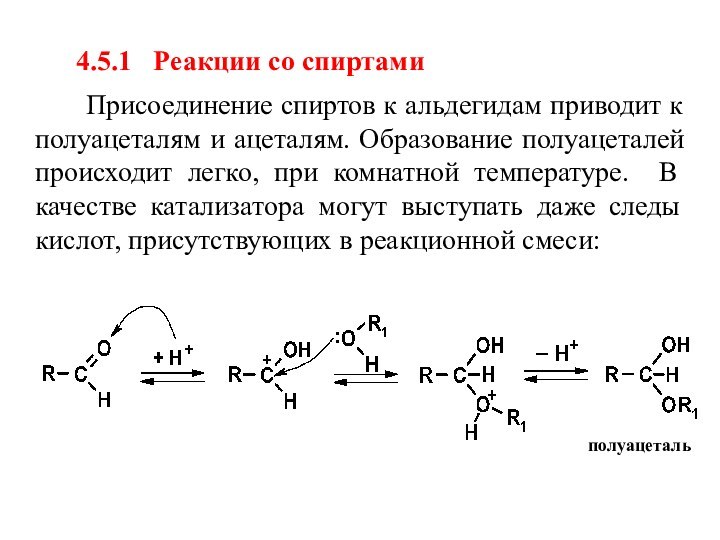
4.5.1 Реакции со спиртами
Присоединение спиртов к альдегидам приводит к полуацеталям
и ацеталям. Образование полуацеталей происходит легко, при комнатной температуре. В качестве катализатора могут выступать даже следы кислот, присутствующих в реакционной смеси:полуацеталь
Слайд 49 Растворы альдегидов в
этаноле, по сути, представляют собой равновесные смеси альдегидов, этанола
и полуацеталей. Запах полуацеталей терпеновых альдегидов приятный, и их образование не является нежелательным в процессах приготовления и созревания парфюмерных жидкостей. В присутствии сильных кислот полуацетали в результате дальнейшей реакции с новой молекулой спирта дают ацетали:
Слайд 50 Реакция ацетализации обратима. Смещение
равновесия вправо может быть достигнуто, как и в случае
реакции этерификации, удалением образую-щейся воды. Образование кеталей протекает значительно труднее в связи с меньшей активностью карбонильной группы кетонов в реакциях нуклеофильного присоединения.
Многие ацетали и кетали являются душистыми веществами и находят применение в парфюмерных композициях и других искусственных душистых смесях. Ацетали более устойчивы при хранении, чем соответствующие альдегиды.
Слайд 51
4.5.2 Реакции с производными аммиака
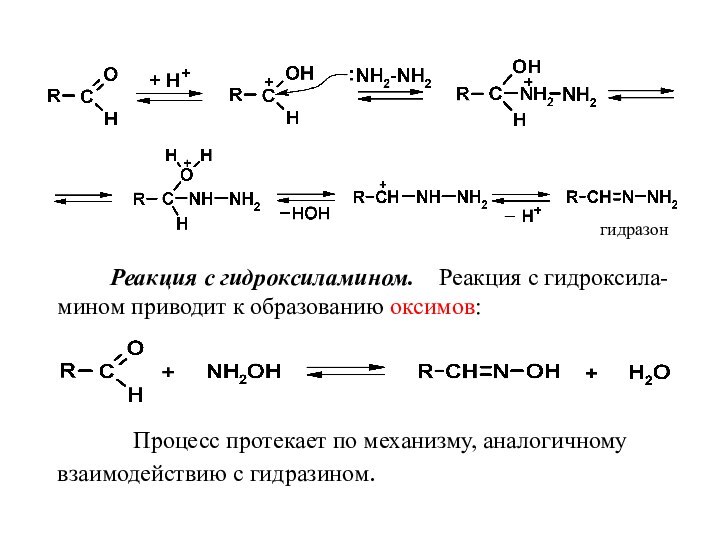
Реакции оксосоединений с аминами, гидроксил-амином, гидразином и его производными
широко применяют в анализе душистых веществ, а также в ряде промышленных синтезов. Реакция с гидразином и его производными.
Реакция с гидразином приводит к образованию гидразонов. Превращение протекает быстро и катализируется кислотами:





























