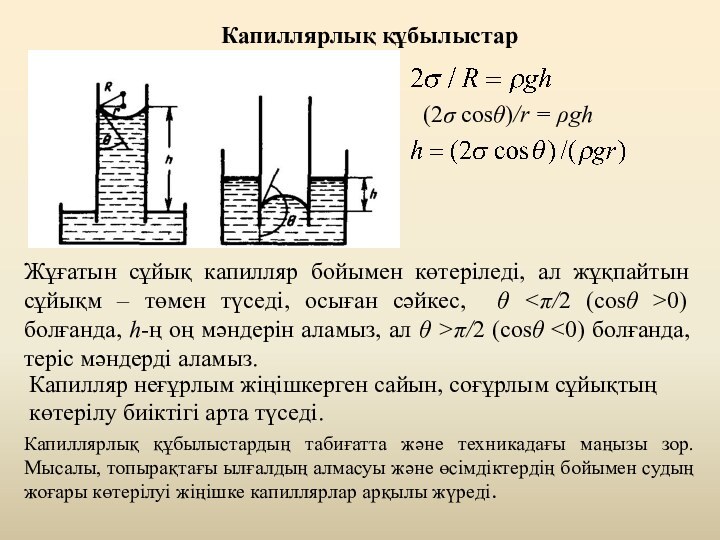
Қасиеттері олардың молекулаларының арасындағы өзара әсерлесуге тәуелді болатын нақты
газдарды қарастырғанда, молекула аралық өзара әсер күштерін ескеру қажет. Бұл күштер 10–9 м қашықтықта әсер етеді және молекулалардың ара қашықтығы артқан сайын, жылдам азаяды. Мұндай күштер жақыннан әсер етуші күштер деп аталады. Пmin<< kT
– зат газ тәрізді күйде болады
Пmin kT – зат сұйық күйде болады
Пmin >> kT – онда зат қатты күйде болады