- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Знакомство с морем кислот
Содержание
- 2. Загадочны морей просторы…Что там – под толщей
- 3. Маршрут нашего путешествия 12345Залив ИнформационныйСтоп! Опасно! Бермудский треугольникГавань Индикаторно – экспериментальнаяБухта ПримененияПролив ЗакрепленияФинишСтарт
- 4. Залив ИнформационныйПланЗнакомство с морем кислот;Разнообразие кислот;Получение кислот.
- 5. Знакомство с морем кислот
- 6. Разнообразие кислотНемало кислот содержится в нашей пище
- 7. Природные кислотыЯблочнаяЛимоннаяАскорбиновая кислота витамин САскорбиновая кислота витамин СМуравьиная кислотаЩавелевая кислота
- 8. Получение кислотСО2+Н2ОН2СО3→
- 9. Стоп! Опасно! Бермудский треугольникТехника безопасности при обращении с кислотами;Оказание первой помощи;3. Физические свойства кислот;План
- 10. Техника безопасности
- 11. Запомни!Сначала вода, затем кислотаИначе может случиться беда!
- 12. Оказание первой помощи при ожогах кислотой
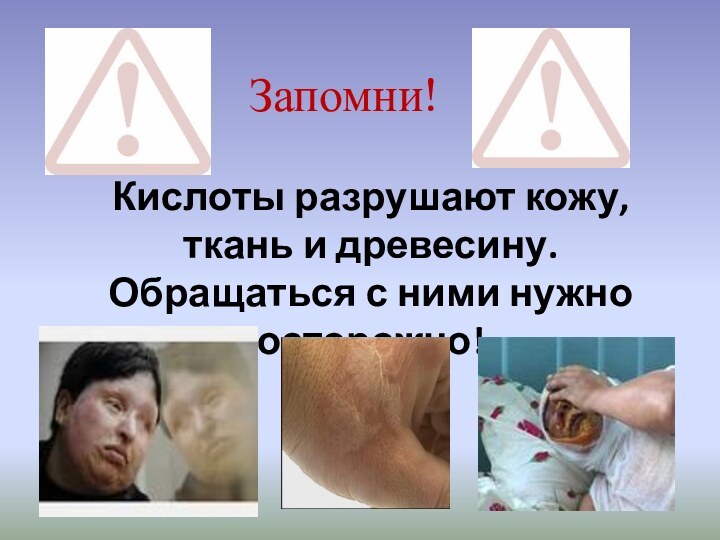
- 13. Запомни!Кислоты разрушают кожу, ткань и древесину. Обращаться с ними нужно осторожно!
- 14. Физические свойства кислот
- 15. Отдохнем?Смотрим, слушаем и повторяем!Море, море – мир
- 16. Гавань Индикаторно - экспериментальнаяХимические свойства кислот;Открытие индикаторов;Исследование химических свойств кислот индикаторами.План
- 17. Химические свойства кислотКислоты реагируют:С металлами (образуется соль
- 18. Открытие индикаторовПостепенно химики научились распознавать кислоты. Однажды
- 19. Запомни!Индикаторы краснеют в кислотах, т.е. в кислой среде!
- 20. Запомни!Кислоты, полученные в лаборатории и кислоты в продуктах питания проявляют общие химические свойства!
- 21. Бухта ПримененияУгольная кислота;Серная кислота;Ортофосфорная кислота;Азотная кислота;Соляная кислота.ПланН2СО3Н2SО4Н3PО4НNО3НСL
- 22. Угольная кислота Н2CО3
- 23. Серная кислота Н2SО4Серную кислоту применяют:в производстве минеральных
- 24. Ортофосфорная кислота Н3РООртофосфорную кислоту применяют:при пайке в
- 25. Азотная кислота НNО3Азотная кислота применяется:в производстве минеральных
- 26. Эта кислота содержится в желудке и выполняет
- 27. Пролив ЗакрепленияПланХимические реакции;Найди соответствие.
- 28. АI + HCI = AICI2+ H2↑Mg +
- 29. Скачать презентацию
- 30. Похожие презентации
Загадочны морей просторы…Что там – под толщей темных вод?Долины, впадины, и горы Веществ сплошной круговорот…К. ПаустовскийИсследование морей кислот


























Слайд 3
Маршрут нашего путешествия
1
2
3
4
5
Залив
Информационный
Стоп! Опасно! Бермудский треугольник
Гавань
Индикаторно –
экспериментальная
Бухта
Применения
Пролив
Закрепления
Финиш
Старт
Слайд 6
Разнообразие кислот
Немало кислот содержится в нашей пище и
лекарствах. Фрукты, овощи, молочные продукты, соусы, приправы ежедневно поставляют
нам целый «букет» кислот: яблочную, винную, кофейную, уксусную, аскорбиновую, камфорную, валериановую и др
Слайд 7
Природные кислоты
Яблочная
Лимонная
Аскорбиновая кислота
витамин С
Аскорбиновая кислота
витамин С
Муравьиная кислота
Щавелевая кислота
Слайд 9
Стоп! Опасно!
Бермудский треугольник
Техника безопасности при обращении с
кислотами;
Оказание первой помощи;
3. Физические свойства кислот;
План
Слайд 15
Отдохнем?
Смотрим, слушаем и повторяем!
Море, море – мир бездомный,
Пенный
шелест волн прибрежных.
Над тобой встают как зори,
Над тобой встают
как зориНашей юности надежды!
Слайд 16
Гавань Индикаторно - экспериментальная
Химические свойства кислот;
Открытие индикаторов;
Исследование химических
свойств кислот индикаторами.
План
Слайд 17
Химические свойства кислот
Кислоты реагируют:
С металлами (образуется соль и
водород).
С основными оксидами (образуется соль и вода).
С основаниями (образуется
соль и вода).С солями (образуется новая соль и новая кислота).
С индикаторами (меняется окраска индикаторов)
Слайд 18
Открытие индикаторов
Постепенно химики научились распознавать кислоты. Однажды английский
химик Р. Бойль, изучая свойства соляной кислоты, случайно пролил
её на лепестки синей фиалки – лепестки стали красными. Так были открыты индикаторы.
Слайд 20
Запомни!
Кислоты, полученные в лаборатории
и кислоты в продуктах
питания
проявляют общие химические свойства!
Слайд 21
Бухта Применения
Угольная кислота;
Серная кислота;
Ортофосфорная кислота;
Азотная кислота;
Соляная кислота.
План
Н2СО3
Н2SО4
Н3PО4
НNО3
НСL
Слайд 23
Серная кислота Н2SО4
Серную кислоту применяют:
в производстве минеральных удобрений;
как
электролит в свинцовых аккумуляторах;
для получения различных минеральных кислот и
солей;в производстве химических волокон, красителей, дымообразующих веществ и взрывчатых веществ;
в нефтяной, металлообрабатывающей, текстильной, кожевенной и др. отраслях промышленности.
Слайд 24
Ортофосфорная кислота Н3РО
Ортофосфорную кислоту применяют:
при пайке в качестве
флюса (по окисленой меди, по чёрному металлу, по нержавеющей
стали);для исследований в области молекулярной биологии;
для очищения от ржавчины металлических поверхностей;
в пищевой промышленности;
в сельском хозяйстве. В звероводстве (в частности, при выращивании норок);
в стоматологии.
Слайд 25
Азотная кислота НNО3
Азотная кислота применяется:
в производстве минеральных удобрений;
в
военной промышленности;
в фотографии — подкисление некоторых тонирующих растворов;
в станковой графике
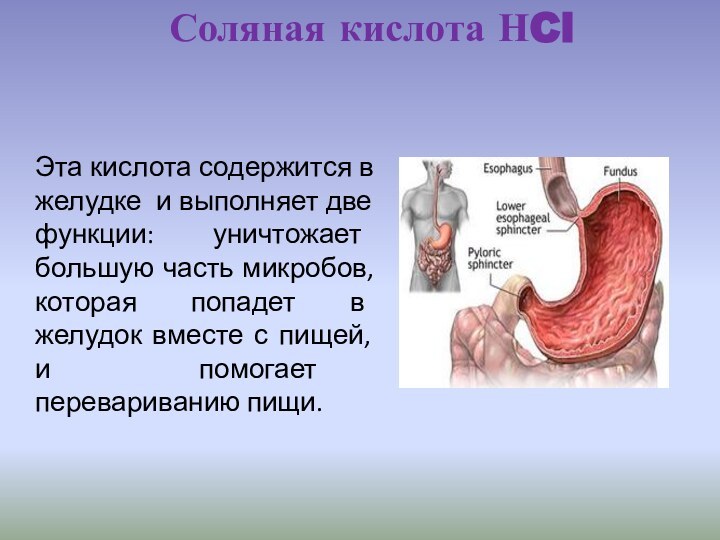
— для травления печатных форм.Слайд 26 Эта кислота содержится в желудке и выполняет две
функции: уничтожает большую часть микробов, которая попадет в желудок
вместе с пищей, и помогает перевариванию пищи.Соляная кислота НCl