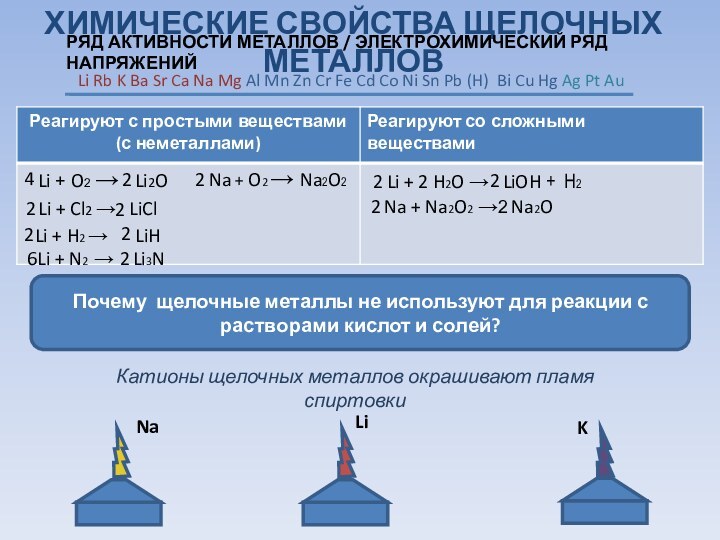
светлое тело, которое ковать можно».
Самый тугоплавкий.
Самый распространенный на земле.
Самый
легкий.Самый электропроводный.
Самый твердый .
Самый пластичный.
Самый легкоплавкий.
Самый тяжелый.
Самый космический.
Л
О
М
О
Н
О
С
О
В
Au
Os
Cr
Hg
Li
W
Fe
Al
Ag
МЕТАЛЛЫ - ЧЕМПИОНЫ




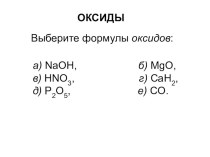
![Щелочные металлы ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ I ГРУППЫ ГЛАВНОЙ ПОДГРУППЫ LiNaKRbCsFr7233985133[223]2s13s14s15s16s17s1))))))))))))))))))))))))))) усиливаются усиливаютсяЭлементАrВалентные электроныЧисло](/img/tmb/12/1167876/1f7445c2c1dacc5fe84be6c0414d8af2-720x.jpg)