- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Периодическая система Д.И. Менделеева (Занятие 3)
Содержание
- 2. Периодический закон:свойства элементов, а также свойства образуемых
- 3. Периодическая система (таблица) - это графическое выражение Периодического закона.
- 6. Порядковый номер – наиболее важная характеристика элемента.Порядковый
- 7. Группы - вертикальные столбцы.В периодической системе 8 групп.Группы делятся на подгруппы.
- 8. Подгруппы:Главные (А) – содержат элементы малых и больших периодов.Побочные (Б) – содержат элементы только больших периодов.
- 10. Атомы элементов одной группы имеют одинаковое число валентных электронов и, следовательно, одинаковую высшую степень окисления.
- 11. Период - Горизонтальный ряд элементов, расположенных в порядке возрастания зарядов ядер атомов.
- 13. Каждый период начинается щелочным металлом и заканчивается инертным газом.
- 14. Номер периода указывает на число энергетических уровней, на которых расположены электроны в этом атоме.
- 16. На что указывает порядковый номер элемента?
- 17. Порядковый номер элемента указывает на общее число электронов атоме.
- 18. Изменение свойств элементов в главных подгруппах и периодах
- 19. Химическая связь и строение веществаХимическая связь – это взаимодействие, в результате которого образуется устойчивая межатомная система.
- 20. Типы химических связейКовалентная.Ионная.Металлическая.Водородная.
- 21. Химическая связь — это связь между атомами,
- 22. ИоннаяХимическая связьКовалентнаяМеталлическая
- 23. Ковалентная связь — химическая связь, возникающая в результате образования общих электронных пар.
- 24. ПолярнаяКовалентная связьНеполярная
- 25. Электроотрицательность — это способность атомов химического элемента
- 26. Валентность — это число ковалентных связей, которыми
- 29. Ковалентная связьОсуществляется за счет образования общих электронных
- 30. Ковалентная неполярная связь – образование молекулы водорода.
- 31. Образование молекул водорода, хлора и азота.
- 32. Ковалентная полярная связь образуется между атомами (обычно неметаллов), отличающимися по электроотрицательности.
- 33. Связывающая электронная пара смещена к более электроотрицательному атому хлора.
- 34. Характеристики связиДлина.Энергия.
- 35. Длина связи – расстояние между ядрами взаимодействующих
- 36. Ионная связь – осуществляется за счет электростатического
- 37. Взаимодействие атомов натрия и хлора
- 39. В твердом (кристаллическом) состоянии каждый положительно заряженный
- 40. Каждый ион натрия окружен шестью хлорид-ионами, а каждый хлорид-ион шестью ионами натрия.
- 41. Металлическая связь – осуществляется между атомами с
- 42. В узлах кристаллической решетки положительные ионы.Подвижные электроны
- 43. Свойства металлов:Электропроводность.Теплопроводность.Металлический блеск.Пластичность.Ковкость.
- 45. Водородная связь – возникает между молекулами, в
- 46. За счет водородных связей происходит ассоциация (объединение) молекул.
- 47. Электроотрицательность – способность атома в соединении смещать к себе электронную плотность от соседних атомов.
- 49. Электроотрицательность химических элементов изменяется периодически:в группе с увеличением заряда ядра – ЭО уменьшается;в периоде – возрастает.
- 51. Углерод более ЭО, чем водород, но менее
- 52. В реакции с водородом кислород: окислитель/восстановитель?В реакции с хлором кислород: окислитель/восстановитель?
- 53. Углерод более ЭО, чем водород, но менее ЭО, чем хлор.
- 54. Валентность – способность атомов химического элемента к образованию химических связей.
- 55. Валентность определяется числом:неспаренных электронов (одноэлектронных орбиталей);неподеленных электронных пар;вакантных свободных орбиталей.
- 59. Степень окисления – условный заряд атома в
- 60. Степень окисления может быть отрицательной, нулевой и положительной.
- 66. Скачать презентацию
- 67. Похожие презентации
Периодический закон:свойства элементов, а также свойства образуемых ими соединений находятся в периодической зависимости от величины заряда ядер их атомов.






























































Слайд 6
Порядковый номер – наиболее важная характеристика элемента.
Порядковый номер
указывает на число протонов в ядре и число электронов
в атоме.
Слайд 8
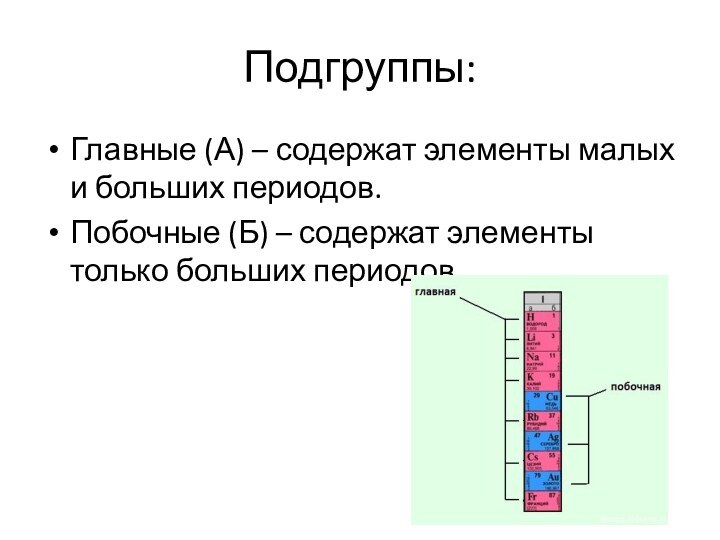
Подгруппы:
Главные (А) – содержат элементы малых и больших
периодов.
Побочные (Б) – содержат элементы только больших периодов.
Слайд 10
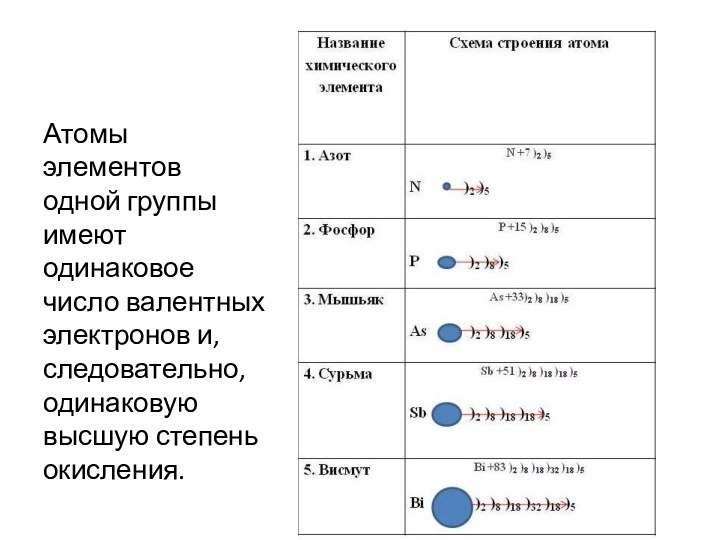
Атомы элементов одной группы имеют одинаковое число валентных
электронов и, следовательно, одинаковую высшую степень окисления.
Слайд 11
Период -
Горизонтальный ряд элементов, расположенных в порядке
возрастания зарядов ядер атомов.
Слайд 14
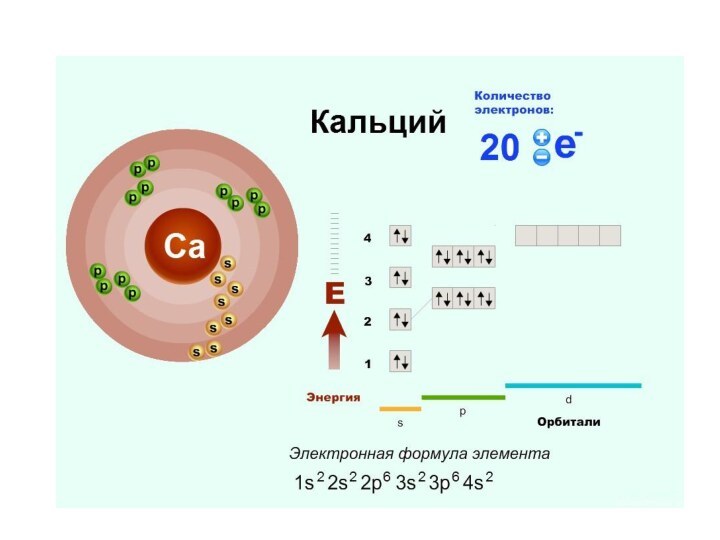
Номер периода указывает на число энергетических уровней, на
которых расположены электроны в этом атоме.
Слайд 19
Химическая связь и строение вещества
Химическая связь – это
взаимодействие, в результате которого образуется устойчивая межатомная система.
Слайд 21
Химическая связь — это связь между атомами, осуществляемая
в молекулах и кристаллах вещества с помощью энергии электронов,
входящих в состав атомов.+
+
+
—
—
—
Слайд 23
Ковалентная связь — химическая связь, возникающая в результате
образования общих электронных пар.
Слайд 25
Электроотрицательность — это способность атомов химического элемента смещать
к себе общие электронные пары, участвующие в образовании химической
связи.
Слайд 26
Валентность — это число ковалентных связей, которыми атом
одного химического элемента связан с атомами этого же или
других элементов.
Слайд 29
Ковалентная связь
Осуществляется за счет образования общих электронных пар.
Ковалентная
неполярная связь образуется между атомами одного и того же
химического элемента.
Слайд 32
Ковалентная полярная связь образуется между атомами (обычно неметаллов),
отличающимися по электроотрицательности.
Слайд 35
Длина связи – расстояние между ядрами взаимодействующих атомов.
Энергия
связи – энергия, выделяющаяся при образовании одного моля связей
(кДж/моль).
Слайд 36
Ионная связь – осуществляется за счет электростатического взаимодействия
ионов с разными зарядами.
Ион – заряженная частица, которая образуется
при присоединении электрона к атому или молекуле / или при отдаче электрона атомом или молекулой.
Слайд 39
В твердом (кристаллическом) состоянии каждый положительно заряженный ион
взаимодействует не с одним отрицательно заряженным ионом, а со
множеством. Это является следствием ненаправленности и ненасыщаемости ионной связи.
Слайд 41
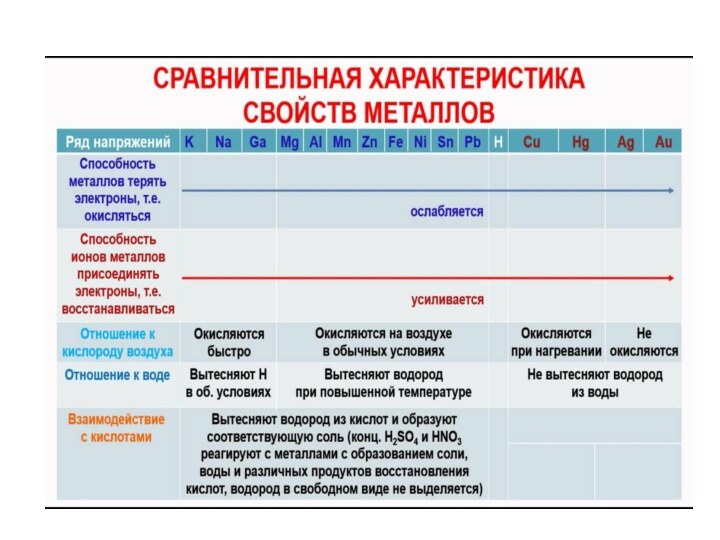
Металлическая связь – осуществляется между атомами с небольшим
числом валентных электронов, слабо удерживаемых ядром, и большим числом
валентных орбиталей.Металлическая связь существует в твердых металлах и их сплавах.





























