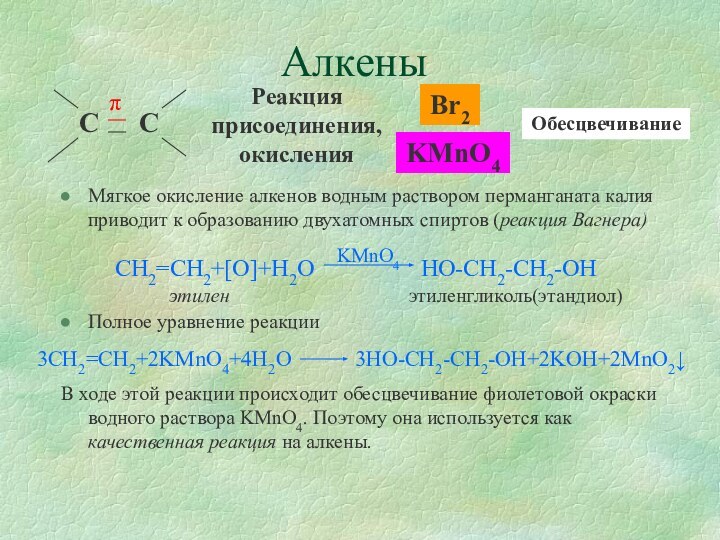
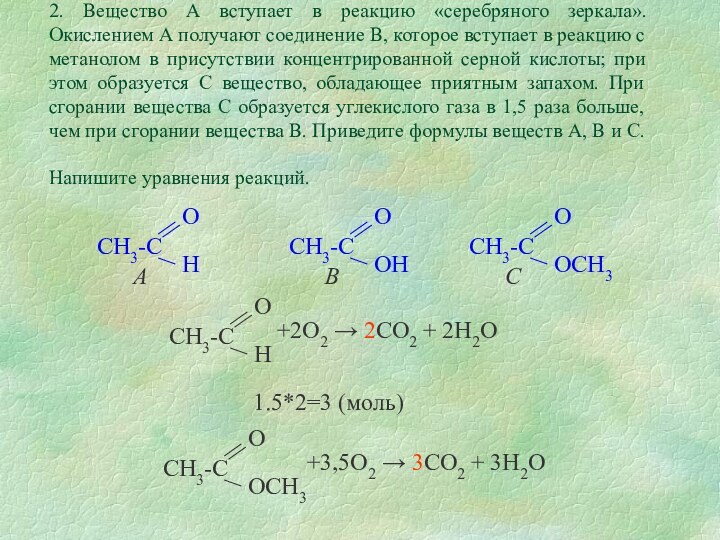
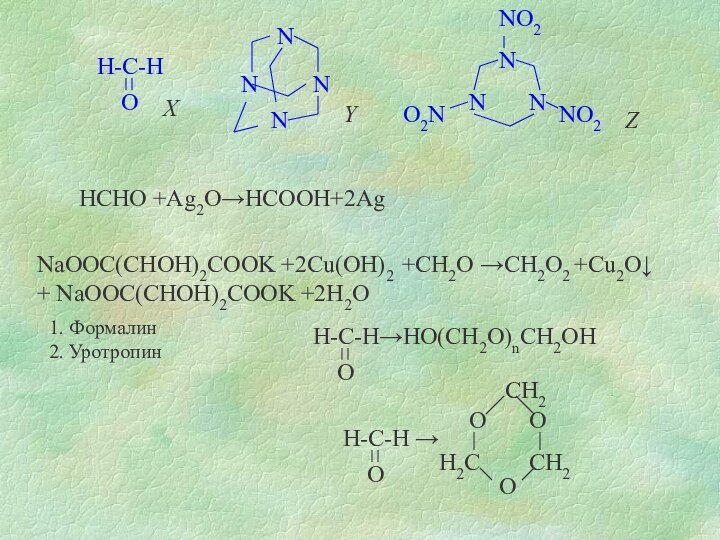
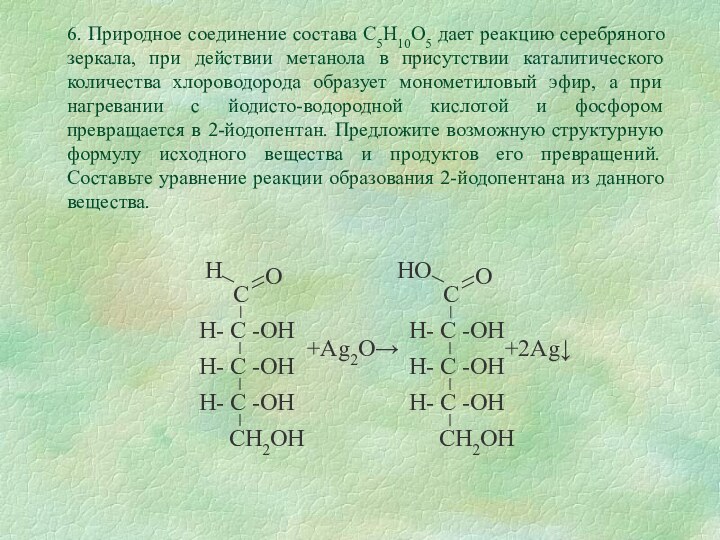
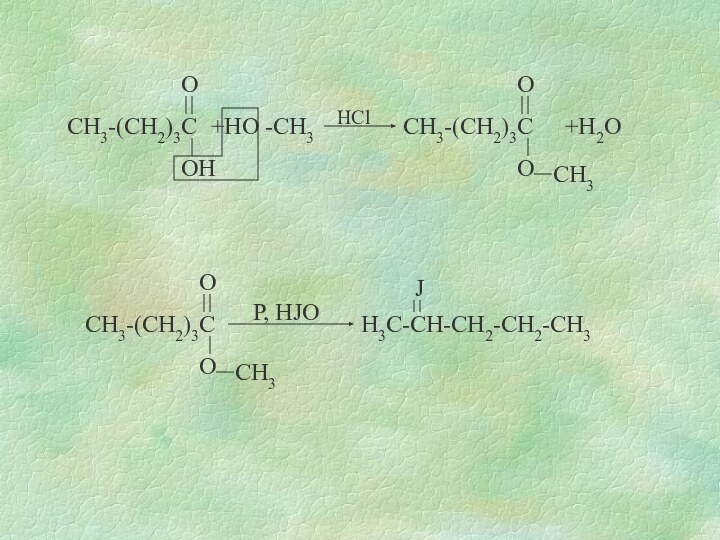
к образованию двухатомных спиртов (реакция Вагнера)
Реакция присоединения, окисления
Br2
KMnO4
Обесцвечивание
Полное уравнение
реакцииВ ходе этой реакции происходит обесцвечивание фиолетовой окраски водного раствора KMnO4. Поэтому она используется как качественная реакция на алкены.