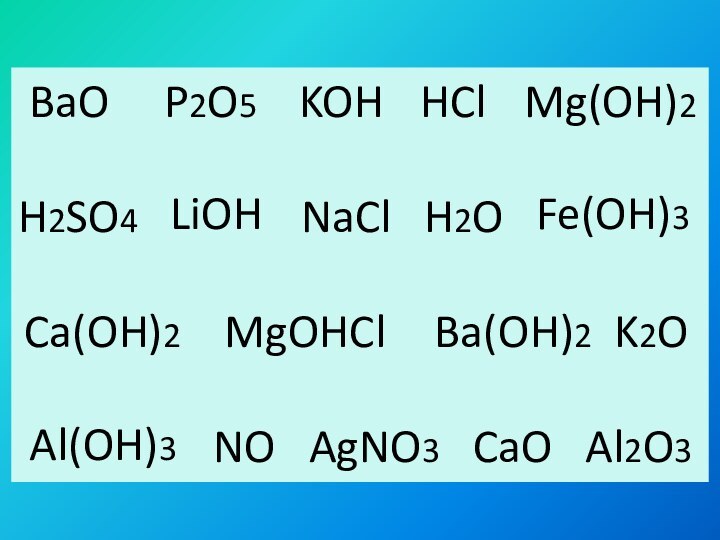
HCl
H2SO4 NaCl H2O
MgOHCl K2O
NO AgNO3 CaO Al2O3
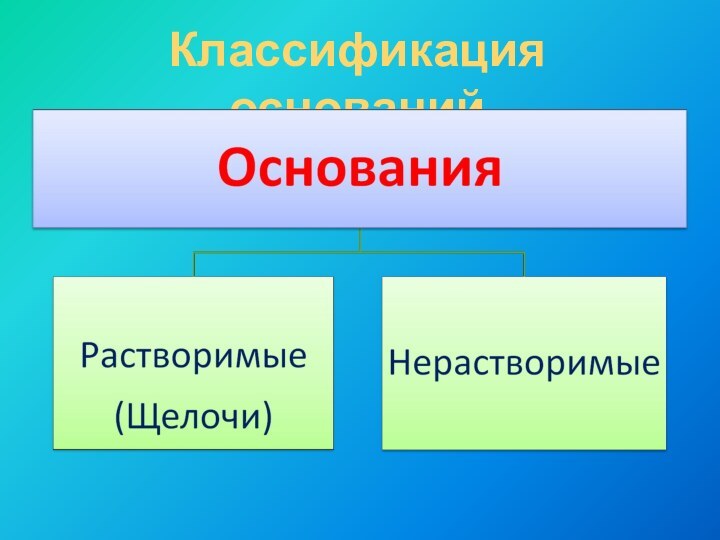
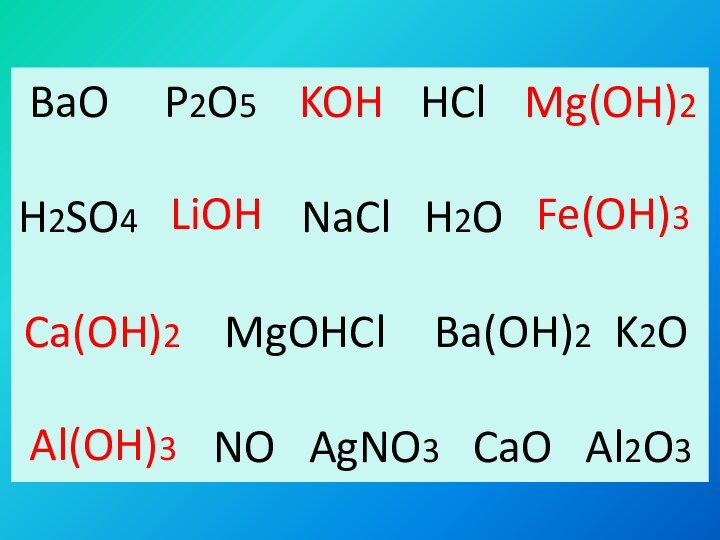
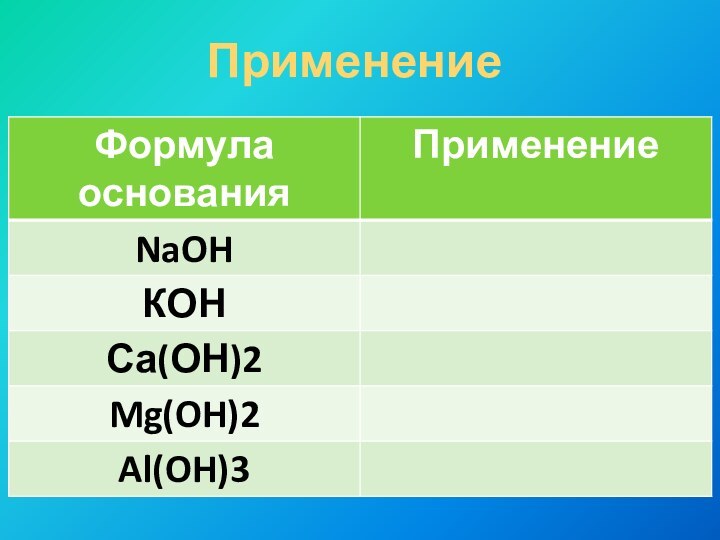
KOH
Mg(OH)2
LiOH
Fe(OH)3
Ca(OH)2
Ba(OH)2
Al(OH)3
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть





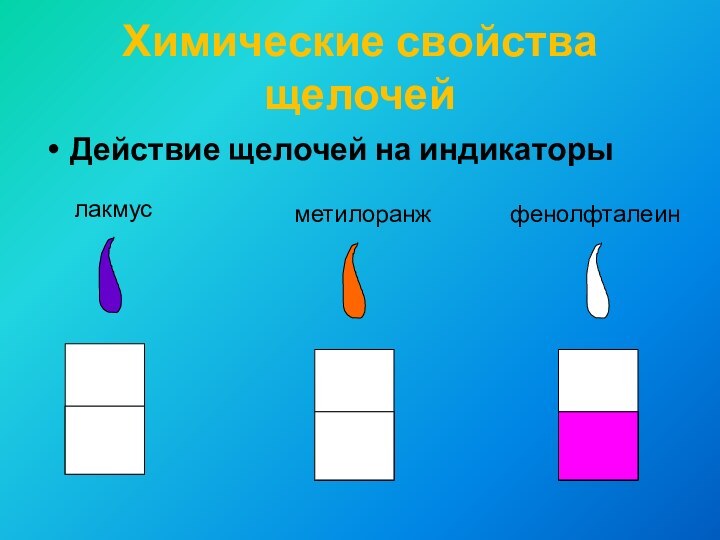



KOH
Mg(OH)2
LiOH
Fe(OH)3
Ca(OH)2
Ba(OH)2
Al(OH)3
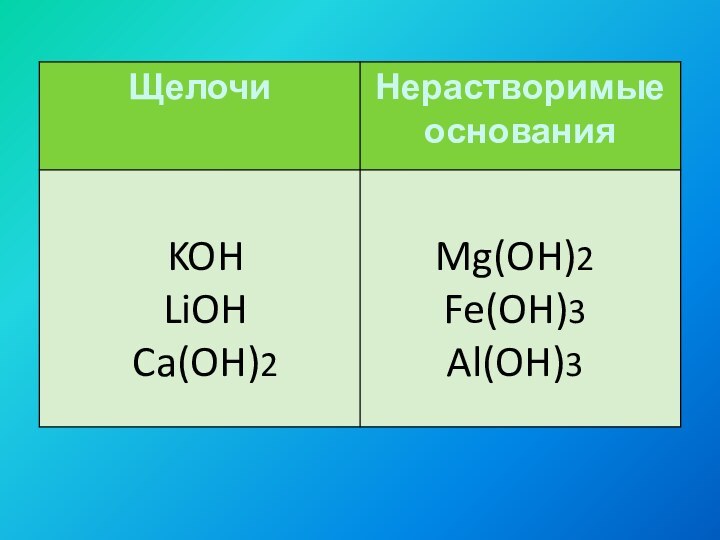
KOH
Mg(OH)2
LiOH
Fe(OH)3
Ca(OH)2
Ba(OH)2
Al(OH)3
2. Оксид активного металла + + вода = щелочь
CaO + H2O = Ca(OH)2
Соль (в растворе)+ щелочь =
= нерастворимое основание +
+ другая соль
FeCl3 + 3NaOH = Fe(OH)3 +
+ 3NaCl