- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Классификация органических соединений
Содержание
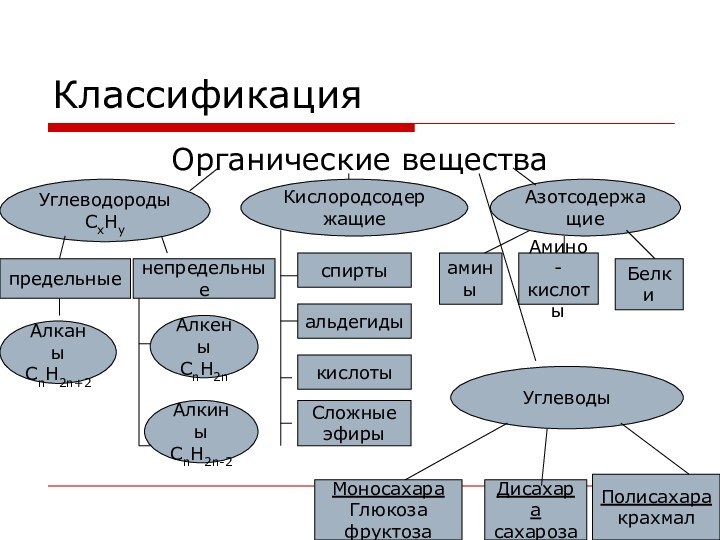
- 2. Классификация Органические веществаУглеводородыСхНуКислородсодержащие Азотсодержащие Углеводы предельныенепредельныеАлканыСnH2n+2АлкиныСnH2n-2АлкеныСnH2nспиртыальдегидыкислотыСложныеэфирыаминыАмино-кислотыБелки МоносахараГлюкозафруктозаДисахарасахарозаПолисахаракрахмал
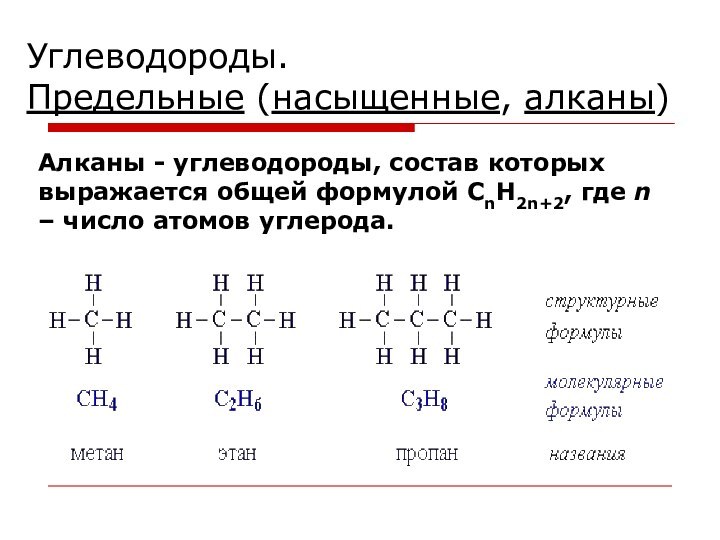
- 3. Углеводороды. Предельные (насыщенные, алканы) Алканы - углеводороды,
- 5. Гомологи – вещества одного класса, отличающиеся друг
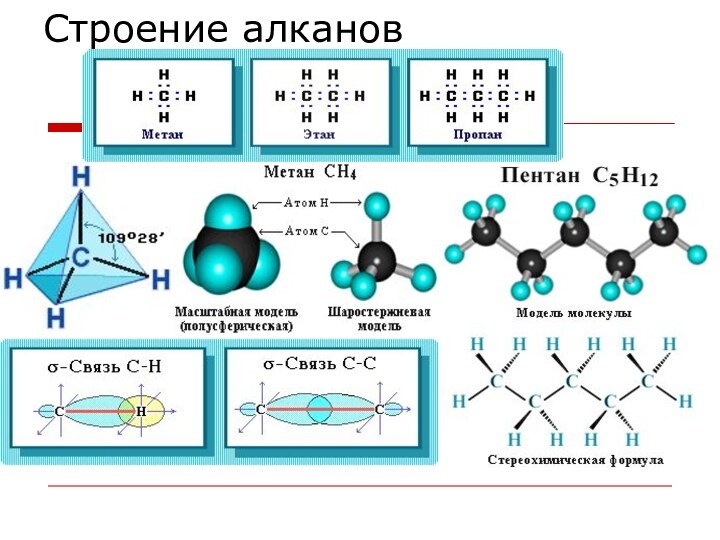
- 6. Строение алканов
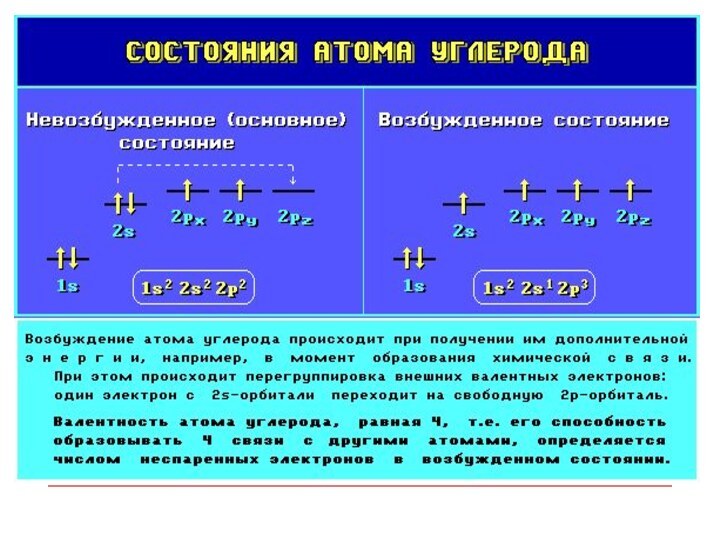
- 8. Атомные орбитали Атомная орбиталь (АО) - область
- 9. Гибридизация АО - это взаимодействие (смешение) разных
- 11. сигма-Связь - ковалентная связь, образованная при перекрывании
- 13. Задание.Построить и назвать изомеры для гексана.
- 14. Алгоритм построения изомеров для алкановПо корню слова
- 15. Пускают разветвление с другой стороныС – С
- 16. Доставить атомы водорода с учётом, что углерод
- 17. Порядок построения названия1.Выбрать в молекуле главную углеродную
- 18. Порядок построения названия2. Пронумеровать атомы углерода в
- 19. Порядок построения названия3. Указать в префиксе (приставке)
- 20. Порядок построения названия4. Записать корень, соответствующий числу
- 21. Таким образом, в названии разветвленного алкана корень+суффикс
- 22. Назовём полученные изомерыСН3 – СН2 – СН2
- 23. Химические свойства алкановТак как все связи насыщены
- 24. алкеныАлкены (этиленовые углеводороды, олефины) - непредельные алифатические
- 26. пи-Связьпи-Связь - ковалентная связь, возникающая при боковом
- 27. Алкены. Строение
- 28. Номенклатура алкенов По систематической номенклатуре названия алкенов
- 29. Изомерия алкенов Изомерия углеродного скелета (начиная с
- 30. Химические свойства алкенов. Характерны реакции присоединения
- 31. Реакция полимеризацииCH2=CH2 + CH2=CH2 + CH2=CH2 +
- 32. Реакции окисленияПолное окисление (горение)С2Н4 + 3O2 =
- 33. алкиныАлкины (ацетиленовые углеводороды) – непредельные углеводороды, молекулы
- 35. Номенклатура алкиновПо систематической номенклатуре названия ацетиленовых углеводородов
- 36. Химические свойства алкиновКак и для этиленовых характерны
- 37. Функциональная группа – группа атомов, обеспечивающая химические свойства органических веществ
- 38. Спирты.Спирты – производные углеводородов, в которых углеводородный
- 39. Многоатомные спиртыЭтиленгликоль – двухатомный спирт СН2 –
- 40. Многоатомные спиртыГлицерин – трёхатомный спиртСН2 – СН
- 41. Химические свойства спиртов обусловлены наличием функциональной группы
- 42. Альдегиды – производные углеводородов, в молекуле которых
- 43. Карбоновые кислотыКарбоновые кислоты - органические соединения, содержащие
- 44. Систематические названия кислот даются по названию соответствующего
- 45. Химические свойстваКарбоксильная группа содержит две функциональные группы
- 46. Характерны реакции с:Со спиртами (реакция этерификации)Продуктом является
- 47. С солями более слабых карбоновых кислот Составьте
- 48. Жиры.Жиры - сложные эфиры глицерина и высших
- 49. Жидкие жиры превращают в твердые путем реакции
- 50. Углеводы (сахара) - органические вещества, состав которых
- 51. Моносахариды Моносахариды - гетерофункциональные соединения, в состав
- 52. Дисахариды.это углеводы, молекулы которых состоят из двух
- 53. Крахмал В его состав входят:амилоза (внутренняя часть
- 54. Аминокислоты – органические бифункциональные соединения, в
- 55. Физические свойства Аминокислоты – твердые кристаллические вещества
- 56. Химические свойстваАминокислоты проявляют свойства оснований за счет
- 57. Практическое значение имеет внутримолекулярное взаимодействие функциональных групп
- 58. Белки
- 59. Белки (полипептиды) - биополимеры, построенные из остатков
- 60. Уровни структурной организации белков.
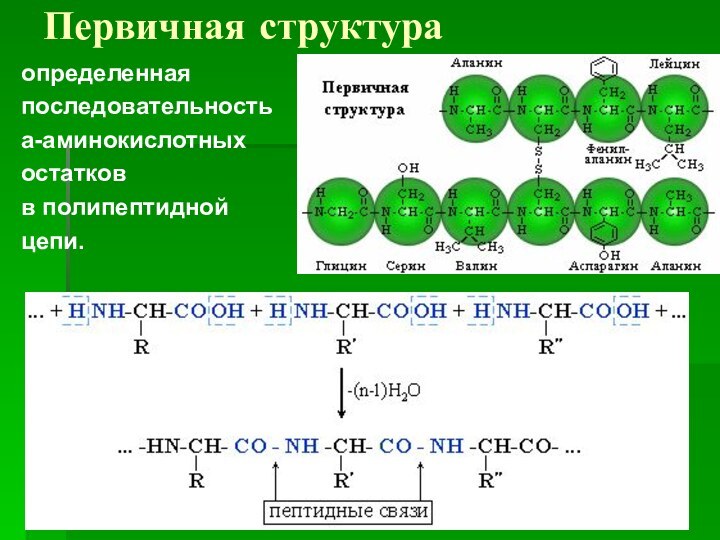
- 61. Первичная структураопределенная последовательность a-аминокислотных остатков в полипептидной цепи.
- 62. Вторичная структураконформация полипептидной цепи, закрепленная множеством водородных
- 63. Третичная структура - форма закрученной спирали в
- 64. Четвертичная структура -агрегаты нескольких белковых макромолекул(белковые комплексы), образованные за счет взаимодействия разных полипептидных цепей.
- 65. Скачать презентацию
- 66. Похожие презентации
Классификация Органические веществаУглеводородыСхНуКислородсодержащие Азотсодержащие Углеводы предельныенепредельныеАлканыСnH2n+2АлкиныСnH2n-2АлкеныСnH2nспиртыальдегидыкислотыСложныеэфирыаминыАмино-кислотыБелки МоносахараГлюкозафруктозаДисахарасахарозаПолисахаракрахмал











































Слайд 2
Классификация
Органические вещества
Углеводороды
СхНу
Кислородсодержащие
Азотсодержащие
Углеводы
предельные
непредельные
Алканы
СnH2n+2
Алкины
СnH2n-2
Алкены
СnH2n
спирты
альдегиды
кислоты
Сложные
эфиры
амины
Амино-
кислоты
Белки
Моносахара
Глюкоза
фруктоза
Дисахара
сахароза
Полисахара
крахмал
Слайд 5 Гомологи – вещества одного класса, отличающиеся друг от
друга на одну или несколько групп – СН2 –
Гомологический ряд – ряд веществ, расположенных в порядке возрастания относительных молекулярных масс, сходных по строению и свойствам, но отличающиеся друг от друга на одну или несколько групп – СН2 –
Слайд 8
Атомные орбитали
Атомная орбиталь (АО) - область наиболее вероятного
пребывания электрона (электронное облако) в электрическом поле ядра атома.
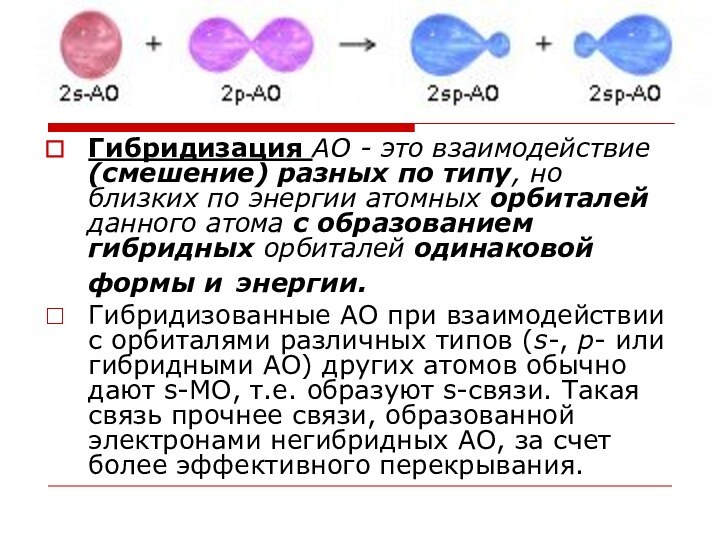
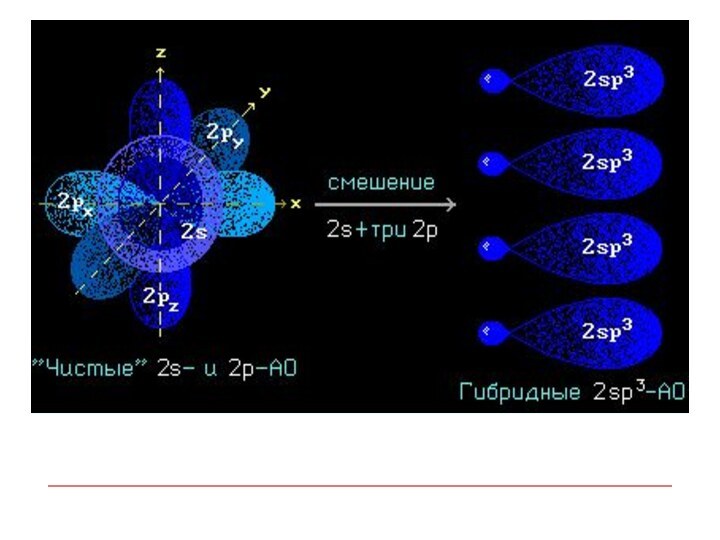
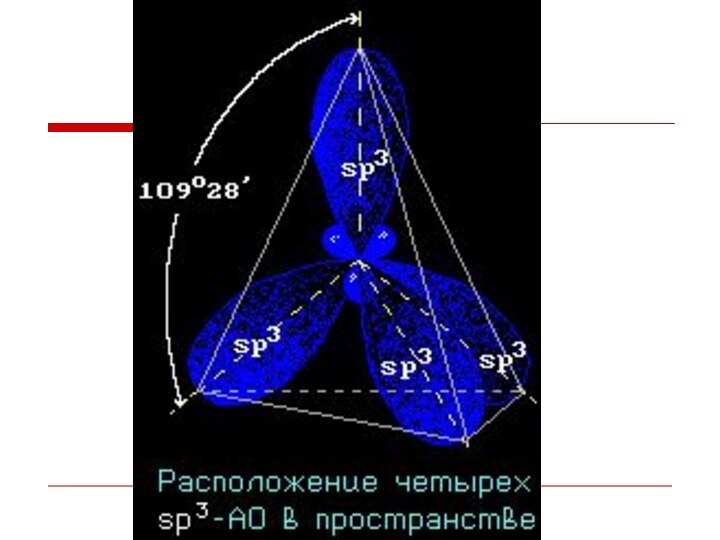
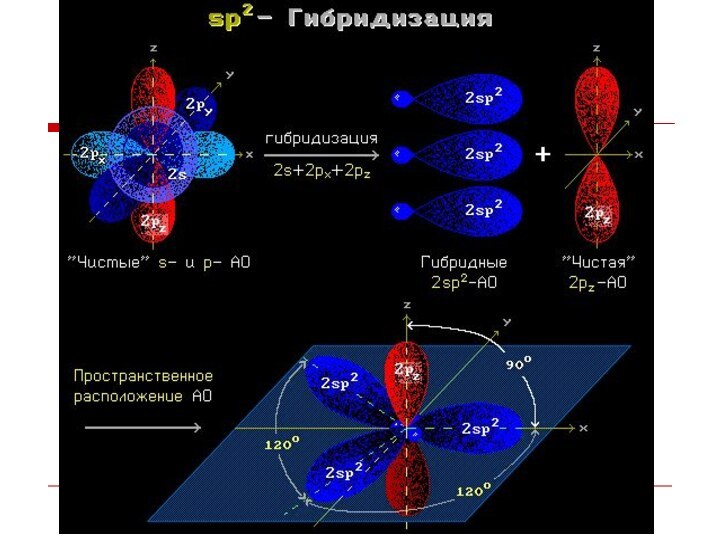
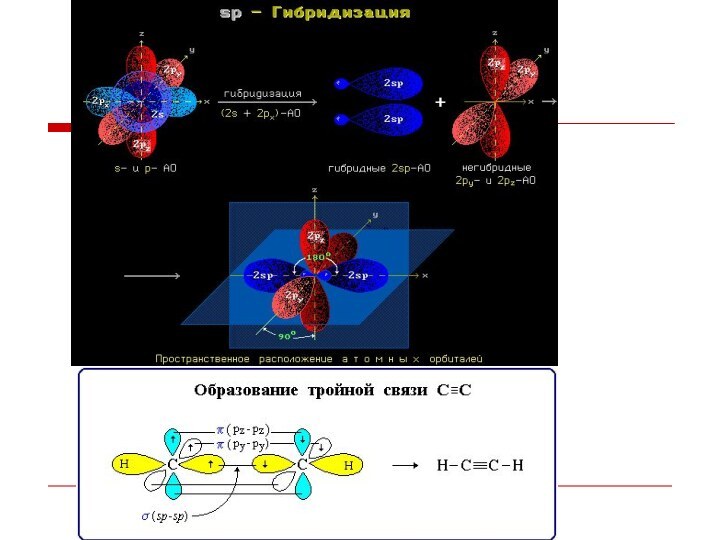
Слайд 9 Гибридизация АО - это взаимодействие (смешение) разных по
типу, но близких по энергии атомных орбиталей данного атома
с образованием гибридных орбиталей одинаковой формы и энергии.Гибридизованные АО при взаимодействии с орбиталями различных типов (s-, р- или гибридными АО) других атомов обычно дают s-МО, т.е. образуют s-связи. Такая связь прочнее связи, образованной электронами негибридных АО, за счет более эффективного перекрывания.
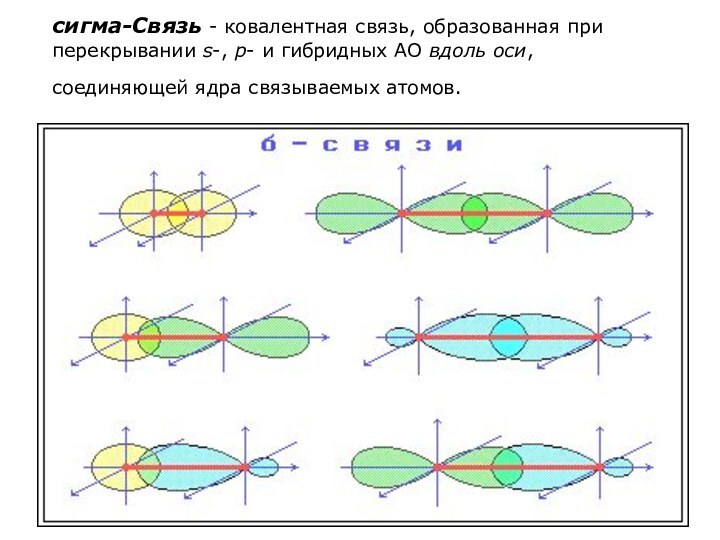
Слайд 11 сигма-Связь - ковалентная связь, образованная при перекрывании s-,
p- и гибридных АО вдоль оси, соединяющей ядра связываемых
атомов.
Слайд 14
Алгоритм построения изомеров для алканов
По корню слова строят
углеродный скелет (гекса – 6 атомов углерода) С –
С – С – С – С – С это первый изомер.Пускают разветвление с одной стороны (кроме последних атомов углерода)
С – С – С – С – С
С это второй изомер
Слайд 15
Пускают разветвление с другой стороны
С – С –
С – С
С С это
третий изомерМожно сделать 2 разветвления у одного атома углерода кроме последних
С
С – С – С – С
С это четвёртый изомер
Слайд 16
Доставить атомы водорода с учётом, что углерод 4-хвалентен
СН3
– СН2 – СН2 – СН2 – СН2 –
СН3СН3 – СН2 – СН2 – СН2 – СН3
СН3
СН3 – СН2 – СН2 – СН3
СН3 СН3
СН3
СН3 – СН2 – СН2 – СН3
СН3
Слайд 17
Порядок построения названия
1.Выбрать в молекуле главную углеродную цепь.
Во-первых, она должна быть самой длинной. Во-вторых, если имеются
две или более одинаковые по длине цепи, то из них выбирается наиболее разветвленная. Например, в молекуле есть 2 цепи с одинаковым числом (7) атомов С (выделены цветом):В случае (а) цепь имеет 1 заместитель, а в (б) – 2. Поэтому следует выбрать вариант (б).
Слайд 18
Порядок построения названия
2. Пронумеровать атомы углерода в главной
цепи с той стороны, к которой ближе радикалы, или
старший заместитель, или кратная связь (в зависимости от класса веществ) Например:
Слайд 19
Порядок построения названия
3. Указать в префиксе (приставке) положение
(номер атома углерода) и название радикала, заместителя, функциональной группы
в алфавитном порядке. Если есть несколько одинаковых заместителей, то для каждого из них через запятую записывается цифра (местоположение), а их количество указывается приставками ди-2, три-3, тетра-4, пента-5 и т.д. название радикала от количества атомов углерода в нём + суффикс илНапример , 2,2-диметил или 2,3,3,5-тетраметил.
Слайд 20
Порядок построения названия
4. Записать корень, соответствующий числу атомов
углерода в главной цепи.
5. Если есть двойная связь, то
после корня поставить суффикс –ен с указанием положения связи в цепидля тройной связи использовать суффикс –ин. Если кратных связей нет – суффикс -ан
Слайд 21
Таким образом, в названии разветвленного алкана
корень+суффикс –
название нормального алкана (греч. числительное+суффикс "ан"), приставки – цифры и
названия углеводородных радикалов.Пример построения названия:
Слайд 22
Назовём полученные изомеры
СН3 – СН2 – СН2 –
СН2 – СН2 – СН3
СН3 – СН2 – СН2
– СН2 – СН3СН3
СН3 – СН2 – СН2 – СН3
СН3 СН3
СН3
СН3 – СН2 – СН2 – СН3
СН3
н-гексан
2-метилпентан
2,3 – диметилбутан
2,2 - диметилбутан
Слайд 23
Химические свойства алканов
Так как все связи насыщены до
предела, для алканов характерны реакции
Замещение СН4 + Сl2 hv
CH3Cl + HClРазложение (крекинг)
C8H18 t C4H10 + C4H8
Отщепление (дегидрирование – отщепление водорода)
С2Н6 t C2H4 + H2
Горение 2С2Н6 + 5O2 = 4CO2 + 6H2O
Слайд 24
алкены
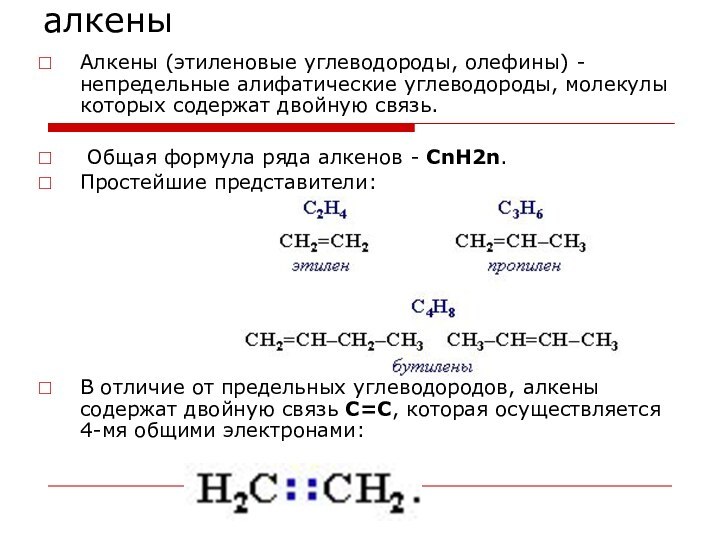
Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды,
молекулы которых содержат двойную связь.
Общая формула ряда алкенов
- CnH2n. Простейшие представители:
В отличие от предельных углеводородов, алкены содержат двойную связь С=С, которая осуществляется 4-мя общими электронами:
Слайд 26
пи-Связь
пи-Связь - ковалентная связь, возникающая при боковом перекрывании
негибридных р-АО. Такое перекрывание происходит вне прямой, соединяющей ядра
атомов
Слайд 28
Номенклатура алкенов
По систематической номенклатуре названия алкенов производят
от названий соответствующих алканов (с тем же числом атомов
углерода) путем замены суффикса –ан на –ен:2 атома С - этен; 3 атома С - пропен и т.д.
Главная цепь выбирается таким образом, чтобы она обязательно включала в себя двойную связь (т.е. она может быть не самой длинной).
Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение двойной связи, ставится обычно после суффикса –ен. Например:
Для простейших алкенов применяются также исторически сложившиеся названия:этилен (этен), пропилен (пропен), бутилен (бутен-1), изобутилен (2-метилпропен) и т.п.
В номенклатуре различных классов органических соединений наиболее часто используются следующие одновалентные радикалы алкенов:
Слайд 29
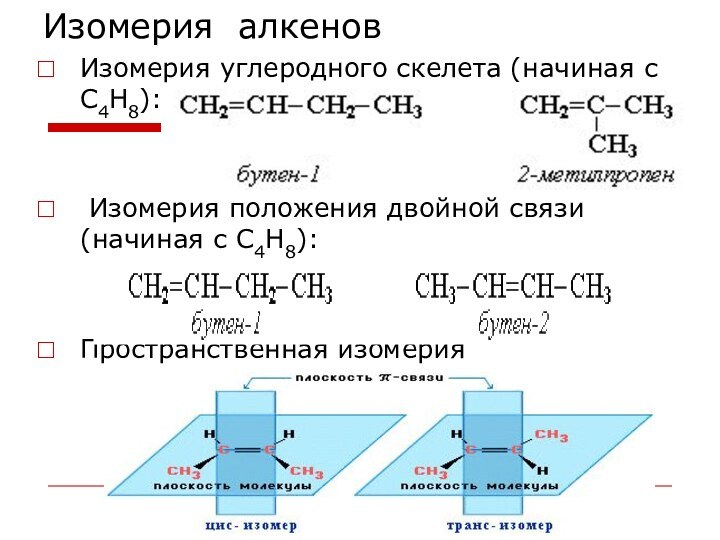
Изомерия алкенов
Изомерия углеродного скелета (начиная с С4Н8):
Изомерия положения двойной связи (начиная с С4Н8):
Пространственная изомерия
Слайд 30
Химические свойства алкенов.
Характерны реакции присоединения по двойной связи:
С
галогенами
CH2=CH2 + Br2(вод.) СH2 – CH2 +
Br:BrCH2 – CH2 дибромэтан.
Br Br
С водой (гидратация)
CH2=CH2 + Н2О кат С2Н5ОН
С водородом (гидрирование)
CH2=CH2 + Н2 = CH3 – CH3 этан
Слайд 31
Реакция полимеризации
CH2=CH2 + CH2=CH2 + CH2=CH2 + …
-СH2
– CH2- + -СH2 – CH2- + -СH2–CH2-
-СH2
– CH2-СH2–CH2-СH2–CH2- …Или: nCH2=CH2 (-СH2 – CH2- )n
этилен полиэтилен
Полимеризация – это …… (см. учебник стр. 208)
Мономер – это ……
Полимер – это ……
Слайд 32
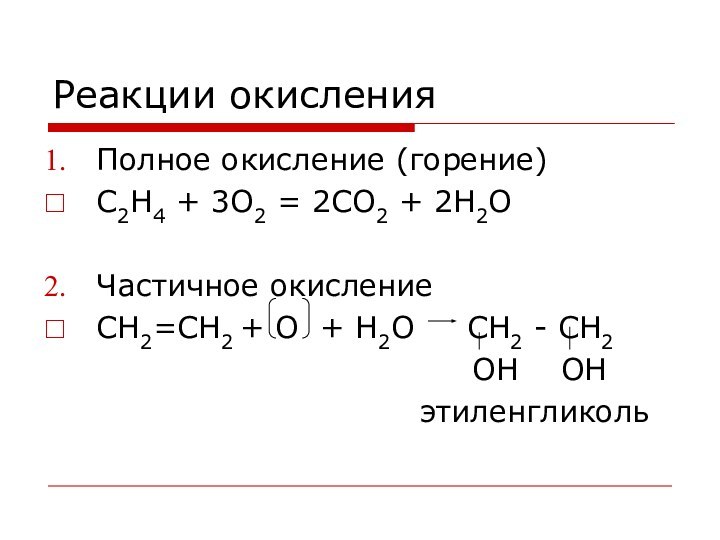
Реакции окисления
Полное окисление (горение)
С2Н4 + 3O2 = 2CO2
+ 2H2O
Частичное окисление
CH2=CH2 + О + H2O
CH2 - CH2ОН ОН
этиленгликоль
Слайд 33
алкины
Алкины (ацетиленовые углеводороды) – непредельные углеводороды, молекулы которых
содержат одну тройную связь.
Общая формула алкинов СnH2n-2.
Простейшие представители:
Тройную
связь осуществляют 6 общих электронов:
Слайд 35
Номенклатура алкинов
По систематической номенклатуре названия ацетиленовых углеводородов производят
от названий соответствующих алканов (с тем же числом атомов
углерода) путем замены суффикса –ан на –ин: 2 атома С - этин; 3 атома С - пропин и т.д.Главная цепь выбирается таким образом, чтобы она обязательно включала в себя тройную связь (т.е. она может быть не самой длинной).
Нумерацию углеродных атомов начинают с ближнего к тройной связи конца цепи. Цифра, обозначающая положение тройной связи, ставится обычно после суффикса –ин.
Например:
Для простейших алкенов применяются также исторически сложившиеся названия: ацетилен (этин), аллилен (пропин), кротонилен (бутин-1), валерилен (пентин-1).
В номенклатуре различных классов органических соединений наиболее часто используются следующие одновалентные радикалы алкинов:
Слайд 36
Химические свойства алкинов
Как и для этиленовых характерны реакции
присоединения, окисления.
Запишите в тетрадях уравнения реакций:
Гидрирования ацетилена
Полного окисления
ацетилена
Слайд 37
Функциональная группа – группа атомов, обеспечивающая химические свойства
органических веществ
Слайд 38
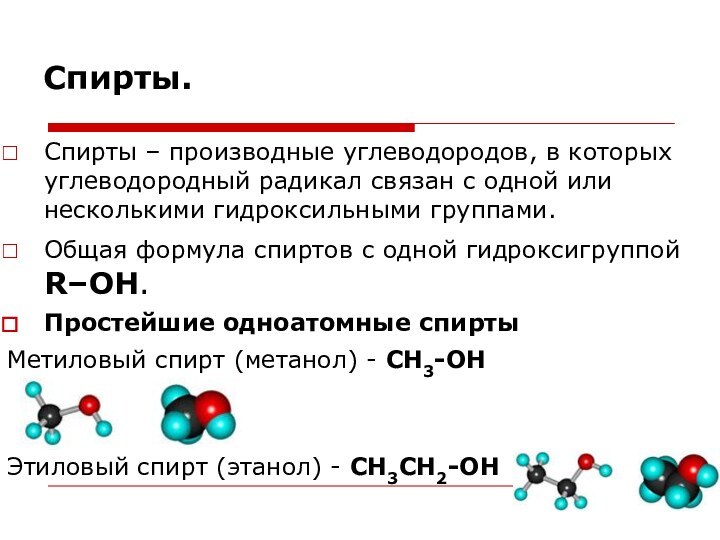
Спирты.
Спирты – производные углеводородов, в которых углеводородный радикал
связан с одной или несколькими гидроксильными группами.
Общая формула спиртов
с одной гидроксигруппой R–OH.Простейшие одноатомные спирты
Метиловый спирт (метанол) - CH3-OH
Этиловый спирт (этанол) - CH3CH2-OH
Слайд 39
Многоатомные спирты
Этиленгликоль – двухатомный спирт СН2 – СН2
ОН
ОНКак его можно получить?
Бесцветная густая жидкость тяжелее воды, имеет сладкий вкус. t кип - +197оС, замерзания – (-13оС)
Применяют в качестве антифриза – незамерзающей охлаждающей жидкости.
Слайд 40
Многоатомные спирты
Глицерин – трёхатомный спирт
СН2 – СН –
СН2
ОН ОН ОН
Густая сиропообразная бесцветная жидкость сладкого
вкуса. Хорошо растворяется в воде.Применяют при выделке кожи и отдельных тканей(предохраняет предметы от высыхания), в парфюмерии и медицине используют только водные растворы, так как безводный глицерин очень гигроскопичен и поэтому обезвоживает кожу.
Слайд 41 Химические свойства спиртов обусловлены наличием функциональной группы -
ОН
Взаимодействует:
С кислотами
С активными металлами
Горит с выделением углекислого газа и
воды (составьте уравнение реакции)Частично окисляется О
СН3–СН2–ОН + О СН3–С +Н2О
Н
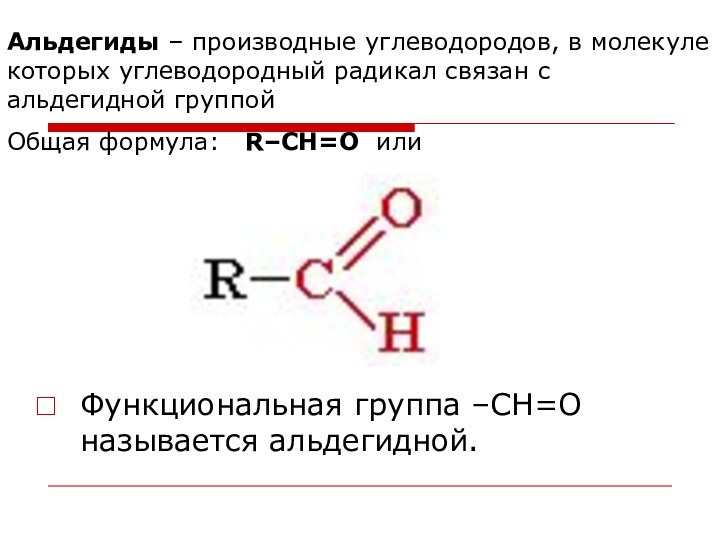
Слайд 42 Альдегиды – производные углеводородов, в молекуле которых углеводородный
радикал связан с альдегидной группой
Общая формула: R–CН=O или
Функциональная группа –СН=О
называется альдегидной.
Слайд 43
Карбоновые кислоты
Карбоновые кислоты - органические соединения, содержащие одну
или несколько карбоксильных групп –СООН, связанных с углеводородным радикалом.
Простейшие карбоновые кислоты
Муравьиная кислота (метановая)
Уксусная кислота (этановая)
Пропионовая кислота (пропановая)
Слайд 44 Систематические названия кислот даются по названию соответствующего углеводорода
с добавлением суффикса -овая и слова кислота.
HCOOH метановая муравьиная
CH3COOH
этановая уксуснаяC2H5COOH пропановая пропионовая
C3H7COOH бутановая масляная
C4H9COOH пентановая валерьяновая
C5H11COOH гексановая капроновая
C15H31COOH пентадекановая пальмитиновая
C17H35COOH гептадекановая стеариновая
Общая формула предельных одноосновных кислот: СnH2n+1COOH
Слайд 45
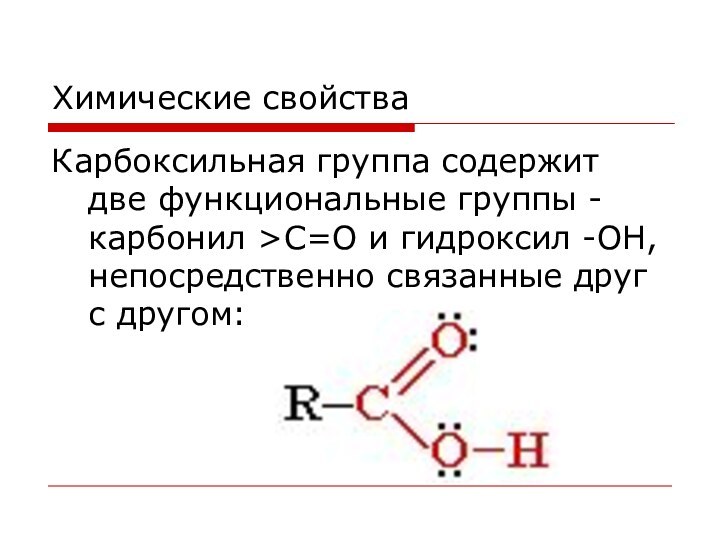
Химические свойства
Карбоксильная группа содержит две функциональные группы -
карбонил >С=О и гидроксил -OH, непосредственно связанные друг с
другом:
Слайд 46
Характерны реакции с:
Со спиртами (реакция этерификации)
Продуктом является сложный
эфир
Составьте уравнение реакции взаимодействия уксусной кислоты и этилового спирта.
С
металлами Составьте уравнение реакции взаимодействия уксусной кислоты и натрия, назовите продукты реакции (соли уксусной кислоты называются ацетатами)
Слайд 47
С солями более слабых карбоновых кислот
Составьте уравнение
реакции взаимодействия уксусной кислоты и карбоната натрия, назовите продукты
реакцииПолучить одноосновную карбоновую кислоту можно окислением альдегида
См. учебник стр. 217
Слайд 48
Жиры.
Жиры - сложные эфиры глицерина и высших одноатомных
карбоновых кислот.
В состав природных триглицеридов входят остатки насыщенных
кислот (пальмитиновой C15H31COOH, стеариновой C17H35COOH) и ненасыщенных (олеиновой C17H33COOH, линолевой C17H29COOH). Жиры содержатся во всех растениях и животных. Животные жиры (бараний, свиной, говяжий и т.п.), как правило, являются твердыми веществами с невысокой температурой плавления (исключение - рыбий жир). Жиры состоят главным образом из триглицеридов предельных кислот.
Растительные жиры - масла (подсолнечное, соевое, хлопковое и др.) - жидкости (исключение - кокосовое масло). В состав триглицеридов масел входят остатки непредельных кислот.
Слайд 49 Жидкие жиры превращают в твердые путем реакции гидрирования.
При этом водород присоединяется по двойной связи, содержащейся в
углеводородном радикале молекул масел.Продукт гидрогенизации масел - твердый жир (искусственное сало, саломас).
Маргарин - пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др.), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др.).
Продуктами щелочного гидролиза жиров являются мыла - соли высших карбоновых кислот и щелочных металлов. (Омыление жиров)
Слайд 50 Углеводы (сахара) - органические вещества, состав которых выражается
формулой Cx(H2O)y, где x и y > 3.
В
природе образуются в результате фотосинтеза.НЕКОТОРЫЕ ВАЖНЕЙШИЕ УГЛЕВОДЫ
Простые (негидролизующиеся) - Моносахариды:
глюкоза С6Н12О6
фруктоза С6Н12О6
рибоза С5Н10О5
Сложные (гидролизующиеся) - Олигосахариды: сахароза (дисахарид) С12Н22О11
Полисахариды: крахмал (С6Н10О5)n, целлюлоза (С6Н10О5)n
Слайд 51
Моносахариды
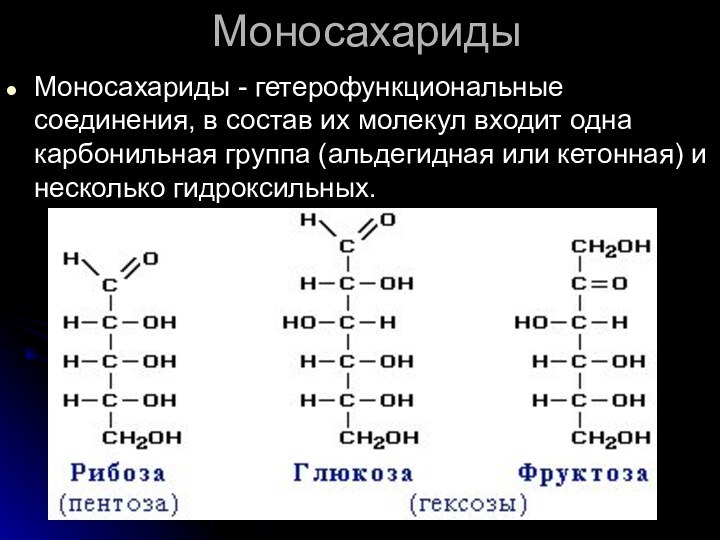
Моносахариды - гетерофункциональные соединения, в состав их
молекул входит одна карбонильная группа (альдегидная или кетонная) и
несколько гидроксильных.
Слайд 52
Дисахариды.
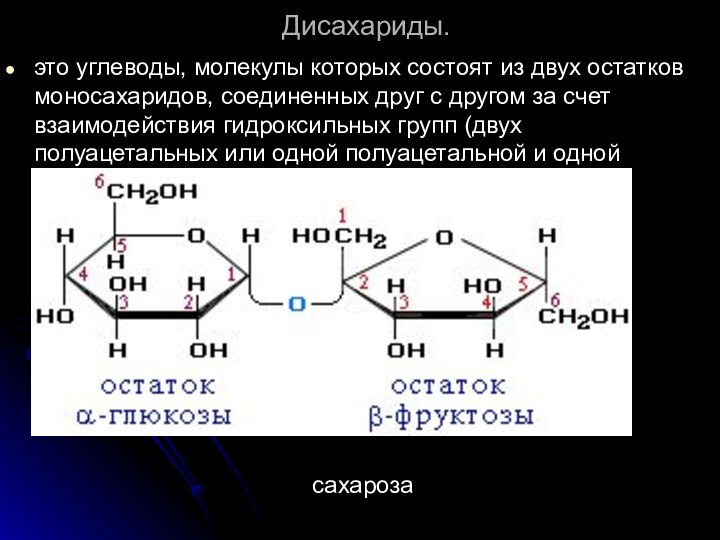
это углеводы, молекулы которых состоят из двух остатков
моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных
групп (двух полуацетальных или одной полуацетальной и одной спиртовой).сахароза
Слайд 53
Крахмал
В его состав входят:
амилоза (внутренняя часть крахмального
зерна) - 10-20%
амилопектин (оболочка крахмального зерна) - 80-90%
Макромолекула
амилозы представляет собой спираль, каждый виток которой состоит из 6 звеньев a-глюкозы. Амилопектин состоит из разветвленных макромолекул, молекулярная масса которых достигает 1 - 6 млн. Подобно амилопектину построен гликоген (животный крахмал).
Слайд 54 Аминокислоты – органические бифункциональные соединения, в состав которых
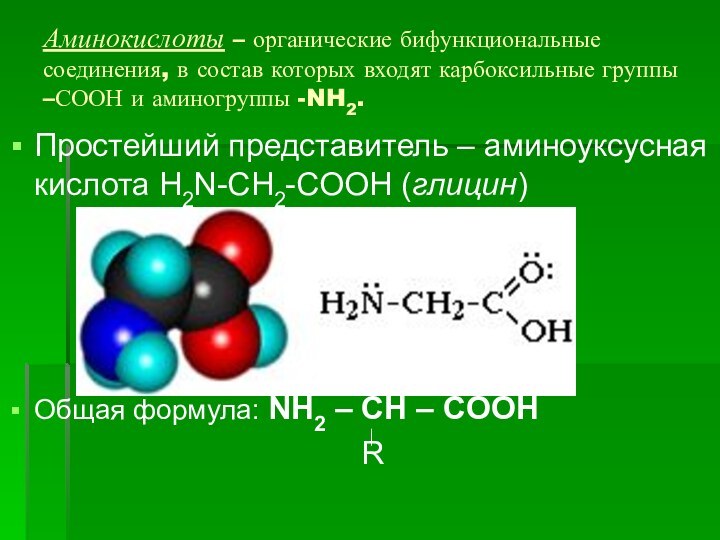
входят карбоксильные группы –СООН и аминогруппы -NH2.
Простейший представитель –
аминоуксусная кислота H2N-CH2-COOH (глицин)Общая формула: NH2 – CH – COOH
R
Слайд 55
Физические свойства
Аминокислоты – твердые кристаллические вещества с
высокой т.пл., при плавлении разлагаются. Хорошо растворимы в воде,
водные растворы электропроводны. Эти свойства объясняются тем, что молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе.
Слайд 56
Химические свойства
Аминокислоты проявляют свойства оснований за счет аминогруппы
и свойства кислот за счет карбоксильной группы, т.е. являются
амфотерными соединениями. Подобно аминам, они реагируют с кислотами с образованием солей аммония:H2N–CH2–COOH + HCl Cl- [H3N–CH2–COOH]+
Как карбоновые кислоты они образуют функциональные производные:
а) соли
H2N–CH2–COOH + NaOH H2N–CH2–COO- Na+ + H2O
б) сложные эфиры
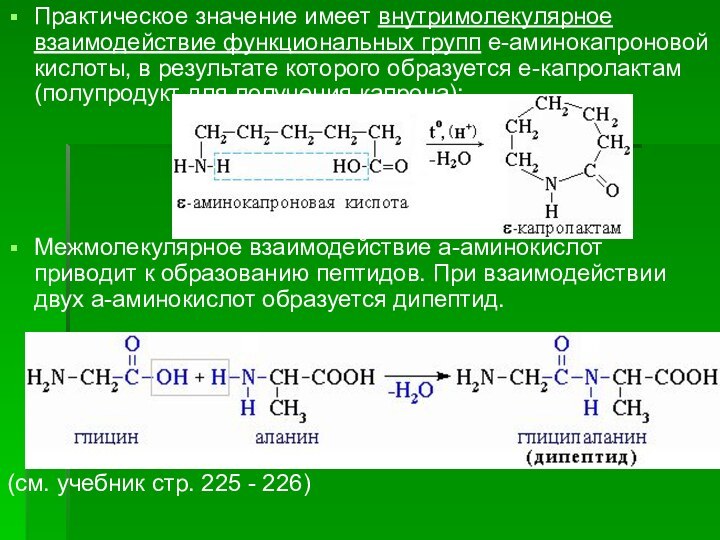
Слайд 57 Практическое значение имеет внутримолекулярное взаимодействие функциональных групп e-аминокапроновой
кислоты, в результате которого образуется e-капролактам (полупродукт для получения
капрона):Межмолекулярное взаимодействие a-аминокислот приводит к образованию пептидов. При взаимодействии двух a-аминокислот образуется дипептид.
(см. учебник стр. 225 - 226)
Слайд 59 Белки (полипептиды) - биополимеры, построенные из остатков a-аминокислот,
соединённых пептидными (амидными) связями.
Функции белков в природе :
каталитические
(ферменты); регуляторные (гормоны);
структурные (кератин шерсти, фиброин шелка, коллаген);
двигательные (актин, миозин);
транспортные (гемоглобин);
запасные (казеин, яичный альбумин);
защитные (иммуноглобулины) и т.д.
Слайд 61
Первичная структура
определенная
последовательность
a-аминокислотных
остатков
в полипептидной
цепи.
Слайд 62
Вторичная структура
конформация полипептидной
цепи, закрепленная
множеством водородных
связей
между группами
N-H и С=О.
Одна из моделей вторичной
структуры - a-спираль.
Слайд 63
Третичная структура -
форма закрученной
спирали в пространстве,
образованная главным
образом за счет
дисульфидных мостиков
-S-S-, водородных
связей, гидрофобных и ионных
взаимодействий.





























