образуются другие, отличающиеся от них по составу и (или)
строению.Химические реакции -
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть






















Химические реакции -
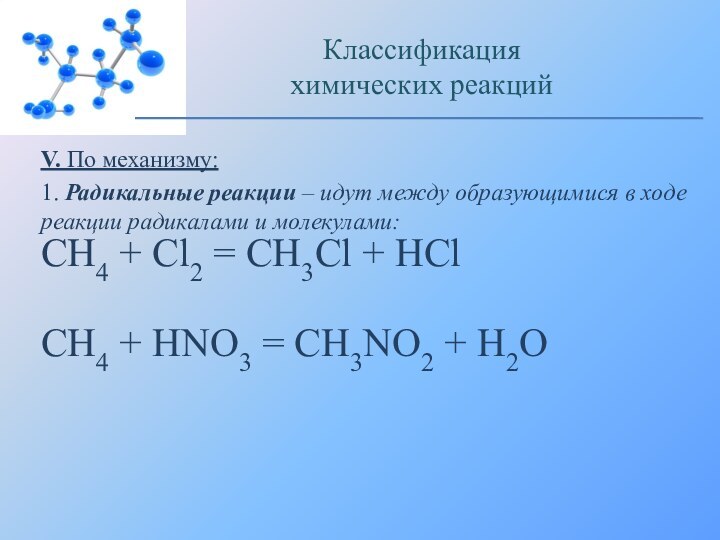
Классификация
химических реакций
Классификация
химических реакций
Sn (белое олово) Sn (серое олово)
Классификация
химических реакций
S + O2 = SO2
2SO2 + O2 = 2SO3
SO3 + H2O = H2SO4
Классификация
химических реакций
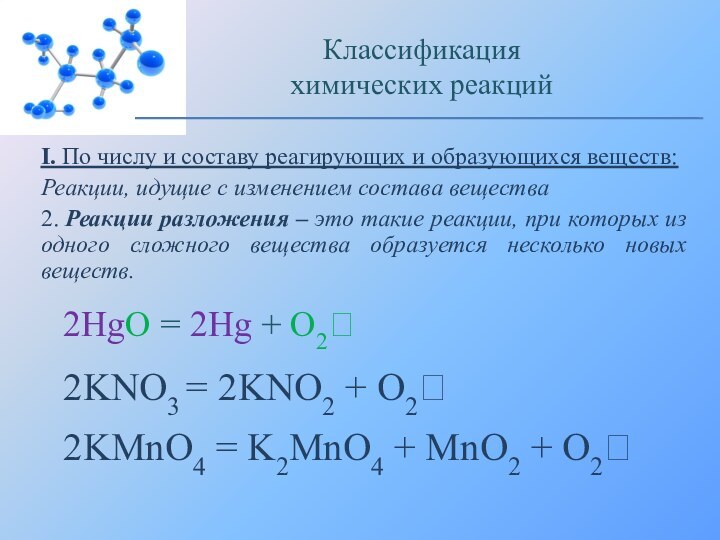
2HgO = 2Hg + O2
2KNO3 = 2KNO2 + O2
2KMnO4 = K2MnO4 + MnO2 + O2
Классификация
химических реакций
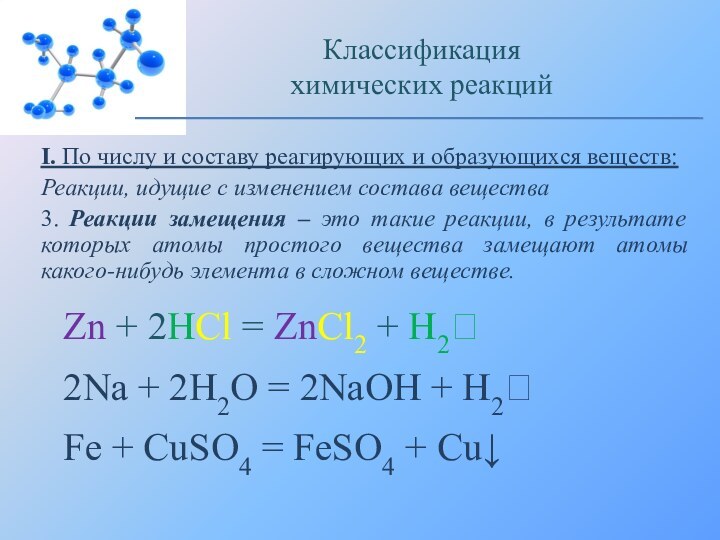
Zn + 2HCl = ZnCl2 + H2
2Na + 2H2O = 2NaOH + H2
Fe + CuSO4 = FeSO4 + Cu↓
Классификация
химических реакций
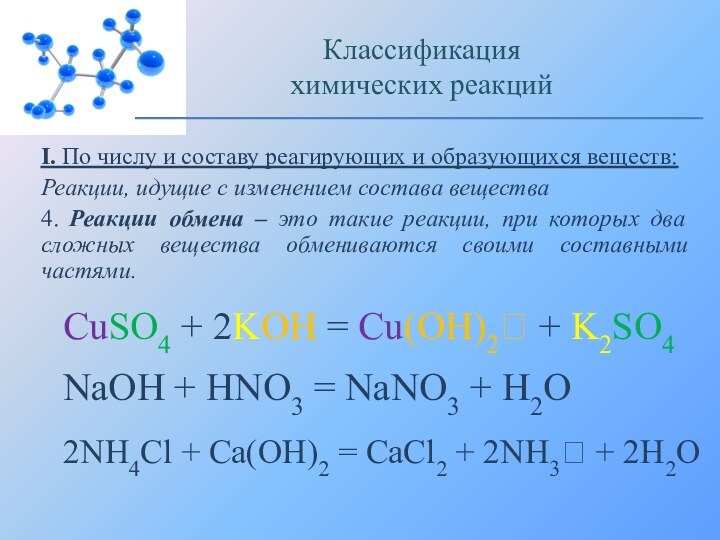
CuSO4 + 2KOH = Cu(OH)2 + K2SO4
NaOH + HNO3 = NaNO3 + H2O
2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3 + 2H2O
Классификация
химических реакций
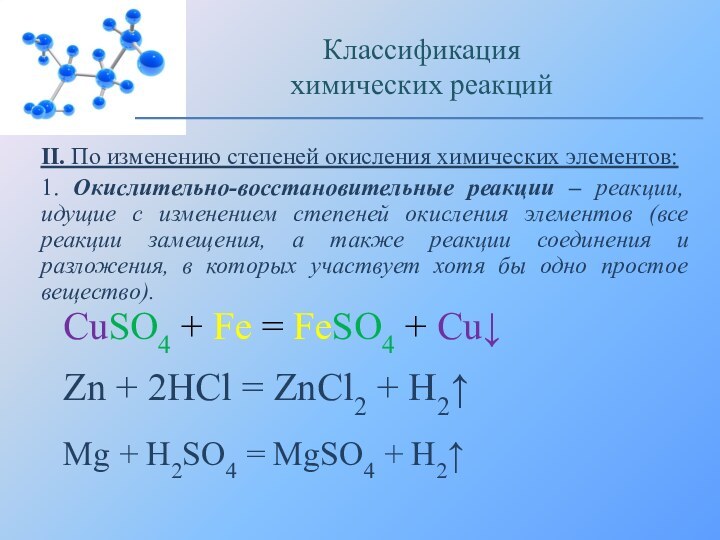
CuSO4 + Fe = FeSO4 + Cu↓
Zn + 2HCl = ZnCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
t
3H2 + N2 2NH3
N2O4 2NO2
CH4 + HNO3 = CH3NO2 + H2O
2HgO = 2Hg↓ + O2↑ - Q кДж
Классификация
химических реакций
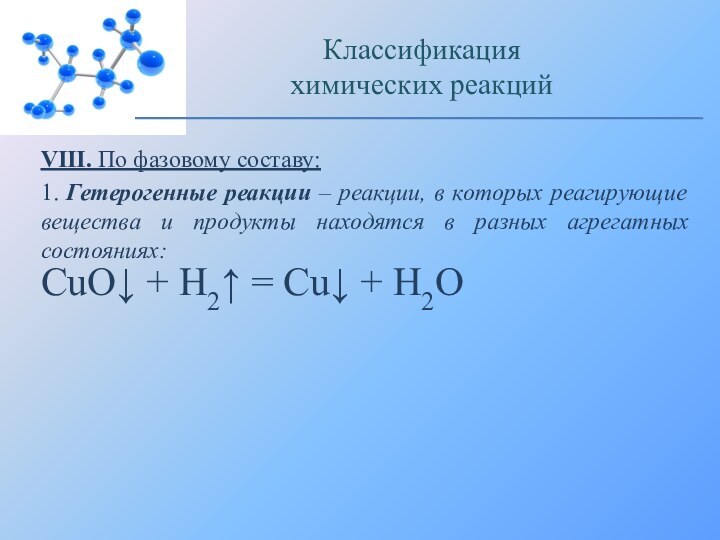
Классификация
химических реакций
CuO↓ + H2↑ = Cu↓ + H2O