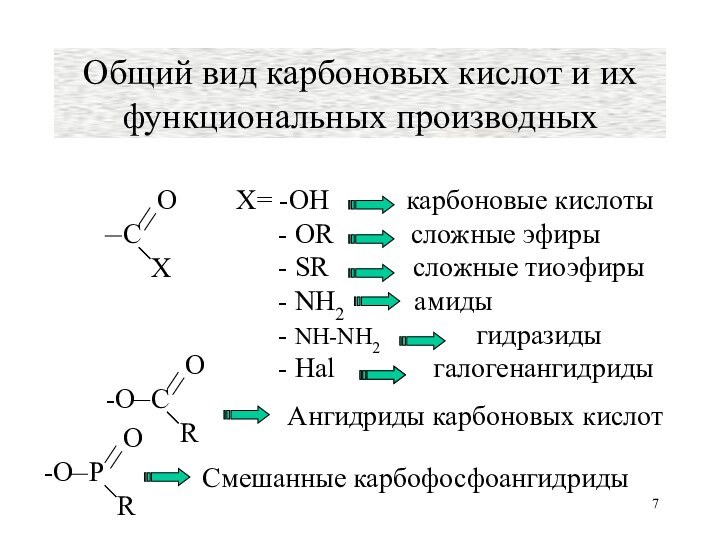
и тиоэфиры, амиды, гидразиды галогенангидриды и ангидриды) широко распространены
в природе.Работа функциональных групп этих классов лежит в основе различных процессов жизнедеятельности.
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть













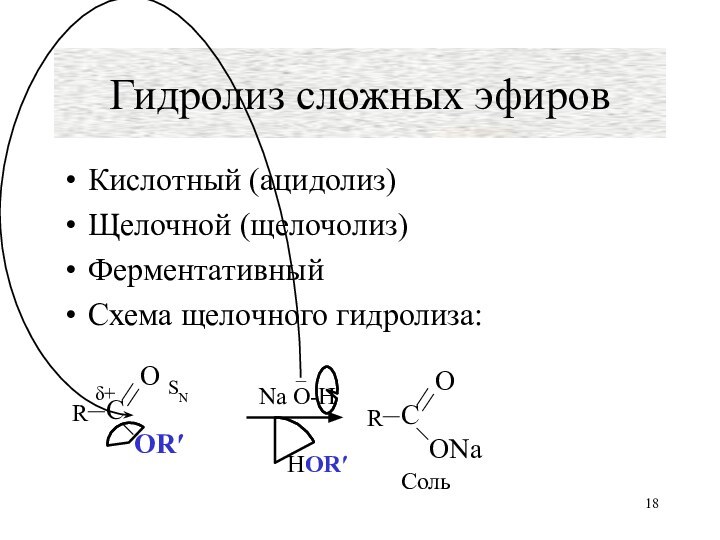
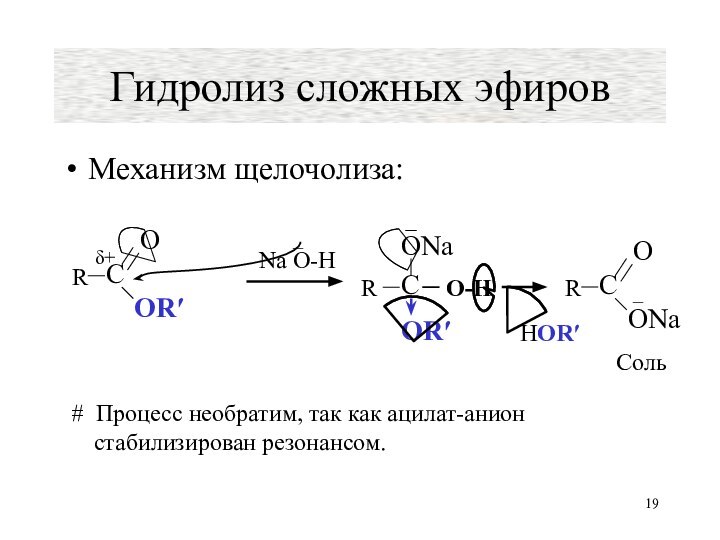


Актуальность
R-COOH / RCOO–
Кислотность карбоновых кислот