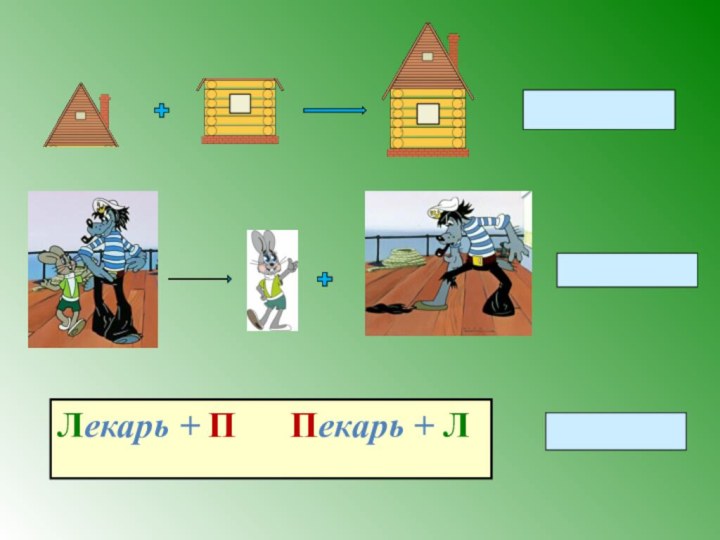
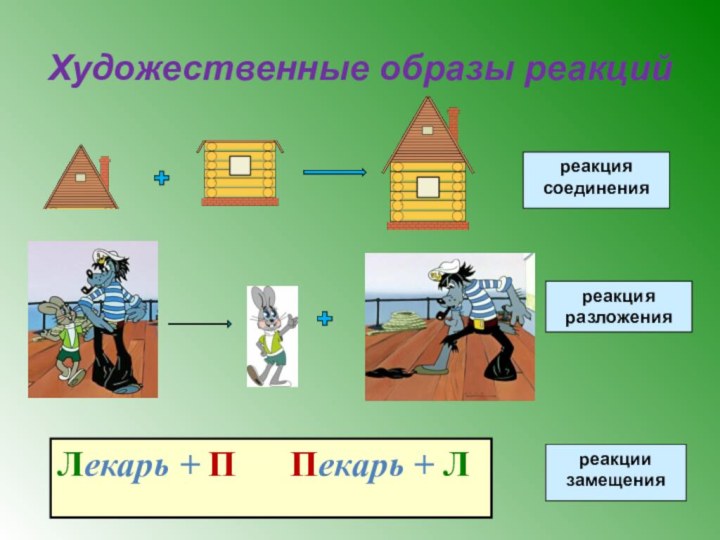
из одного или нескольких веществ веществ образуется одно сложное
веществво.2 Li + O2 = 2 Li2 O
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть















Оценивание: максимум 5б за верно расставленные коэффициенты
и указанные типы реакций.
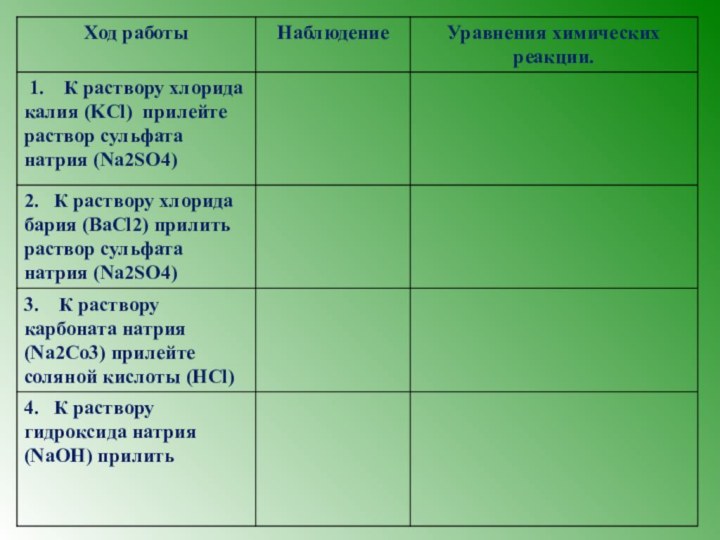
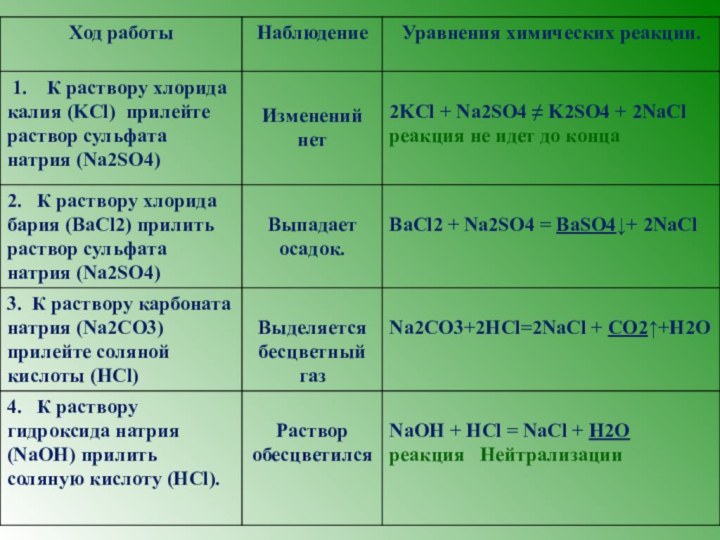
г) CaO + 2HCl → CaCl2 + H2O – реакция обмена, протекает до конца.
Оцените его и выставите в лист рефлексии
(колонка 5).
д) 2NaOH + Li2SO4 =2 LiOH + Na2SO4– реакция обмена, не идет до конца.
Оцените его и выставите в лист рефлексии
(колонка 5).