- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Химические свойства спиртов
Содержание
- 2. Проверка знаний.Работа по индивидуальным заданиям.Работа с терминами (тпо,стр.67, упр.2,3-1,2.)Работа с тренажером.
- 3. Тренажёр к уроку Представлена структурная формула
- 4. Шаг 1. Сколько углеродных атомов содержит основная цепь?645Шаг
- 5. Шаг 1. Сколько углеродных атомов содержит основная цепь?564Верно! Основная
- 6. 4-диметил-2-этил4-метил-2-этил2-метил-4-этилВерно! Нумерация основной цепи начинается с того конца, где ближе находится гидроксил. Название заместителей по алфавиту 4-метил-2-этил
- 7. Формула вещества:2-метил-4-этилпентанол-54-метил-2-этилгексанол-14-метил-2-этилпентанол-1Верно! Название спирта: 4-метил-2-этилпентанол-1.
- 8. Физические свойства спиртов1. Температуры плавления и кипения спиртов,
- 9. Химические свойства спиртов.1.ГОРЕНИЕ.Все органические вещества горят. Спирты
- 10. Запомним, друг, и я и ты, Чем
- 11. СВОЙСТВА ГИДРОКСИЛЬНОЙ ГРУППЫ СПИРТОВ.Взаимодействие с активными металлами.Взаимодействие
- 12. ДЕГИДРАТАЦИЯ (ВНУТРИМОЛЕКУЛЯРНАЯ И МЕЖМОЛЕКУЛЯРНАЯ)ОтнВНУТРИМОЛЕКУЛЯРНАЯ:
- 13. ОКИСЛЕНИЕ.Этанол окисляется в печени под действием фермента,
- 14. Окисление спирта до альдегида в пробиркеCH3CH2–OH
- 15. Установите соответствие между исходными веществами и продуктами
- 16. Скачать презентацию
- 17. Похожие презентации













Слайд 2
Проверка знаний.
Работа по индивидуальным заданиям.
Работа с терминами (тпо,стр.67,
упр.2,3-1,2.)
Слайд 3
Тренажёр к уроку
Представлена структурная формула спирта. Назовите
его по международной номенклатуре ИЮПАК.
Воспользуемся знаниями, полученными на уроке,
о номенклатуре спиртов
Слайд 4
Шаг 1. Сколько углеродных атомов содержит основная цепь?
6
4
5
Шаг 2. У
какого углеродного атома находятся заместители и как они называются?
4-диметил-2-этил
4-метил-2-этил
2-метил-4-этил
Шаг
3. Добавьте название основной цепи и укажите место гидроксила
2-метил-4-этилпентанол-5
4-метил-2-этилгексанол-1
4-метил-2-этилпентанол-1
Слайд 5
Шаг 1. Сколько углеродных атомов содержит основная цепь?
5
6
4
Верно! Основная цепь
должна содержать гидроксил и быть самой длинной. Она содержит
5 углеродных атомов.
Слайд 6
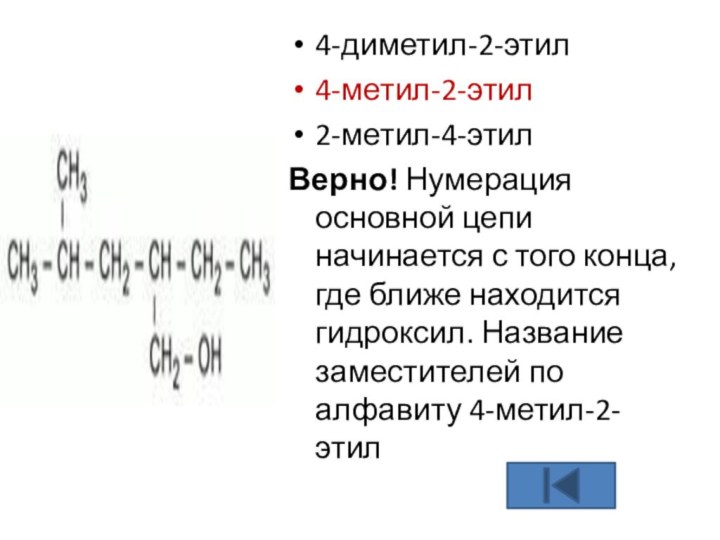
4-диметил-2-этил
4-метил-2-этил
2-метил-4-этил
Верно! Нумерация основной цепи начинается с того конца, где
ближе находится гидроксил. Название заместителей по алфавиту 4-метил-2-этил
Слайд 7
Формула вещества:
2-метил-4-этилпентанол-5
4-метил-2-этилгексанол-1
4-метил-2-этилпентанол-1
Верно! Название спирта:
4-метил-2-этилпентанол-1.
Слайд 8
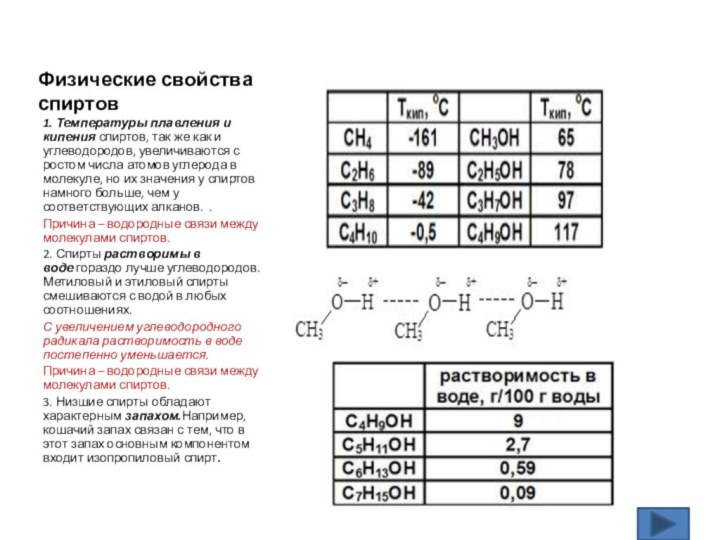
Физические свойства спиртов
1. Температуры плавления и кипения спиртов, так
же как и углеводородов, увеличиваются с ростом числа атомов
углерода в молекуле, но их значения у спиртов намного больше, чем у соответствующих алканов. .Причина – водородные связи между молекулами спиртов.
2. Спирты растворимы в воде гораздо лучше углеводородов. Метиловый и этиловый спирты смешиваются с водой в любых соотношениях.
С увеличением углеводородного радикала растворимость в воде постепенно уменьшается.
Причина – водородные связи между молекулами спиртов.
3. Низшие спирты обладают характерным запахом.Например, кошачий запах связан с тем, что в этот запах основным компонентом входит изопропиловый спирт.
Слайд 9
Химические свойства спиртов.
1.ГОРЕНИЕ.
Все органические вещества горят. Спирты –
не исключение.
С2Н5ОН + 3О2 = 2СО2 + 3Н2О. При горении
образуются углекислый газ и вода.Слайд 10 Запомним, друг, и я и ты, Чем отличаются спирты. В
них углерод и гидроксид,
И каждый спирт легко горит.
Слайд 11
СВОЙСТВА ГИДРОКСИЛЬНОЙ ГРУППЫ СПИРТОВ.
Взаимодействие с активными металлами.
Взаимодействие с
галогеноводородами
ДЕГИДРАТАЦИЯ (ВНУТРИМОЛЕКУЛЯРНАЯ И МЕЖМОЛЕКУЛЯРНАЯ)
1. Взаимодействие с активными металлами:
2CH3-CH2-OH + 2Na 2CH3-CH2-ONa + H2 этанол этилат натрия
Реакция с галогеноводородами:
C2H5OH + HBr C2H5Br + H2O
этанол бромо- бромэтан
водород
Слайд 12
ДЕГИДРАТАЦИЯ (ВНУТРИМОЛЕКУЛЯРНАЯ И МЕЖМОЛЕКУЛЯРНАЯ)
ОтнВНУТРИМОЛЕКУЛЯРНАЯ:
CH2-CH2 H2SO4, t
| | -----------> CH2=CH2 + H2O
H OH этилен
этанол
Межмолекулярная дегидратация
(с образованием простых эфиров)
<140 С, H2SO4 конц.
С2Н5 ─ О ─ Н + Н ─ О ─ С2Н5 С2Н5 ─ О ─ С2Н5 + H2O
этиловый спирт этиловый спирт диэтиловый эфир
Слайд 13
ОКИСЛЕНИЕ.
Этанол окисляется в печени под действием фермента, превращаясь
в этаналь – вещество, относящееся к классу альдегидов
Обычно организм
быстро окисляет этаналь дальше, переводя его с помощью другого фермента в уксусную кислоту.Если человек злоупотребил алкоголем, то организм не справляется с переработкой этаналя, и наступает отравление, называемое похмельем
Слайд 14
Окисление спирта до альдегида в пробирке
CH3CH2–OH
+ CuO → CH3CH=O + Cu + H2O
черный
розово-красныйВторичный спирт окислится в этих условиях до кетона:
(CH3)2CH–OH + CuO → (CH3)2C=O + Cu + H2O
изопропиловый спирт ацетон
(пропанол-2) (пропанон)
Слайд 15
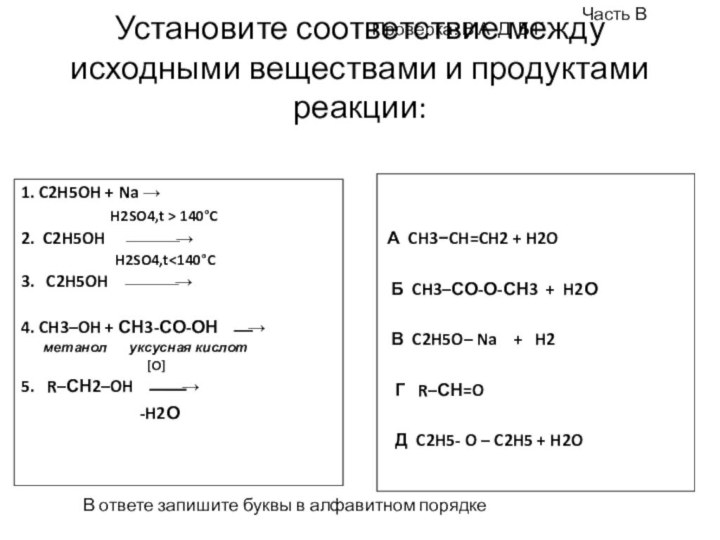
Установите соответствие между исходными веществами и продуктами реакции:
1.
C2H5OH + Na
H2SO4,t > 140C2. C2H5OH
H2SO4,t<140C
3. C2H5OH
4. CH3–OH + СН3-СО-ОН
метанол уксусная кислот
[O]
5. R–СН2–OH
-H2О
А CH3CH=CH2 + H2O
Б CH3–СО-О-СН3 + H2О
В C2H5O– Na + H2
Г R–СН=O
Д C2H5- O – C2H5 + H2O
Часть В
В ответе запишите буквы в алфавитном порядке
Проверка: В А Д Б Г





























