- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Химические связи . Кристаллические решетки
Содержание
- 2. ВИДЫ ХИМИЧЕСКИХ СВЯЗЕЙ.ИОННАЯ. (В.Коссель в 1916 г.)Катион+анион
- 3. NaCl MgCl2 AlCl3
- 4. Металлическая связьВозникает в Металле, или между двумя
- 5. Ковалентная полярная связьВозникает между двумя разными неметаллами. Механизм образования связи: ОБМЕННЫЙ
- 6. Подвиды ковалентной полярной связи1.ВОДОРОДНАЯ.Атом H + атом
- 7. 2.Вандер- Вальсово взаимодействие (межмолекулярное) . – это
- 8. КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ СВЯЗЬВозникает между двумя одинаковыми неметаллами (Cl2 , O2)Механизм : обменный.
- 9. Дз. 1.Тест А3 “Хим связь” (скинуть прорешенный
- 10. Типы кристаллических решеток
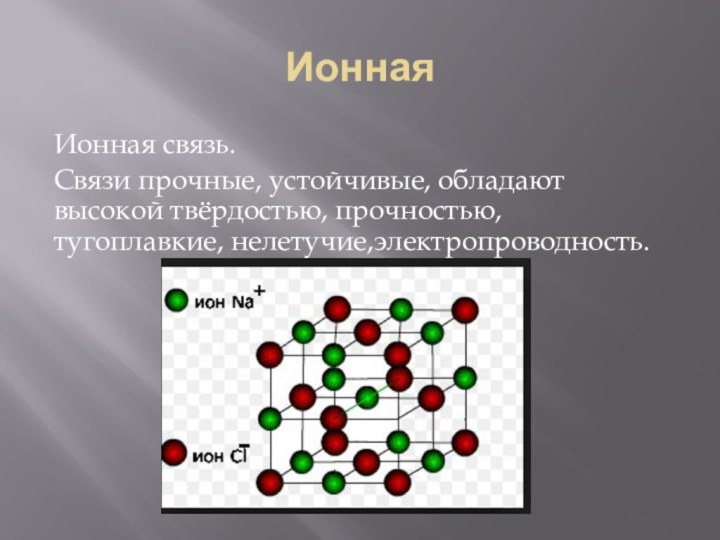
- 11. ИоннаяИонная связь.Связи прочные, устойчивые, обладают высокой твёрдостью, прочностью, тугоплавкие, нелетучие,электропроводность.
- 12. Атомная Ковалентная связь. САМАЯ ПРОЧНАЯ! Очень тугоплавкие
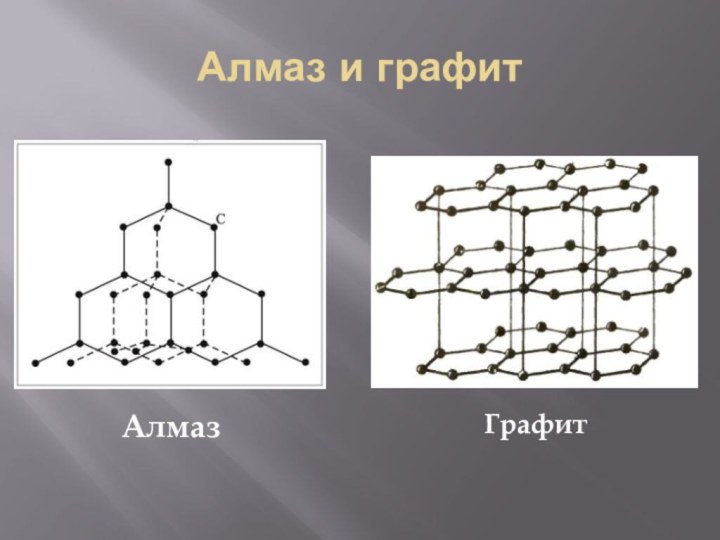
- 13. Алмаз и графитАлмазГрафит
- 14. МолекулярнаяКовалентные связи, водородные, Вандер-Вальсовы силы.Связи не прочные, легкоплавкие вещества, маленькая твердость, многие растворимы в воде.
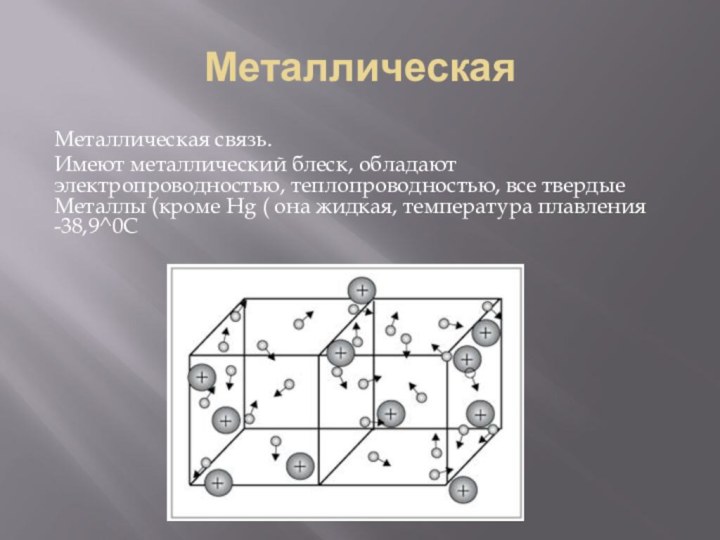
- 15. МеталлическаяМеталлическая связь.Имеют металлический блеск, обладают электропроводностью, теплопроводностью,
- 16. Скачать презентацию
- 17. Похожие презентации
ВИДЫ ХИМИЧЕСКИХ СВЯЗЕЙ.ИОННАЯ. (В.Коссель в 1916 г.)Катион+анион /(Ме+НеМе) в том числе NH4ClМеханизм образования:Донорно акцепторный.А – донорВ - акцептор