көр
Тағы да байқап көр
CnH2n+2
А
CnH2n
В
CnH2n-2
Г
CnH2n-6
Б
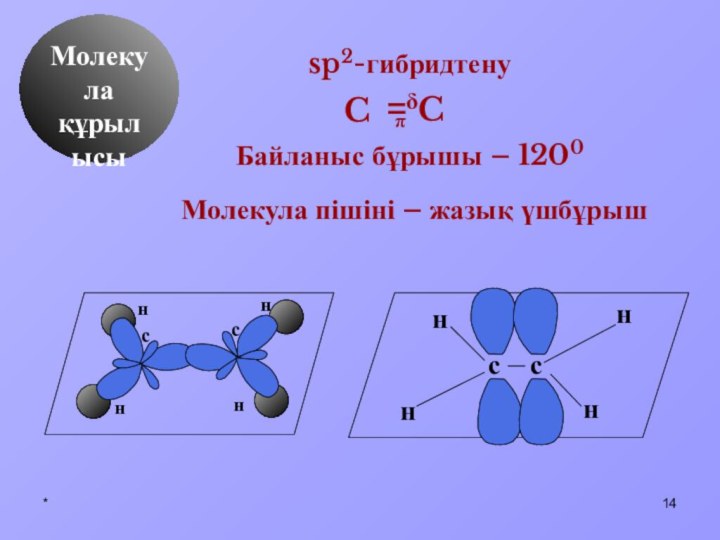
Алкендердің жалпы
формуласы
Жарайсың!
Тағы да байқап көр
Тағы
да байқап көр
Тағы да байқап көр
sp2,sp2,sp2
А
sp,sp,sp2
Б
Пропендегі көміртек
атомының
гибридтену түрі:
sp2,sp2,sp3
Г
sp2,sp,sp3
В
Сұрақ 2
Жарайсың!
Тағы да байқап көр
Тағы да байқап көр
Тағы да байқап көр
Көміртек
қаңқалы
А
Байланыстың
орналасуына
байланысты
Б
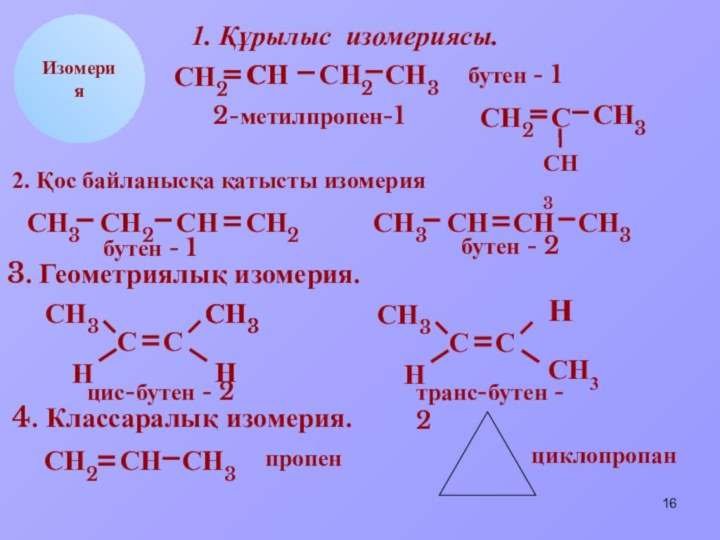
Алкендерге қандай
изомериялар тән емес?
геометриялық
функциональды топтың
орналасуына
байланысты
Сұрақ 3
В
Г
Жарайсың!
Тағы да байқап көр
Тағы да байқап көр
Тағы да байқап көр
орынбасу
тотығу
Б
Алкендерге тән емес
реакциялар
полимерлену
қосылу
Г
Сұрақ 4
А
В
Тағы да байқап көр
Жарайсың!
Тағы да байқап көр
Тағы да байқап көр
С6Н6
С6Н12
Массасы 4,2 г алкен
8 г бромды қосып алуға қабілетті.
Алкеннің молекулалық
формуласы қандай:
С12Н24
С10Н20
Г
В
Сұрақ 5
Б
А