- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Инвариативные задачи по химии для 8-9 классов (8-9 классы)
Содержание
- 2. Вычислить массовую долю каждого элемента в NaHCO3
- 3. Дано:NaHCO3W(Na)=23/84=0,2738или 27,38%W(C)=12/84=0,1429или 14,29%
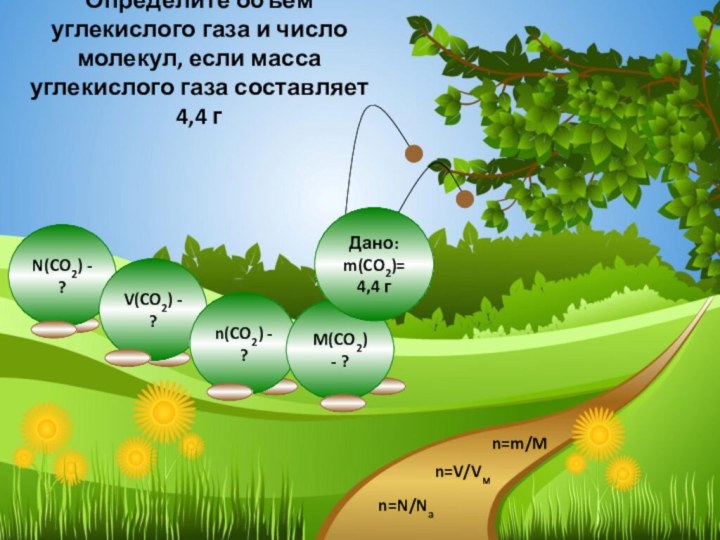
- 4. Определите объём углекислого газа и число молекул, если масса углекислого газа составляет 4,4 гn=m/Mn=V/Vмn=N/Na
- 5. Дано:m(CO2)=4,4 гn=m/Mn=V/Vмn=N/Na
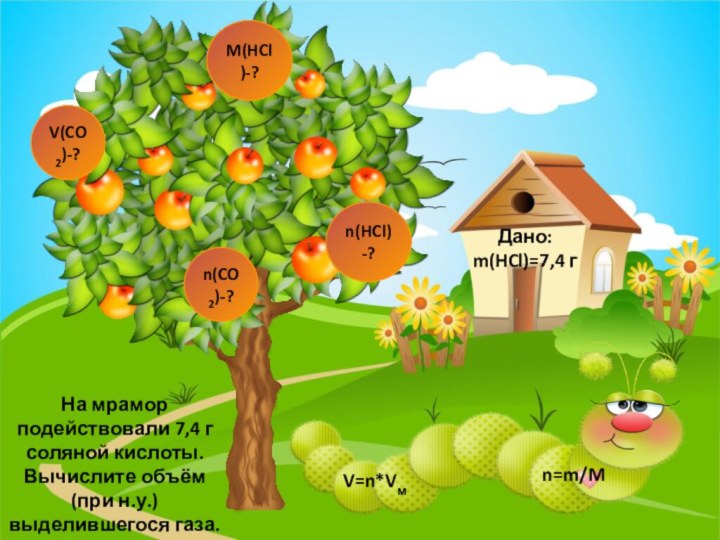
- 6. V(CO2)-?n(CO2)-?Дано: m(HCl)=7,4 гM(HCl)-?n(HCl)-?n=m/MНа мрамор подействовали 7,4 г соляной кислоты. Вычислите объём (при н.у.) выделившегося газа.V=n*Vм
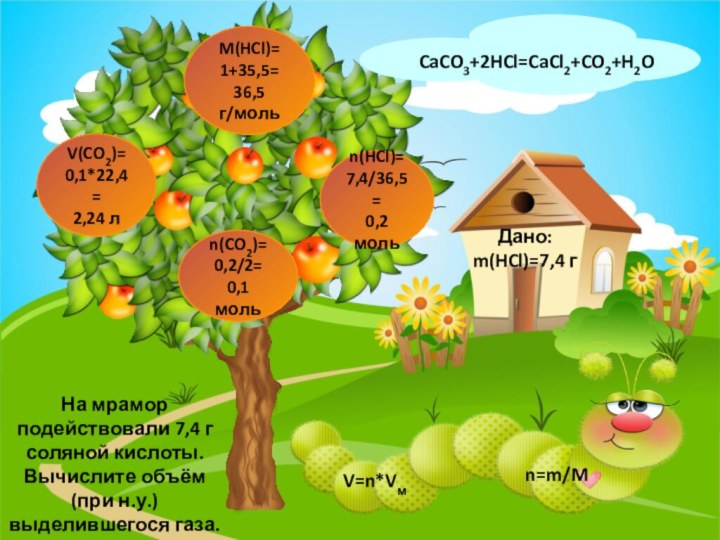
- 7. V(CO2)=0,1*22,4=2,24 лn(CO2)=0,2/2=0,1 мольCaCO3+2HCl=CaCl2+CO2+H2OДано: m(HCl)=7,4 гM(HCl)=1+35,5=36,5г/мольn(HCl)=7,4/36,5=0,2 мольn=m/MV=n*VмНа мрамор
- 8. V(CO2)-?n(CO2)-?n(HCl)-?Дано: mр(HCl)=20 г W(HCl)=0,71mв(HCl)-?n=m/Mn=V/VмW=mв/mрНа мел подействовали 20
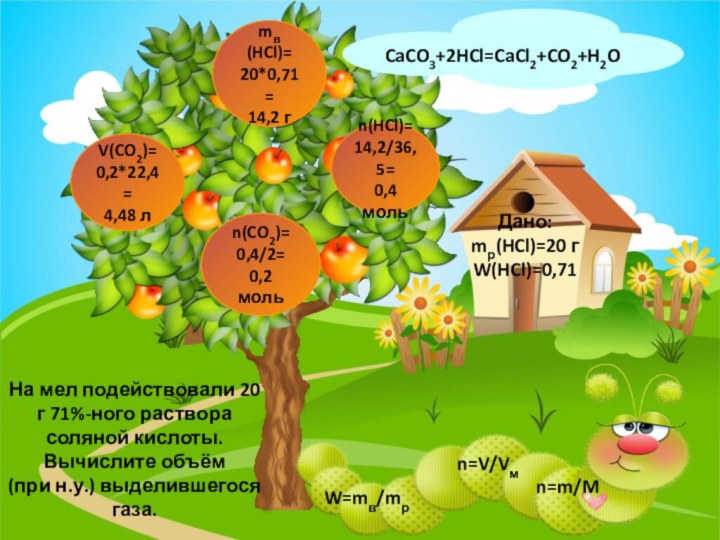
- 9. V(CO2)=0,2*22,4=4,48 лn(CO2)=0,4/2=0,2 мольCaCO3+2HCl=CaCl2+CO2+H2On(HCl)=14,2/36,5=0,4 мольДано: mр(HCl)=20 г W(HCl)=0,71mв(HCl)=20*0,71=14,2
- 10. Дано: mр(HCl)=100 г W(HCl)=0,2 m (CaCO3)=10
- 11. CaCO3+2HCl=CaCl2+CO2+H2O Дано: mр(HCl)=100 г W(HCl)=0,2 m (CaCO3)=10
- 12. mв(HCl)-?n(HCl)-?n(CaCl2)-?n(AgCl)-?m(AgCl)-?На мел подействовали 100 г 11%-ного раствора
- 13. CaCO3+2HCl=CaCl2+CO2+H2O Дано: mр(HCl)=100 г W(HCl)=0,11
- 14. Дано: mр(HCl)=100 г W(HCl)=0,2 m (CaCO3)=10
- 15. Скачать презентацию
- 16. Похожие презентации
Вычислить массовую долю каждого элемента в NaHCO3









Слайд 4 Определите объём углекислого газа и число молекул, если
масса углекислого газа составляет 4,4 г
Слайд 6
V(CO2)-?
n(CO2)-?
Дано:
m(HCl)=7,4 г
M(HCl)-?
n(HCl)-?
n=m/M
На мрамор подействовали 7,4 г соляной кислоты.
Вычислите объём
(при н.у.) выделившегося газа.
V=n*Vм
Слайд 7
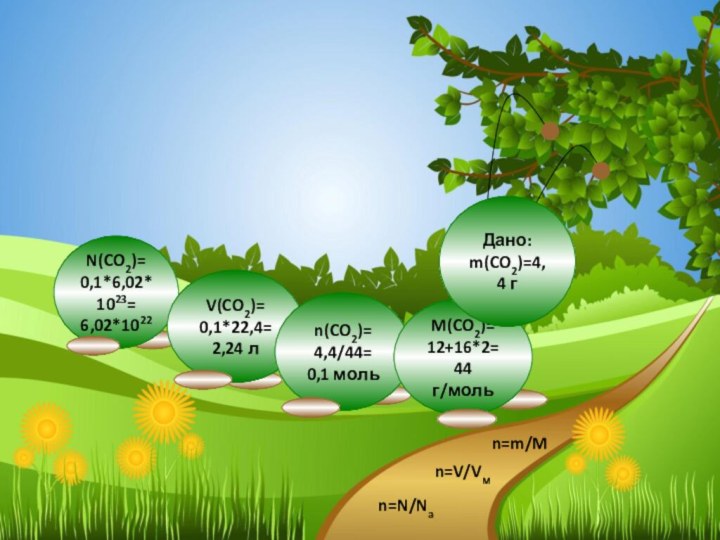
V(CO2)=
0,1*22,4=
2,24 л
n(CO2)=
0,2/2=
0,1 моль
CaCO3+2HCl=CaCl2+CO2+H2O
Дано:
m(HCl)=7,4 г
M(HCl)=
1+35,5=
36,5г/моль
n(HCl)=
7,4/36,5=
0,2 моль
n=m/M
V=n*Vм
На мрамор подействовали 7,4
г соляной кислоты. Вычислите объём
(при н.у.) выделившегося газа.
Слайд 8
V(CO2)-?
n(CO2)-?
n(HCl)-?
Дано:
mр(HCl)=20 г
W(HCl)=0,71
mв(HCl)-?
n=m/M
n=V/Vм
W=mв/mр
На мел подействовали 20 г 71%-ного раствора
соляной кислоты. Вычислите объём
(при н.у.) выделившегося газа.
Слайд 9
V(CO2)=
0,2*22,4=
4,48 л
n(CO2)=
0,4/2=
0,2 моль
CaCO3+2HCl=CaCl2+CO2+H2O
n(HCl)=
14,2/36,5=
0,4 моль
Дано:
mр(HCl)=20 г
W(HCl)=0,71
mв(HCl)=
20*0,71=
14,2 г
n=m/M
n=V/Vм
W=mв/mр
На мел подействовали
20 г 71%-ного раствора соляной кислоты. Вычислите объём (при
н.у.) выделившегося газа.
Слайд 10
Дано:
mр(HCl)=100 г
W(HCl)=0,2
m (CaCO3)=10 г
mв(HCl)-?
n(HCl)-?
n(CaCO3)-?
n(CO2)-?
V(CO2)-?
На мел массой 10
г подействовали 100 г 20%-ного раствора соляной кислоты. Вычислите
объём (при н.у.) выделившегося газа.
Слайд 11
CaCO3+2HCl=CaCl2+CO2+H2O
Дано:
mр(HCl)=100 г
W(HCl)=0,2
m (CaCO3)=10 г
На мел массой 10
г подействовали 100 г 20%-ного раствора соляной кислоты. Вычислите
объём (при н.у.) выделившегося газа.
Слайд 12
mв(HCl)-?
n(HCl)-?
n(CaCl2)-?
n(AgCl)-?
m(AgCl)-?
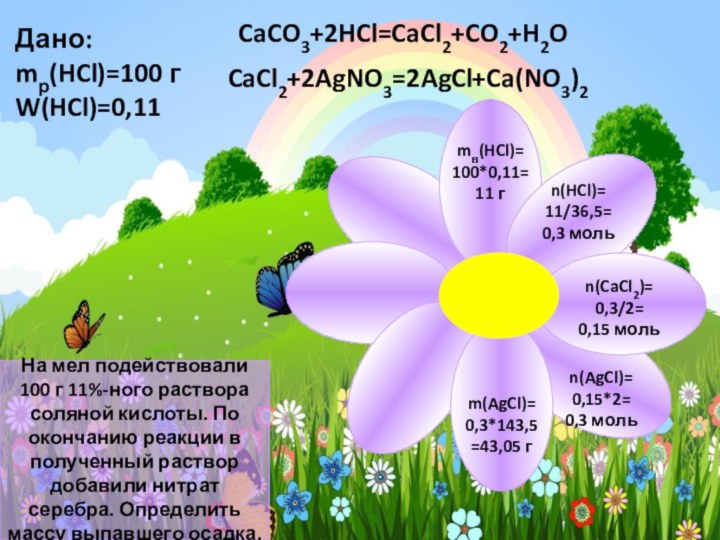
На мел подействовали 100 г 11%-ного раствора соляной
кислоты. По окончанию реакции в полученный раствор добавили нитрат
серебра. Определить массу выпавшего осадка.
Дано:
mр(HCl)=100 г
W(HCl)=0,11
Слайд 13
CaCO3+2HCl=CaCl2+CO2+H2O
Дано:
mр(HCl)=100 г
W(HCl)=0,11
На мел подействовали 100 г 11%-ного раствора
соляной кислоты. По окончанию реакции в полученный раствор добавили
нитрат серебра. Определить массу выпавшего осадка.CaCl2+2AgNO3=2AgCl+Ca(NO3)2