состоянии, а также плотные газы.
Чтобы получить, надо нагреть
тело до высокой температуры.Характер спектра зависит не только от свойств отдельных излучающих атомов, но и от взаимодействия атомов друг с другом.
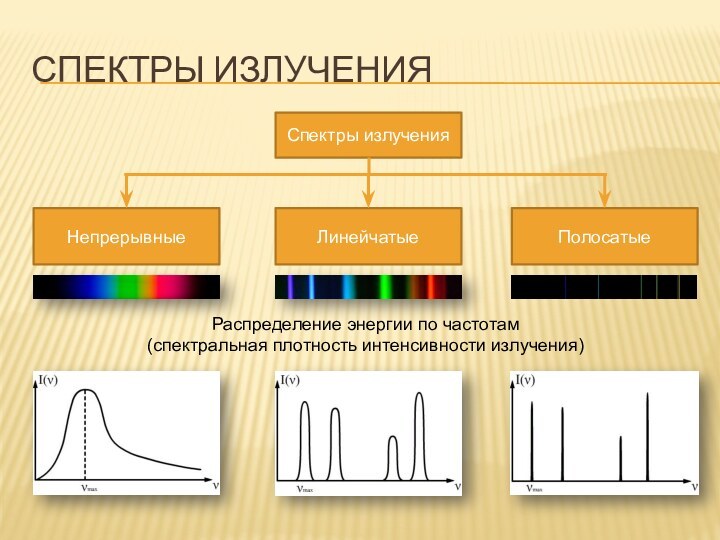
В спектре представлены волны всех длин и нет разрывов.
Непрерывный спектр цветов можно наблюдать на дифракционной решетке. Хорошей демонстрацией спектра является природное явление радуги.