- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Ток в жидкости
Содержание
- 2. Носителями свободных зарядов являются ионы электролитов, которые
- 3. В процессе растворения в жидкостях, атомы электролитов
- 4. электроны же уходят по металлическим проводам в
- 5. диэлектрики (дистиллированная вода)проводники (электролиты)полупроводники (расплавленный селен)Жидкости по степени электропроводности делятся на:
- 6. - это проводящая жидкость (растворы кислот , щелочей, солей и расплавленные соли). Электролит
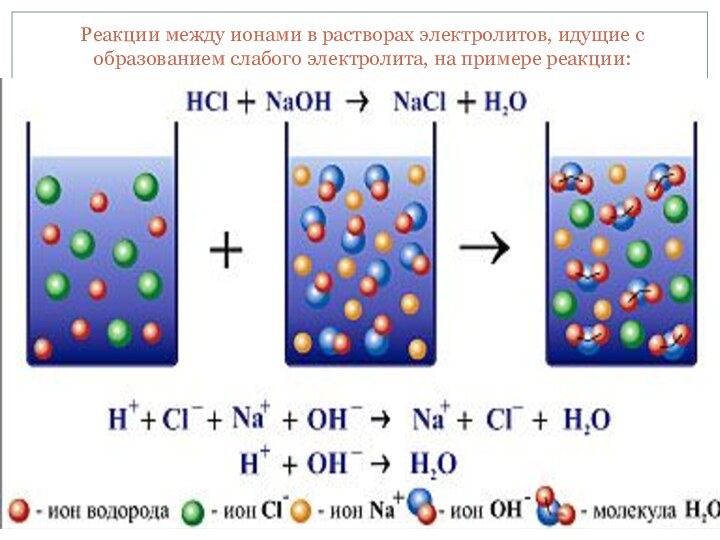
- 7. Реакции между ионами в растворах электролитов, идущие с образованием слабого электролита, на примере реакции:
- 8. Введение в раствор электролитов электродовСпособ создания электрического поля
- 9. Законы протекания тока в жидкости
- 11. выряяакррррррррррррррррррррррррр
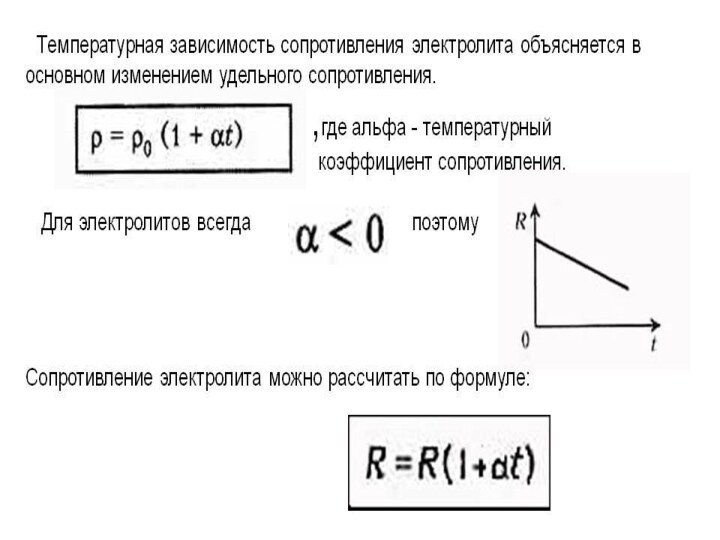
- 12. Зависимость сопротивления электролита от температуры
- 14. При постоянной температуре графиком, выражающим зависимость силы
- 15. а) электролитический метод получения чистых металлов (рафинирование).
- 16. б) посредством электролиза можно покрыть металлические предметы
- 17. Применениев) гальванопластика- изготовление рельефной копии предмета. Этот
- 18. г) получение оксидных защитных пленок на металлах (анодирование)Применение
- 19. д) электрохимическая обработка поверхности металлического изделия (полировка)Применение
- 20. е) электрохимическое окрашивание металлов (медь, латунь, цинк)Применение
- 21. ж) очистка воды – удаление из нее растворимых примесей, в результате получается так называемая мягкая водаПрименение
- 22. з) электрохимическая заточка режущих инструментов (хирургические ножи, бритвы)Применение
- 23. Почему нельзя прикасаться к неизолированным электрическим проводам голыми руками? Задания
- 24. Почему для гальванического покрытия изделия чаще используют никель и хром?Задания
- 25. Скачать презентацию
- 26. Похожие презентации
Носителями свободных зарядов являются ионы электролитов, которые и создают электрический ток.Основные носители заряда создающие ток в жидкости

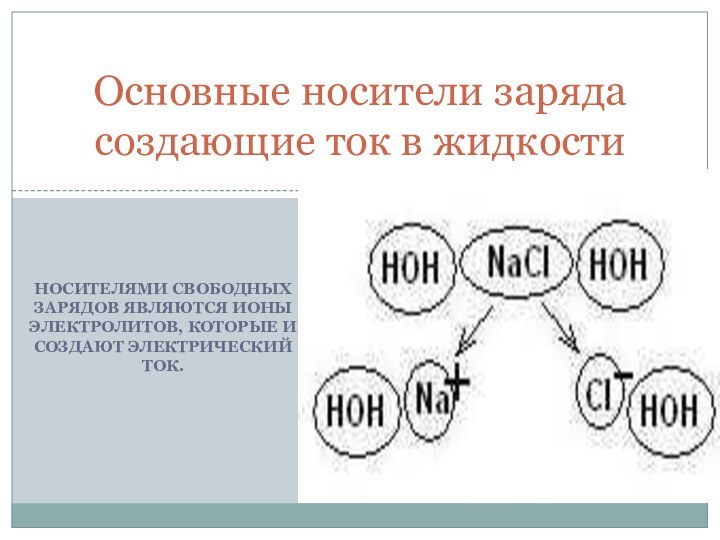



















Слайд 2 Носителями свободных зарядов являются ионы электролитов, которые и
создают электрический ток.
Слайд 3 В процессе растворения в жидкостях, атомы электролитов распадаются
на катионы и анионы. При соприкосновении с катодом положительные
ионы получают недостающие им электроны и выделяются в виде нейтральных атомов, а взамен электронов, нейтрализовавших ионы, новые электроны переходят от батареи к катоду. Точно так же отрицательные ионы при соприкосновении с анодом отдают ему свои избыточные электроны, превращаясь в нейтральные атомы;Механизм получения основных носителей
Слайд 4 электроны же уходят по металлическим проводам в батарею.
Таким образом, ток в электролите обусловлен движущимися ионами; на
электродах же происходит нейтрализация ионов и выделение их в виде нейтральных атомов (или молекул). Итак, электрический ток в электролитах представляет собой движение положительных и отрицательных ионов.Механизм получения основных носителей
Слайд 5
диэлектрики (дистиллированная вода)
проводники (электролиты)
полупроводники (расплавленный селен)
Жидкости по степени
электропроводности делятся на:
Слайд 6 - это проводящая жидкость (растворы кислот , щелочей,
солей и расплавленные соли).
Электролит
Слайд 7 Реакции между ионами в растворах электролитов, идущие с
образованием слабого электролита, на примере реакции:
Слайд 14 При постоянной температуре графиком, выражающим зависимость силы тока
от напряжения (вольт-амперная характеристика) для растворов электролитов, является прямая
линия. Эта прямая не проходит через начало координат, а “сдвинута” вправо. Это объясняется тем, что при электролизе происходит поляризация электродов, погруженных в раствор электролита, причем ЭДС поляризации имеет знак, противоположный знаку напряжения на электродах.Вольтамперная характеристика тока в жидкостях
Слайд 15
а) электролитический метод получения чистых металлов (рафинирование). Хорошим
примером является электролитическое очищение меди, драгоценных металлов - золото
и серебро.Применение
Слайд 16 б) посредством электролиза можно покрыть металлические предметы слоем
другого металла. Этот процесс называется гальваностегией. Особое техническое значение
имеют покрытия трудноокисляемыми металлами: никелирование и хромирование.Применение





























