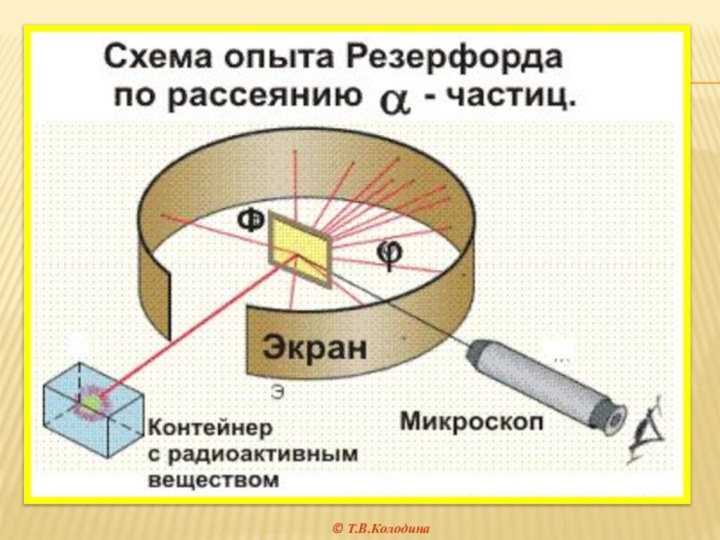
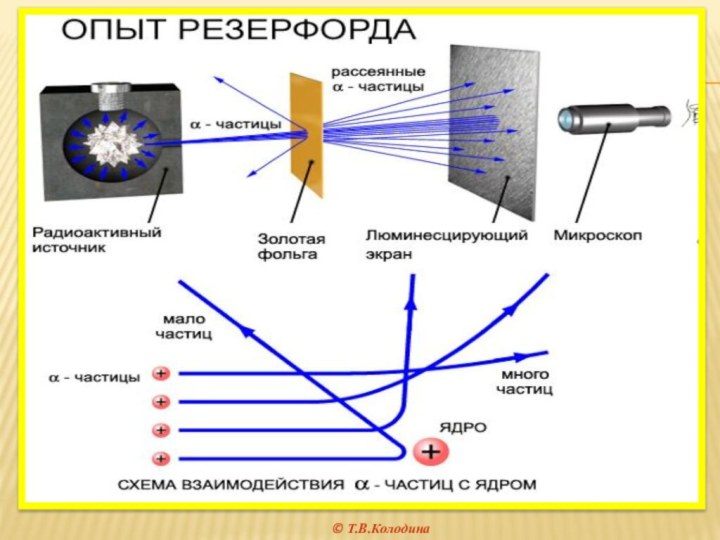
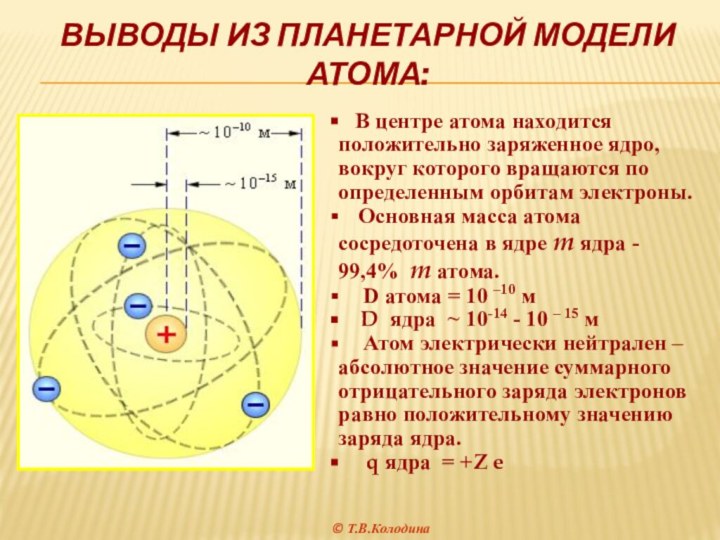
называется
а) джоулем;
б) электрон-вольт; в) электроном; г) квантом; д) ваттом.
2.Коэффициентом пропорциональности во второй из простых «великих» формул называется постоянной
а) Фарадея; б) Авогадро; в) Планка; г) Больцмана; д) Эйнштейна.
3.Явление вырывания электронов из вещества под действием света называют
а) фотосинтезом; б) ударная ионизацией; в) фотоэффектом;
г) электризацией; д) квантованием.
4.Максимальная кинетическая энергия фотоэлектронов …
а) линейно возрастает с увеличением длины волны и мощности излучения;
б) линейно возрастает с частотой света и не зависит от его интенсивности;
в) линейно взрастает с частотой света и его интенсивностью;
г) линейно убывает с частотой света и не зависит от его интенсивности;
д) линейно убывает с частотой света и его интенсивностью.
5.Какое из перечисленных ниже выражений объясняет фотоэффект?
© Т.В.Колодина