г. обнаружили, что радий самопроизвольно превращается в радон с
излучением α-частиц Открытие радиоактивных превращений атомных ядер
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть
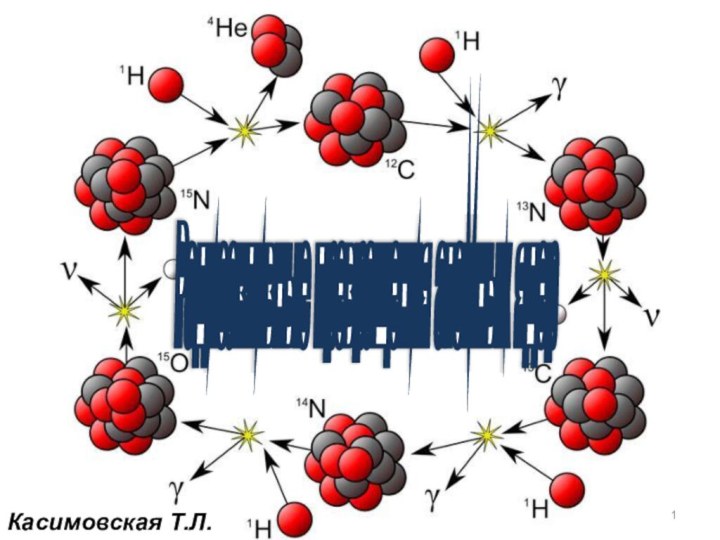

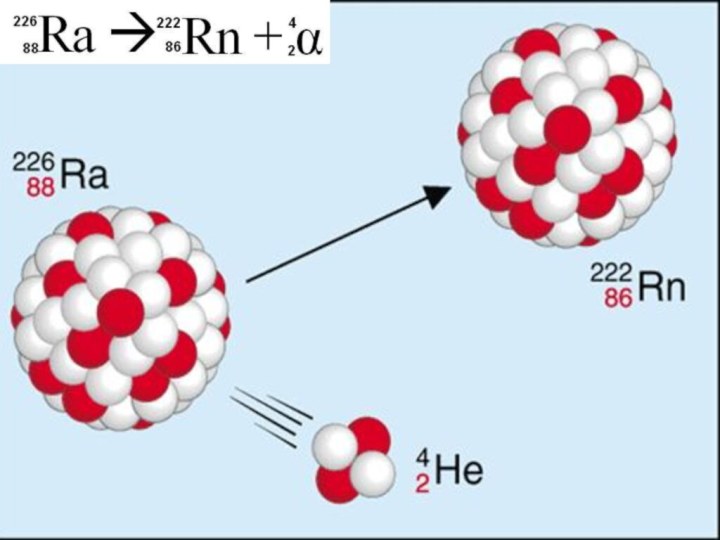











Открытие радиоактивных превращений атомных ядер
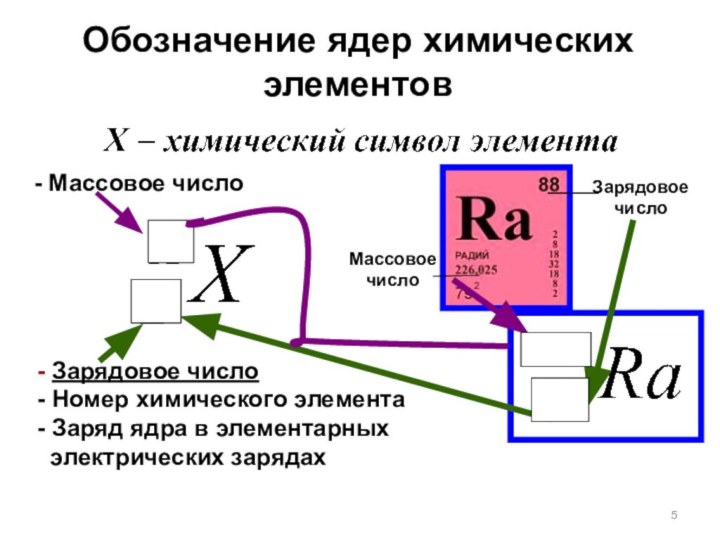
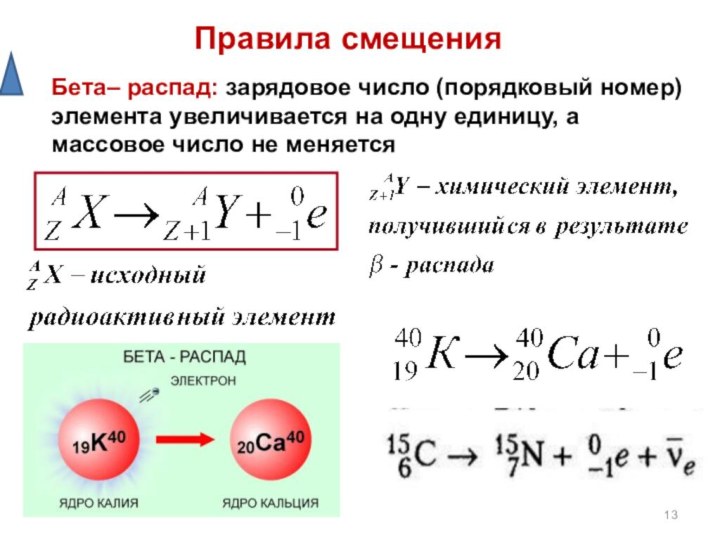
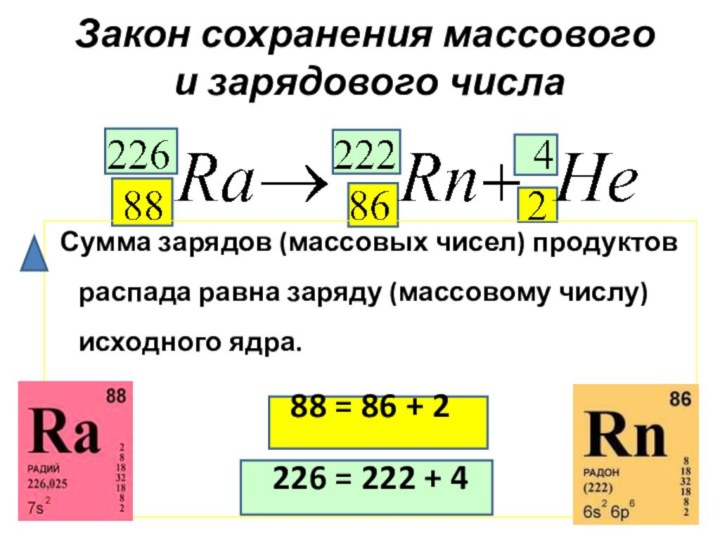
Зарядовое число
Массовое
число
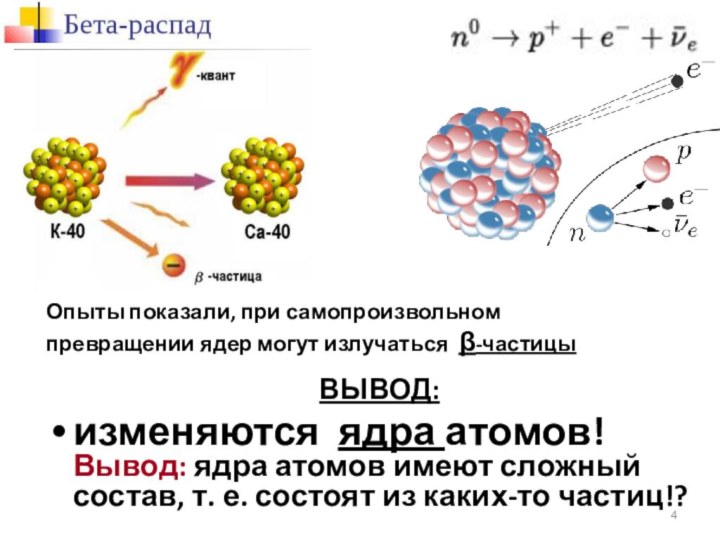
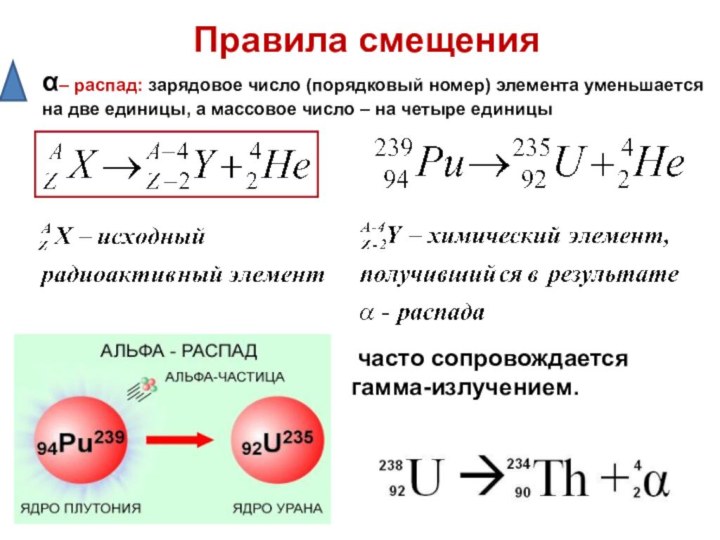
часто сопровождается гамма-излучением.
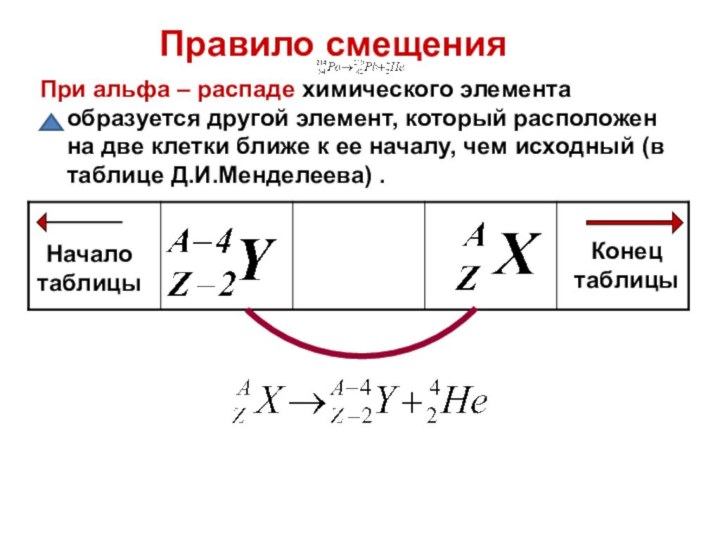
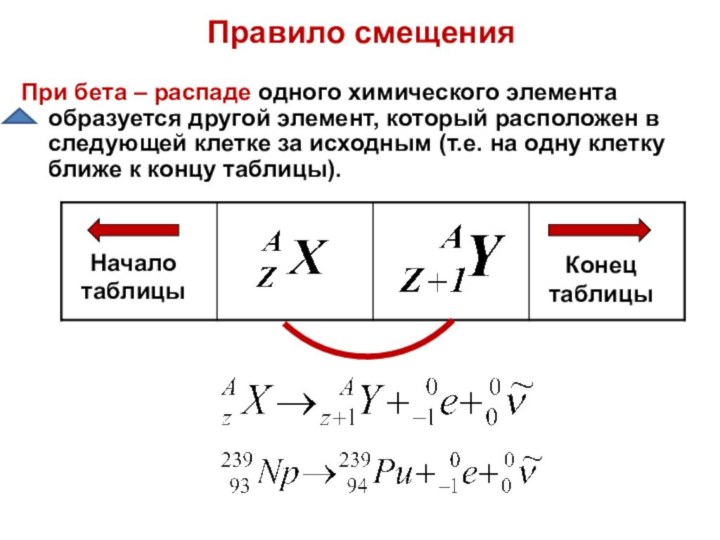
Правило смещения
Начало таблицы
Конец
таблицы
Начало таблицы
Конец
таблицы
В ходе операции пациент получает ионизирующее излучение из 192 источников кобальта-60…
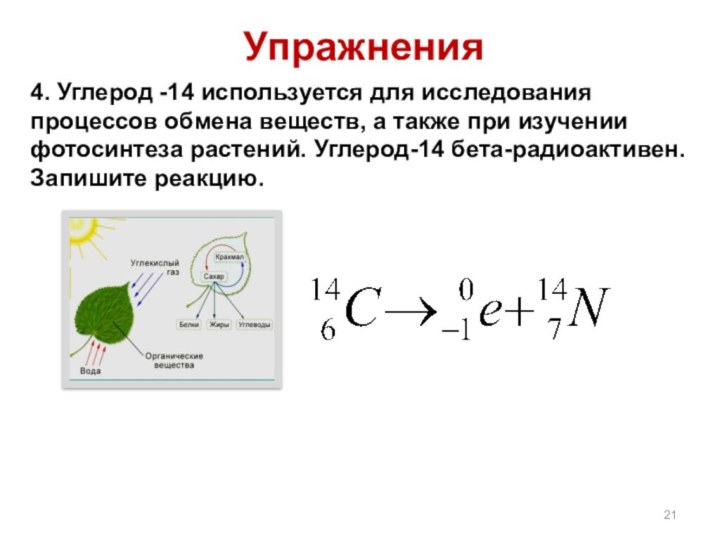
Упражнения
Кобальт-60
Упражнения
Упражнения