примененив к ним первый закон термодинамики.
Рассмотреть адиабатный процесс и
применить к нему первый закон термодинамики.
Цели
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть






























Цели
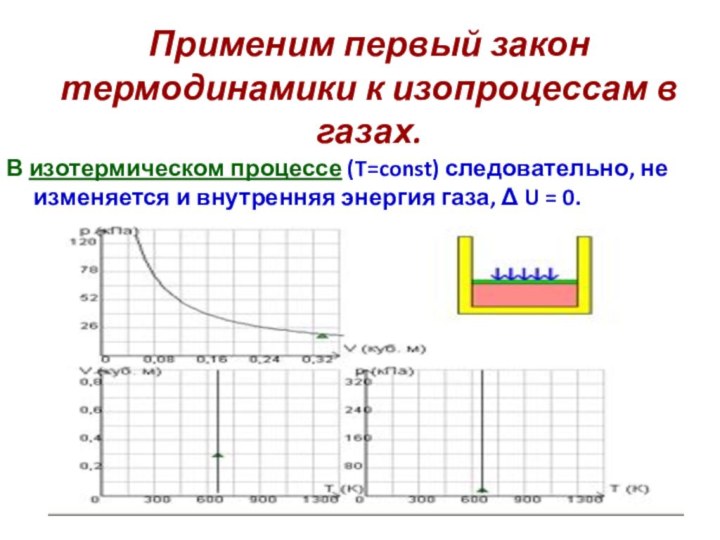
Первый закон термодинамики
ΔU = Q + Aвн
Вторая запись
первого закона термодинамики
Ответы:
В вертикально расположенном цилиндре под поршнем находится газ при Т=323 К, занимающий объём V1= 190 см 3 . Масса поршня М=120 кг, его площадь S=50 см 2 . Атмосферное давление р0 = 100 кПа. Газ нагревается на
T=100 К.
А. Определите давление газа под поршнем.
Б. На сколько изменится объём, занимаемый газом, после нагревания?
В. Найдите работу газа при расширении.
А. Р1 - ?
Б. V- ?
В. А= ?
A = –ΔU
A = CV (T2 – T1)
A<0
Ответ: 6 кДж.
Ответ: 750 Дж.