анализ фундаментальных исторических опытов подвести учащихся к пониманию квантовой
природы атомной системыЗадачи урока:
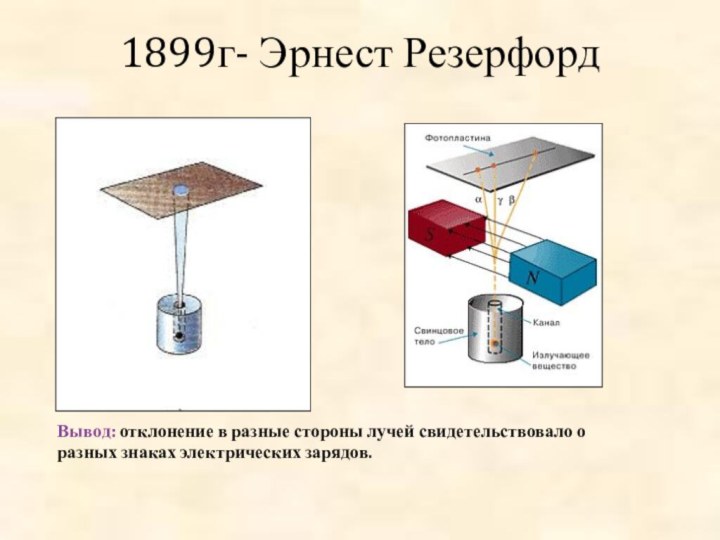
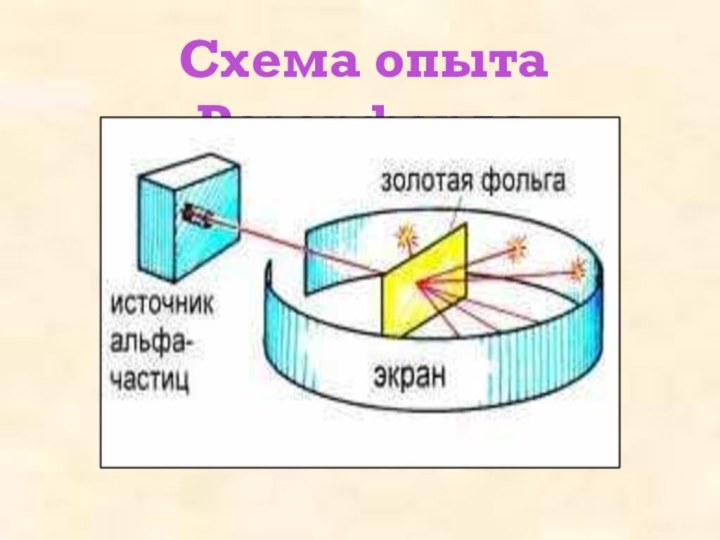
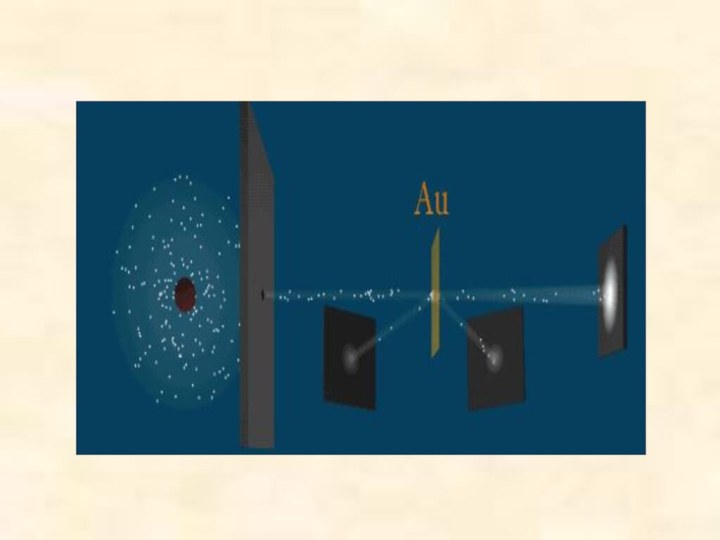
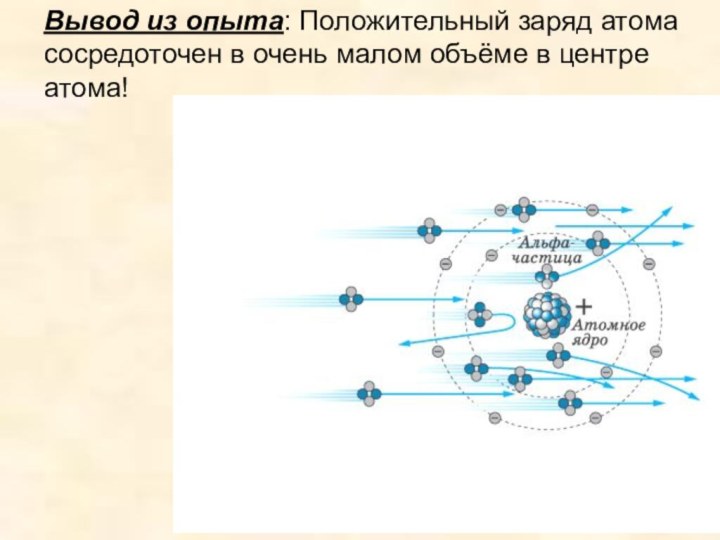
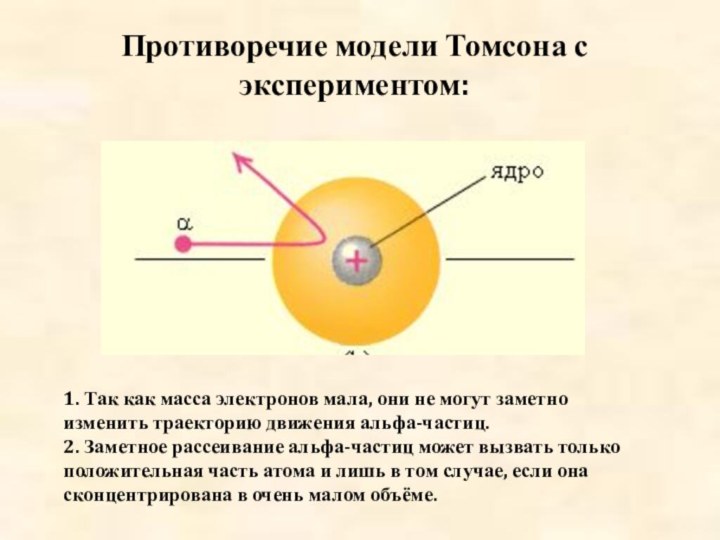
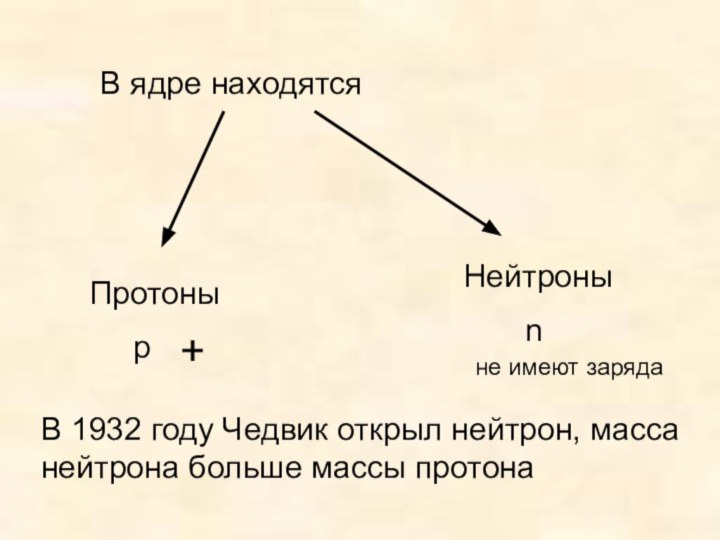
Познакомить учащихся с историей развития взглядов на строение атома, с фундаментальными опытами Резерфорда.
формировать у учащихся научное мировоззрение, умение выделять и описывать физические явления, строить гипотезы.
Формировать умение самостоятельно работать с различными источниками информации, обобщать материалы, развивать монологическую речь.
Показать роль крупных ученых в развитии науки.
Методы обучения:
Репродуктивные методы;
Демонстрации и материалы к уроку: ЭУ-8 класс, М-3, ЭУ-11 кл, модуль «Атомная физика», презентации, видеоролики.